Hỗn hợp X gồm Na và Ba có tỉ lệ mol 1 : 1. Hòa tan một lượng X vào nước được 3,36 lít H2 (đktc) và dung dịch Y. Cho 4,48 lít CO2 hấp thụ hết vào dung dịch Y thì thu được m gam kết tủa. Giá trị của m là:
A. 1,97 gam.
B. 39,4 gam.
C. 19,7 gam.
D. 3,94 gam.
 Giải bởi Vietjack
Giải bởi Vietjack
Trả lời:
Đặt số mol mỗi kim loại là x (mol).
Na + H2O → NaOH + ½ H2
x → x → 0,5x
Ba + 2H2O → Ba(OH)2 + H2
x → x → x
=>nH2 = 0,5x + x = 0,15 =>x = 0,1 mol
=>nOH- = x + 2x = 0,3 mol
*Hấp thụ 0,2 mol CO2 vào {0,3 mol OH-; 0,1 mol Ba2+; Na+}:
Ta thấy: nOH- : nCO2 = 0,3 : 0,2 = 1,5
=>Phản ứng tạo CO32- (a mol) và HCO3- (b mol)
CO2 + 2OH- → CO32- + H2O
CO2 + OH- → HCO3-
+ nCO2 = nCO32- + nHCO3- =>a + b = 0,2 (1)
+ nOH- = 2nCO32- + nHCO3- =>2a + b = 0,3 (2)
Giải hệ (1) và (2) được a = b = 0,1
Ta thấy: nBa2+ (0,1 mol) = nCO32- (0,1 mol) =>nBaCO3 = 0,1 mol
=>mBaCO3 = 0,1.197 = 19,7g
Đáp án cần chọn là: C
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Cho hỗn hợp X gồm x mol FeS2 và 0,025 mol Cu2S tác dụng vừa đủ với HNO3 loãng, đun nóng thu được dung dịch chỉ chứa muối sunfat của các kim loại và giải phóng khí NO duy nhất. Giá trị của x là
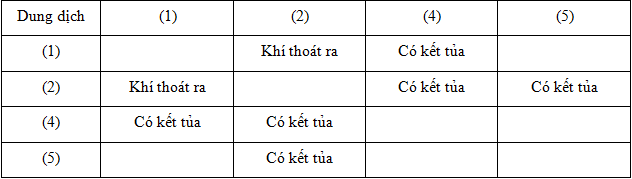
Các dung dịch (1), (3), (5) lần lượt là
1) NaHSO4 + NaHSO3
2) Na3PO4 + K2SO4
3) AgNO3 + Fe(NO3)2
4) C6H5ONa + H2O
5) CuS + HNO3
6) BaHPO4 + H3PO4
7) NH4Cl + NaNO2 (đun nóng)
8) Ca(HCO3)2 + NaOH
9) NaOH + Al(OH)3
10) MgSO4 + HCl.
Số phản ứng xảy ra là
Phần 1: Hòa tan hoàn toàn bằng dung dịch HCl dư thu được 1,792 lít H2 (đktc).
Phần 2: Nung trong không khí dư, thu được 2,84 gam hỗn hợp rắn chỉ gồm các oxit.
Khối lượng hỗn hợp X là:
Ion \[CO_3^{2 - }\]cùng tồn tại với các ion sau trong một dung dịch: