Cho các amin sau: CH3NH2, (C2H5)2NH, C3H7NH2, C2H5NH2, (C6H5)3N, (CH3)2NH, C6H5NH2. Số amin bậc II là
A. 4
B. 6
C. 7
D. 2
 Giải bởi Vietjack
Giải bởi Vietjack
Amin bậc II là amin có 2 nhóm hiđrocacbon thay thế cho 2H trong phân tử NH3
=> Các chất thuộc loại amin bậc II là (C2H5)2NH, (CH3)2NH.
Đáp án cần chọn là: D
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Amin là hợp chất khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH3
Cho các chất sau: CH3NH2, CH3NHCH3, (CH3)3N, CH3CH2NH2. Số chất thuộc loại amin bậc I?
I. Khái niệm, phân loại và danh pháp
1. Khái niệm
- Khi thay thế nguyên tử hiđro trong phân tử NH3 bằng gốc hiđrocacbon ta thu được amin.
- Ví dụ:
CH3–NH2; CH3–NH–CH3; ; CH2=CH–CH2NH2; C6H5NH2
2. Phân loại
Amin được phân loại theo hai cách thông dụng nhất:
a) Theo gốc hiđrocacbon:
– Amin mạch hở: CH3NH2, C2H5NH2, ...
– Amin thơm: C6H5NH2, CH3C6H4NH2, ...
– Amin dị vòng :![]() ;…
;…
b) Theo bậc amin:
– Bậc amin thường được tính bằng số gốc hiđrocacbon liên kết với nguyên tử nitơ.
Theo đó, các amin được phân loại thành:
|
Amin bậc I
|
Amin bậc II
|
Amin bậc III
|
|
R–NH2
|
R–NH–R’
|
|
|
R, R’ và R’’ là gốc hiđrocacbon
|
- Ví dụ: amin bậc I: CH3CH2CH2NH2
amin bậc II: CH3CH2NHCH3
amin bậc III:
3. Đồng phân
Amin thường có đồng phân về:
– Mạch cacbon.
– Vị trí nhóm chức.
– Bậc của amin.
Ví dụ: Ứng với công thức phân tử C3H9N có các đồng phân:
CH3 – CH2 – CH2 – NH2
CH3 – CH (NH2) – CH3
CH3 – NH – CH2 – CH3
4. Danh pháp
Tên của các amin thường được gọi theo tên gốc – chức (gốc hiđrocacbon với chức amin) và tên thay thế.
a) Tên pháp gốc – chức = Tên gốc hiđrocacbon + amin
Ví dụ : CH3NH2 (Metylamin), C2H5–NH2 (Etylamin), CH3CH(NH2)CH3 (Isopropylamin), ….
b) Tên thay thế = Tên hiđrocacbon + vị trí + amin
Ví dụ : CH3NH2 (Metanamin), C2H5–NH2 (Etanamin), CH3CH(NH2)CH3 (Propan - 2 - amin), ...
Tên gọi của một số amin
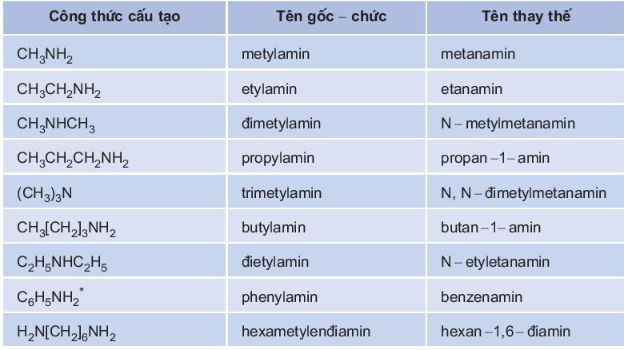
Lưu ý:
– Tên các nhóm ankyl đọc theo thứ tự chữ cái a, b, c, … + amin.
– Với các amin bậc 2 và 3, chọn mạch dài nhất chứa N làm mạch chính:
+ Có 2 nhóm ankyl → thêm 1 chữ N ở đầu.
Ví dụ : CH3–NH–C2H5 : N–metyletanamin.
+ Có 3 nhóm ankyl → thêm 2 chữ N ở đầu (nếu trong 3 nhóm thế có 2 nhóm giống nhau).
Ví dụ : CH3–N(CH3)–C2H5 : N, N–đimetyletanamin.
+ Có 3 nhóm ankyl khác nhau → 2 chữ N cách nhau 1 tên ankyl.
Ví dụ : CH3–N(C2H5 )–C3H7 : N–etyl–N–metylpropanamin.
– Khi nhóm –NH2 đóng vai trò nhóm thế thì gọi là nhóm amino.
Ví dụ : CH3CH(NH2)COOH (axit 2–aminopropanoic).
II. Tính chất vật lý
– Metylamin, đimetylamin, trimetylamin và etylamin là những chất khí có mùi khai khó chịu, tan nhiều trong nước.
- Các amin có phân tử khối cao hơn là những chất lỏng hoặc rắn, nhiệt độ sôi tăng dần và độ tan trong nước giảm dần theo chiều tăng của phân tử khối.
- Các amin thơm là chất lỏng hoặc rắn và dễ bị oxi hóa. Khi để trong không khí các amin thơm bị chuyển từ không màu thành màu đen vì bị oxi hóa.
- Các amin đều độc.

Cây thuốc lá chứa amin rất độc: nicotin
III. Cấu tạo phân tử và tính chất hóa học
1. Cấu tạo phân tử
- Trong phân tử amin, nguyên tử nitơ còn một cặp electron tự do chưa liên kết có thể tạo liên kết cho – nhận giống NH3.
Vì vậy các amin có tính bazơ tương tự NH3.
- Ngoài ra, nguyên tử N trong amin có số oxi hóa -3 như trong NH3 nên amin thường dễ bị oxi hóa. Các amin thơm dễ tham gia phản ứng thế vào nhân thơm do ảnh hưởng của đôi electron chưa tham gia liên kết ở nguyên tử nitơ.
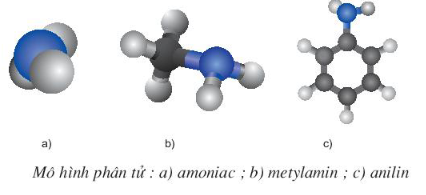
2. Tính chất hoá học :
a) Tính bazơ
- Các amin tan nhiều trong nước như metylamin, etylamin … có khả năng làm xanh giấy quỳ tím hoặc hồng phenolphtalein, có lực bazơ mạnh hơn NH3 nhờ ảnh hưởng của nhóm ankyl.
- Anilin có tính bazơ, nhưng dung dịch của nó không làm xanh giấy quỳ tím cũng không làm hồng phenolphtalein vì lực bazơ của nó yếu và yếu hơn NH3. Đó là do ảnh hưởng của gốc phenyl (tương tự phenol).
- Ta có thể so sánh lực bazơ như sau:
CH3 – NH2 > NH3 > C6H5 – NH2
Tác dụng với axit: R–NH2 + HCl → R–NH3Cl
Ví dụ:
CH3NH2 + HCl → CH3NH3Cl
Tác dụng dung dịch muối của các kim loại có hiđroxit kết tủa
Ví dụ :
3CH3NH2 + FeCl3 + 3H2O → Fe(OH)3↓ + 3CH3NH3Cl
Lưu ý : Khi cho muối của Cu2+, Zn2+, … vào dung dịch amin (dư) → hiđroxit kết tủa ® kết tủa tan (tạo phức chất).
b) Phản ứng thế ở nhân thơm của anilin :
Do ảnh hưởng của nhóm NH2 (tương tự nhóm –OH ở phenol), ba nguyên tử H ở các vị trí ortho và para so với nhóm –NH2 trong nhân thơm của anilin bị thay thế bởi ba nguyên tử brom :
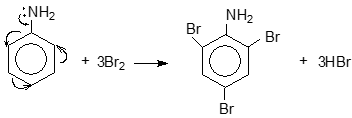
2, 4, 6 tribromanilin
Lưu ý: Phản ứng tạo ra kết tủa trắng 2, 4, 6 tribromanilin dùng nhận biết anilin
c) Phản ứng với axit nitrơ HNO2 :
- Amin bậc một tác dụng với axit nitrơ ở nhiệt độ thường cho ancol hoặc phenol và giải phóng nitơ. Ví dụ:
C2H5NH2 + HONO C2H5OH + N2 ↑ + H2O
- Anilin và các amin thơm bậc một tác dụng với axit nitrơ ở nhiệt độ thấp (0 - 5oC) cho muối điazoni :
C6H5NH2 + HONO + HCl C6H5N2+Cl- + 2H2O
phenylđiazoni clorua
d) Phản ứng cháy của amin no đơn chức mạch hở :
Ví dụ:
V. Ứng dụng và điều chế
1. Ứng dung
Các ankylamin được dùng trong tổng hợp hữu cơ, đặc biệt là các điamin được dùng để tổng hợp polime.
Anilin là nguyên liệu quan trọng trong công nghiệp phẩm nhuộm, polime (nhựa anilin - fomanđehit,…), dược phẩm …
2. Điều chế
- Thay thế nguyên tử H của phân tử amoniac
NH3 CH3NH2 (CH3)2NH (CH3)3N
- Khử hợp chất nitro
C6H5NO2 + 6H C6H5NH2 + 2H2O