Cho các nguyên tố với số hiệu nguyên tử sau: X (Z =1); Y (Z =7); E( Z =12); T (Z =19). Dãy gồm các nguyên tố kim loại là:
A. X, Y, E
B. X, Y, E, T
C. E, T
D. Y, T
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án C
Các nguyên tố kim loại thường có 1, 2, 3 e ở lớp ngoài cùng (trừ H, He, B).
Cấu hình electron nguyên tử của các nguyên tố là:
X: 1s1 => phi kim (vì là H)
Y: 1s22s22p3 => phi kim
E: 1s22s22p63s2 => kim loại
T: 1s22s22p63s23p64s1 => kim loại
Vậy các nguyên tử kim loại là E và T
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Ion M2+ có cấu hình electron ở lớp ngoài cùng là 3s23p63d6. Vị trí của M trong bảng tuần hoàn là:
Dãy kim loại nào sau đây đều tan trong dung dịch H2SO4 loãng và đặc nguội ?
Cho cấu hình electron: 1s22s22p6. Dãy nào sau đây gồm các nguyên tử và ion có cấu hình electron như trên?
Một cation kim loại M2+ có cấu hình e ở lớp ngoài cùng là 2s22p6. Vậy cấu hình e ở lớp ngoài cùng của nguyên tử kim loại M là :
Ở trạng thái cơ bản, cấu hình electron ứng với lớp ngoài cùng nào sau đây là của nguyên tố kim loại?
Hoà tan hoàn toàn 15,4 gam hỗn hợp Mg và Zn trong dung dịch HCl dư thấy có 6,72 lít khí thoát ra (ở đktc) và dung dịch X. Cô cạn dung dịch X được bao nhiêu gam muối khan?
Cho viên kẽm tác dụng với HNO3, sau phản ứng không thấy có khí sinh ra. Tổng hệ số cân bằng của phản ứng là
Cho 4,8 gam kim loại R tan hoàn toàn trong dung dịch HNO3 đặc, nóng, dư thu được 8,96 lít khí NO2 (đktc). Kim loại R là
Cho 1 lượng Cu phản ứng hết với dung dịch H2SO4đặc nóng dư, sau phản ứng thu được 2,24 lít khí SO2 (đktc) và m gam muối khan. Giá trị của m là
Hòa tan hoàn toàn 8,96 gam Fe trong dung dịch H2SO4 dư. Khối lượng muối sinh ra là
Cho 7,8 gam hỗn hợp gồm hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA tác dụng hết với dung dịch HCl (dư), thoát ra 7,84 lít khí H2 (ở đktc). Hai kim loại đó là
I. Vị trí của kim loại trong bảng tuần hoàn
Các nguyên tố hóa học được phân thành kim loại và phi kim. Trong bảng tuần hoàn nguyên tố kim loại có mặt ở:
- Nhóm IA (trừ hiđro), nhóm IIA: các kim loại này là những nguyên tố s.
- Nhóm IIIA (trừ B), một phần của các nhóm IVA, VA, VIA: các kim loại này là những nguyên tố p.
- Các nhóm B (từ IB đến VIIIB): các kim loại chuyển tiếp, chúng là những nguyên tố d.
- Họ lantan và actini (xếp riêng thành hai hàng ở cuối bảng): các kim loại thuộc hai họ này là những nguyên tố f.
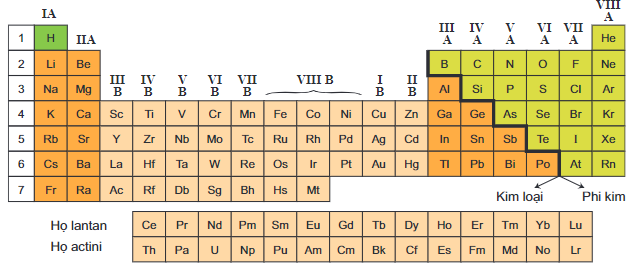
Vị trí của các nguyên tố kim loại trong bảng tuần hoàn
II. Cấu tạo của kim loại
1. Cấu tạo nguyên tử
- Nguyên tử của hầu hết các nguyên tố kim loại có 1, 2 hoặc 3 electron ở lớp ngoài cùng.
Ví dụ:
+ Na: [Ne]3s1 có 1electron ở lớp ngoài cùng.
+ Mg: [Ne]3s2 có 2 electron ở lớp ngoài cùng.
+ Al: [Ne]3s23p1 có 3 electron ở lớp ngoài cùng.
- Trong chu kì, nguyên tử của nguyên tố kim loại có bán kính nguyên tử lớn hơn và điện tích hạt nhân nhỏ hơn so với các nguyên tử của nguyên tố phi kim.
Ví dụ xét với chu kì 3:
|
Nguyên tử |
11Na |
12Mg |
13Al |
14Si |
15P |
16S |
17Cl |
|
rnt |
0,157 |
0,136 |
0,125 |
0,117 |
0,110 |
0,104 |
0,099 |
2. Cấu tạo tinh thể
- Ở nhiệt độ thường, trừ thủy ngân ở thể lỏng, còn các kim loại khác ở thể rắn, có cấu tạo tinh thể.
- Trong tinh thể kim loại, nguyên tử và ion kim loại nằm ở những nút mạng của tinh thể. Các electron hóa trị liên kết yếu với hạt nhân nên dễ tách ra khỏi nguyên tử và chuyển động tự do trong mạng tinh thể.
- Có ba kiểu mạng tinh thể kim loại đặc trưng là: lập phương tâm khối, lập phương tâm diện và lục phương.
a) Mạng tinh thể lục phương
- Đặc điểm: Các nguyên tử, ion kim loại nằm trên các đỉnh và tâm các mặt của hình lục giác đứng và ba nguyên tử, ion nằm phía trong của hình lục giác.
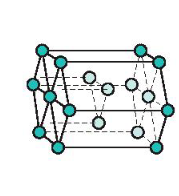
Mạng tinh thể lục phương
- Trong tinh thể, thể tích của các nguyên tử và ion kim loại chiểm 74%, còn lại 26% là không gian trống.
- Thuộc loại này có các kim loại: Be, Mg, Zn …
b) Mạng tinh thể lập phương tâm diện
- Đặc điểm: Các nguyên tử và ion kim loại nằm trên các đỉnh và tâm các mặt của hình lập phương.
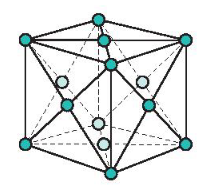
Mạng tinh thể lập phương tâm diện
- Trong tinh thể, thể tích của các nguyên tử và ion kim loại chiểm 74%, còn lại 26% là không gian trống.
- Thuộc loại này có các kim loại: Cu, Ag, Au, Al …
c) Mạng tinh thể lập phương tâm khối
- Đặc điểm: Các nguyên tử và ion kim loại nằm trên các đỉnh và tâm của hình lập phương.
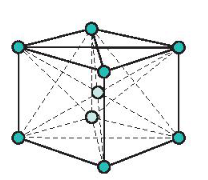
Mạng tinh thể lập phương tâm khối
- Trong tinh thể, thể tích của các nguyên tử và ion kim loại chỉ chiếm 68%, còn lại 32% là các không gian trống.
- Thuộc loại này có các kim loại: Li, Na, K, V, Mo …
3. Liên kết kim loại
Liên kết kim loại là liên kết được hình thành giữa nguyên tử và ion kim loại trong mạng tinh thể do sự tham gia của các electron tự do.