Trong ăn mòn điện hóa, xảy ra
A. sự oxi hóa ở cực dương
B. sự oxi hóa ở cực dương và sự khử ở cực âm
C. sự khử ở cực âm
D. sự oxi hóa ở cực âm và sự khử ở cực dương
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án D
Quá trình ăn mòn điện hóa là quá trình oxi hóa – khử, trong đó kim loại ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương → sự oxi hóa ở cực âm và sự khử ở cực dương
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Kim loại nào sau đây có khả năng tạo ra màng oxit bảo vệ để không bị oxi hóa ngoài không khí ẩm ?
Để bảo vệ các phương tiện giao thông hoạt động dưới nước có vỏ bằng thép người ta gắn vào vỏ đó (ở phần ngập dưới nước) kim loại
Cho viên bi sắt vào ống nghiệm đựng dung dịch HCl, theo thời gian sắt sẽ bị ăn mòn
Để chống ăn mòn cho đường ống dẫn dầu bằng thép chôn dưới đất, người ta dùng phương pháp điện hoá. Trong thực tế, người ta dùng kim loại nào sau đây làm điện cực hi sinh?
Ngâm đinh sắt vào 1 trong 4 dung dịch sau: NaCl, FeCl3, H2SO4, Cu(NO3)2. Hỏi trường hợp nào sẽ xảy ra ăn mòn điện hóa?
Hỗn hợp tecmit dùng để hàn những chỗ vỡ, mẻ của đường tàu hỏa là
Để bảo vệ những vật bằng Fe khỏi bị ăn mòn, người ta phủ một lớp sơn lên vật liệu. Làm như vậy là để chống ăn mòn theo phương pháp nào sau đây?
Cho thanh sắt vào dung dịch H2SO4 loãng sau đó thêm tiếp vài giọt dung dịch CuSO4. Hiện tượng quan sát được là
I. Khái niệm
- Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim dưới tác dụng của môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương:
M → Mn+ + ne
II. Các dạng ăn mòn kim loại
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học.
1. Ăn mòn hóa học
a. Nguyên nhân: do kim loại có phản ứng hóa học trực tiếp với các chất ở môi trường xung quanh.
Ví dụ: Ngâm dinh sắt trong dung dịch H2SO4 loãng
Fe + H2SO4 (loãng) → FeSO4 + H2

Sắt tác dụng với H2SO4 loãng
b. Điều kiện: kim loại được đặt trong môi trường có chứa chất oxi hóa mà kim loại có thể tham gia phản ứng thường là chất khí, hơi nước, dung dịch axit...
c. Bản chất: là quá trình oxi hóa - khử trong đó kim loại đóng vai trò chất khử. Electron chuyển trực tiếp từ kim loại vào môi trường.
2. Ăn mòn điện hóa học
a. Khái niệm
- Ăn mòn điện hóa học là quá trình oxi hóa -khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương.
- Ví dụ: Nhúng thanh Zn và thanh Cu (không tiếp xúc trực tiếp với nhau) vào cốc đựng dung dịch H2SO4 loãng. Nối thanh kẽm với thanh đồng bằng dây dẫn cho đi qua một điện kế, như hình minh họa sau:
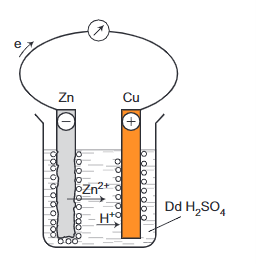
- Hiện tượng:
+ Khi chưa nối dây dẫn, lá Zn bị hòa tan và bọt khí H2 thoát ra ở bề mặt lá Zn.
+ Khí nối dây dẫn, lá Zn bị ăn mòn nhanh trong dung dịch điện li, kim điện kế lệch, bọt khí H2 thoát ra cả ở lá Cu.
- Giải thích:
+ Khi chưa nối dây dẫn, kẽm bị ăn mòn hóa học do phản ứng oxi hóa kẽm bởi ion H+ trong dung dịch axit:
Zn + 2H+ → Zn2+ + H2
Bọt khí sinh ra trên bề mặt lá Zn.
+ Khi nối các thanh Cu và Zn bằng một dây dẫn, một pin điện đã được hình thành, trong đó Zn là cực âm, Cu là cực dương.
Tại cực âm (anot), kẽm bị ăn mòn theo phản ứng:
Zn → Zn2+ + 2e
Tại cực dương (catot), ion H+ của dung dịch H2SO4 nhận electron biến thành H rồi thành phân tử H2 thoát ra:
2H+ + 2e → H2
+ Các electron di chuyển từ lá Zn sang lá Cu qua dây dẫn tạo ra dòng điện một chiều. Dòng điện này làm cho kim điện kế bị lệch.
b. Điều kiện xảy ra sự ăn mòn điện hóa học:
+ Các điện cực phải khác nhau về bản chất, có thể là 2 cặp kim loại khác nhau hoặc cặp kim loại với phi kim….
+ Các điện cực phải tiếp xúc trực tiếp hoặc gián tiếp với nhau qua dây dẫn.
+ Các điện cực phải cùng tiếp xúc với một dung dịch chất điện li.
⇒ Thiếu một trong 3 điều kiện trên sẽ không xảy ra ăn mòn điện hóa học.
Trong tự nhiên, sự ăn mòn kim loại xảy ra phức tạp, có thể xảy ra đồng thời cả ăn mòn hóa học và ăn mòn điện hóa học.
III. Chống ăn mòn kim loại
Sự ăn mòn kim loại gây tổn thất to lớn cho nền kinh tế quốc dân. Để bảo vệ kim loại khỏi sự ăn mòn có thể sử dụng các phương pháp sau:
1. Phương pháp bảo vệ bề mặt
Dùng những chất bền vững với môi trường để phủ ngoài mặt những đồ vật bằng kim loại như bôi dầu, mỡ, sơn, mạ, tráng men…

Sơn chống gỉ
2. Phương pháp điện hóa
- Nối kim loại cần bảo vệ với một kim loại hoạt động hơn để tạo thành pin điện hóa và kim loại hoạt động hơn bị ăn mòn, kim loại kia được bảo vệ.
- Ví dụ để bảo vệ vỏ tàu biển bằng thép, người ta gắn các lá Zn vào phía ngoài vỏ tàu ở phần chìm trong nước biển (nước biển là dung dịch chất điện li). Phần vỏ tàu bằng thép là cực dương, các lá Zn là cực âm.
+ Ở anot (cực âm): Zn bị oxi hóa Zn → Zn2+ + 2e
+ Ở catot (cực dương): O2 bị khử 2H2O + O2 + 4e → 4OH-
- Kết quả vỏ tàu bị bảo vệ, Zn là vật hi sinh, nó bị ăn mòn. Nhưng tốc độ ăn mòn điện hóa của Zn trong điều kiện này tương đối nhỏ và vỏ tàu được bảo vệ trong thời gian dài. Sau một thời gian người ta thay những lá Zn bị ăn mòn thành những lá Zn khác.