Hòa tan hoàn toàn 8,94 gam hỗn hợp gồm Na, K và Ba vào nước thu được dung dịch X và 2,688 lit khí (đktc) . Dung dịch Y gồm HCl và có tỉ lệ mol tương ứng là 4 : 1. Trung hòa dung dịch X bởi dung dịch Y , tổng khối lượng các muối được tạo ra là
A. 13,7
B. 12,78
C. 18,46
D. 14,62
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án C
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Cho các chất sau : .
Số chất bị nhiệt phân có chất khí trong sản phẩm tạo thành là
Hòa tan hỗn hợp (trong đó số mol và bằng nhau) vào nước lọc thu được dung dịch X và m gam kết tủa Y . Biết X tác dụng vừa đủ 0,16 mol NaOH hoặc 0,24 mol HCl thì hết khí bay ra . Giá trị của m là:
Cho 2,22 gam hỗn hợp kim loại gồm K, Na và Ba vào nước được 500ml dung dịch X có pH = 13. Cô cạn dung dịch X được m gam chất rắn. Giá trị của m là:
Tính khử của các nguyên tử Na, K, Al, Mg được xếp theo thứ tự tăng dần là:
Nhỏ từ từ dung dịch chứa a mol và a mol vào dung dịch HCl thu được V lít khí (đktc). Khi cho dung dịch dư vào dung dịch sau phản ứng thu được m gam kết tủa. Quan hệ giữa a với m, V là
Một loại nước cứng tạm thời chứa ion . Cô cạn 100 ml dung dịch nước cứng này thu được 156,8 ml (đktc). Để loại bỏ tính cứng tạm thời của 1 lít nước cứng này cần dùng tối thiếu số ml dung dịch NaOH 0,1M là
Để bảo quản các kim loại kiềm, có thể thực hiện cách nào sau đây ?
Hấp thụ hoàn toàn 1,568 lít (đktc) vào 500ml dung dịch NaOH 0,16M thu được dung dịch X. Thêm 250 ml dung dịch Y gồm 0,16M và a mol/l vào dung dịch X thu được 3,94 gam kết tủa và dung dịch Z. Giá trị của a là :
Các tính chất vật lí (nhiệt độ sôi, nhiệt độ nóng chảy, khối lượng riêng) của các kim loại trong nhóm IA biến đổi có quy luật, trong đó các kim loại nhóm IIA biến đổi không theo quy luật. Để giải thích hiện tượng này có thể dựa vào
Cho x mol hỗn hợp 2 kim loại kiềm thuộc 2 chu kì liên tiếp tác dụng vừa đủ với dung dịch HCl thì thu được a gam muối khan. Nếu cũng cho x mol hỗn hợp trên tác dụng vừa đủ với dung dịch thì thu được b gam muối khan. Giá trị của x là
Chỉ dùng duy nhất một hóa chất nào dưới đây có thể phân biệt được 4 lọ mất nhãn chứa các dung dịch : và NaCl.
Cho 7,1 gam hỗn hợp gồm một kim loại kiềm X và một kim loại kiềm thổ Y tác dụng với lượng dư dung dịch HCl loãng thu được 5,6 lít khí. Hai kim loại X, Y có thể là
Cho các cặp dung dịch phản ứng với nhau:
Các cặp phản ứng có cả kết tủa và khí bay ra là
Hoà tan 46 gam một hỗn hợp Ba và hai kim loại kiềm A, B thuộc hai chu kì kế tiếp nhau vào nước thu được dung dịch C và 11,2 lít khí (đktc). Nếu thêm 0,18 mol vào dung dịch C thì dung dịch sau phản ứng vẫn chưa kết tủa hết Ba. Nếu thêm 0,21 mol vào dung dịch C thì dung dịch sau phản ứng còn dư . A và B là
A. Kim loại kiềm
I. Ví trí trong bảng tuần hoàn và cấu hình electron nguyên tử
- Kim loại kiềm thuộc nhóm IA của bảng tuần hoàn, gồm các nguyên tố: Liti (Li); natri (Na); kali (K); rubiđi (Rb); xesi (Cs) và franxi (Fr).
Trong đó Fr là nguyên tố phóng xạ.
- Cấu hình electron nguyên tử:
Li: [He]2s1; Na: [Ne]3s1;
K: [Ar]4s1; Rb: [Kr]5s1;
Cs: [Xe]6s1
⇒ Nguyên tử kim loại kiềm có 1e ở lớp ngoài cùng.
II. Tính chất vật lí
- Các kim loại kiềm có màu trắng bạc và có ánh kim, dẫn điện tốt, nhiệt độ nóng chảy, nhiệt độ sôi thấp, khối lượng riêng nhỏ và độ cứng thấp.

Kim loại Na
- Kim loại kiềm nhiệt độ nóng chảy, nhiệt độ sôi thấp, khối lượng riêng nhỏ và độ cứng thấp do:
+ Kim loại kiềm có cấu tạo tinh thể lập phương tâm khối, cấu trúc tương đối rỗng.
+ Trong tinh thể, các nguyên tử và ion liên kết với nhau bằng liên kết kim loại yếu.
III. Tính chất hóa học
- Các kim loại kiềm có tính rất khử mạnh: M → M+ + 1e. Tính khử tăng dần từ Li đến Cs.
- Trong hợp chất, các kim loại kiềm có số oxi hóa +1.
1. Tác dụng với phi kim
Kim loại kiềm khử dễ dàng các nguyên tử phi kim thành ion âm.
Ví dụ:
+ Na tác dụng với oxi khô tạo peoxit:
2Na + O2 → Na2O2 (natri peoxit)
+ Na tác dụng với oxi không khí khô ở nhiệt độ phòng tạo Na2O.
4Na + O2 → 2Na2O (natri oxit)
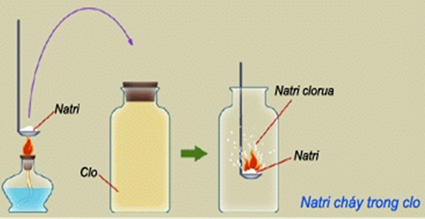
+ Na nóng chảy tác dụng với Cl2 tạo thành natri clorua:
2Na + Cl2 → 2NaCl
2. Tác dụng với axit
- Kim loại kiềm khử mạnh ion H+ trong dung dịch axit HCl và H2SO4 loãng thành khí H2:
2M + 2H+ → 2M+ + H2 ↑ (với M là kim loại kiềm)
- Phản ứng xảy ra mãnh liệt, tất cả các kim loại kiềm đều nổ khi tiếp xúc với axit.
3. Tác dụng với nước
- Kim loại kiềm khử nước dễ dàng ở nhiệt độ thường, giải phóng khí H2:
2M + 2H2O → 2MOH (dd) + H2 ↑ (với M là kim loại kiềm)
- Từ Li đến Cs phản ứng với nước xảy ra càng mãnh liệt. Do đó để bảo quản kim loại kiềm, người ta ngâm chìm các kim loại kiềm trong dầu hỏa.
IV. Ứng dụng, trạng thái tự nhiên và điều chế
1. Ứng dụng
Kim loại kiềm có nhiều ứng dụng quan trọng:
- Dùng chế tạo hợp kim có nhiệt độ nóng chảy thấp.
- Cs dùng chế tạo tế bào quang điện.
- Hợp kim liti – nhôm siêu nhẹ được dùng trong kĩ thuật hàng không.
2. Trạng thái tự nhiên
Trong tự nhiên kim loại kiềm không có ở dạng đơn chất mà chỉ tồn tại ở dạng hợp chất.
3. Điều chế
- Phương pháp: Điện phân nóng chảy muối halogenua hoặc hiđroxit của kim loại kiềm trong điều kiện không có không khí.
- Ví dụ:
2NaCl 2Na + Cl2
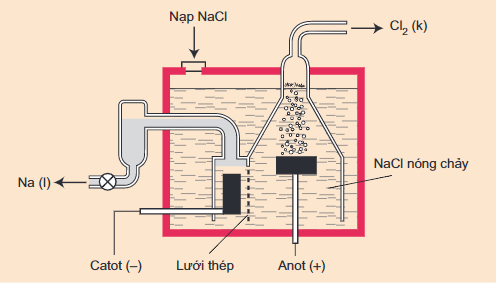
Sơ đồ thùng điện phân NaCl nóng chảy
B. Một số hợp chất quan trọng của kim loại kiềm
I. Natri hiđroxit, NaOH
1. Tính chất vật lí
+ NaOH là chất rắn, không màu, dễ nóng chảy, hút ẩm mạnh (dễ chảy rữa).

NaOH rắn
+ NaOH tan nhiều trong nước và tỏa ra một lượng nhiệt lớn nên cần tuyệt đối cẩn thận khi hòa tan NaOH trong nước.
2. Tính chất hóa học
- Khi tan trong nước, NaOH phân li hoàn toàn thành ion:
NaOH → Na+ + OH-
- NaOH là bazơ mạnh, mang đầy đủ tính chất của một bazơ tan:
+ Dung dịch NaOH làm quỳ tím chuyển sang màu xanh, phenolphtalein chuyển sang màu hồng.
+ Tác dụng với axit, oxit axit tạo thành muối và nước:
NaOH + HCl → NaCl + H2O
Chú ý: Khi tác dụng với axit và oxit axit trung bình, yếu thì tùy theo tỉ lệ mol các chất tham gia mà muối thu được có thể là muối axit, muối trung hòa hay cả hai loại muối.
2NaOH + CO2 → Na2CO3 + H2O
NaOH + CO2 → NaHCO3
+ Tác dụng với dung dịch muối tạo thành muối mới và bazơ mới:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
3. Ứng dụng
NaOH là hóa chất quan trọng, đứng hàng thứ hai sau H2SO4.
NaOH được dùng để nấu xà phòng, chế phẩm nhuộm, tơ nhân tạo, tinh chế quặng nhôm trong công nghiệp luyện nhôm và dùng trong công nghiệp chế biến dầu mỏ.
II. Natri hiđrocacbonat
1. Tính chất
- NaHCO3 là chất rắn, màu trắng, dễ tan trong nước.

NaHCO3
- NaHCO3 dễ bị nhiệt phân hủy tạo thành Na2CO3 và khí CO2:
2NaHCO3 Na2CO3 + CO2 + H2O
- NaHCO3 có tính lưỡng tính (vừa tác dụng với dung dịch axit, vừa tác dụng với dung dịch bazơ)
NaHCO3 + HCl → NaCl + CO2 ↑ + H2O
NaHCO3 + NaOH → Na2CO3 + H2O
2. Ứng dụng
NaHCO3 được dùng trong công nghiệp dược phẩm (chế tạo thuốc đau dạ dày …) và công nghiệp thực phẩm (làm bột nở …).
III. Natri cacbonat
1. Tính chất
- Natri cacbonat (hay soda) là chất rắn màu trắng, dễ tan trong nước.
- Na2CO3 là muối của axit yếu và có những tính chất hóa học chung của muối.
- Muối cacbonat của kim loại kiềm trong nước cho môi trường kiềm.
2. Ứng dụng
Na2CO3 là hóa chất quan trọng cho công nghiệp thủy tinh, bột giặt, phẩm nhuộm, giấy, sợi …
IV. Kali nitrat
1. Tính chất
- KNO3 là tinh thể, không màu, bền trong không khí, tan nhiều trong nước.

KNO3
- Khi đun nóng ở nhiệt độ trên 333oC, KNO3 bắt đầu bị phân hủy tạo thành KNO2 và O2
2KNO3 2KNO2 + O2
2. Ứng dụng
+ KNO3 được sử dụng làm phân bón (phân đạm, phân kali) và được dùng để chế tạo thuốc nổ. Thuốc nổ thông thường (thuốc súng) là hỗn hợp gồm 68% KNO3, 15% S và 17% C (than).
+ Phản ứng của thuốc súng xảy ra theo phương trình:
2KNO3 + 3C + S N2 ↑ + 3CO2 ↑+ K2S