Từ xa xưa con người đã biết lên men các loại ngũ cốc, hoa quả để tạo ra các đồ uống có cồn (có chứa ethanol – một alcohol quen thuộc). Ngày nay, alcohol được sử dụng phổ biến trong nhiều lĩnh vực khác nhau như làm dung môi, nguyên liệu hoá học, nhiên liệu, xăng sinh học, … Vậy alcohol là gì và có những tính chất đặc trưng nào?
 Giải bởi Vietjack
Giải bởi Vietjack
- Alcohol là những hợp chất hữu cơ trong phân tử có chứa nhóm hydroxy (-OH) liên kết với nguyên tử carbon no.
- Tính chất đặc trưng của alcohol:
+ Phản ứng với các kim loại mạnh như sodium, potassium … giải phóng khí hydrogen.
+ Phản ứng tạo ether khi đun nóng alcohol với H2SO4 đặc ở khoảng 140 oC.
+ Alcohol no, đơn chức, mạch hở bị tách nước tạo thành alkene.
+ Khi phản ứng với các tác nhân oxi hoá, ví dụ: CuO: alcohol bậc I bị oxi hoá thành aldehyde, alcohol bậc II bị oxi hoá thành ketone, alcohol bậc III không bị oxi hoá trong điều kiện này.
+ Các alcohol đều cháy, khi cháy toả nhiều nhiệt.
+ Ngoài ra, các polyalcohol có các nhóm -OH liền kề, có thể tác dụng với copper(II) hydroxide tạo thành dung dịch màu xanh lam đậm.
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Một đơn vị cồn tương đương 10 mL (hoặc 7,89 gam) ethanol nguyên chất. Theo khuyến cáo của ngành y tế, để đảm bảo sức khoẻ mỗi người trưởng thành không nên uống quá 2 đơn vị cồn mỗi ngày. Vậy mỗi người trưởng thành không nên uống quá bao nhiêu mL rượu 40o một ngày?
Viết công thức cấu tạo của các alcohol có tên gọi dưới đây:
a) pentan – 1 – ol;
b) but – 3 – en – 1 – ol;
c) 2 – methylpropan – 2 – ol;
d) butane – 2,3 – diol.
Viết phương trình hoá học của các phản ứng trong sơ đồ điều chế glycerol từ propylene.
Các hợp chất propane, dimethyl ether và ethanol có phân tử khối tương đương nhau và có một số tính chất như sau:
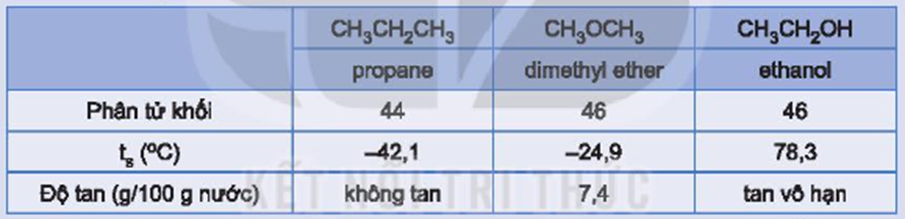
Hãy giải thích tại sao ethanol có nhiệt độ sôi cao hơn và tan trong nước tốt hơn so với hai chất còn lại.
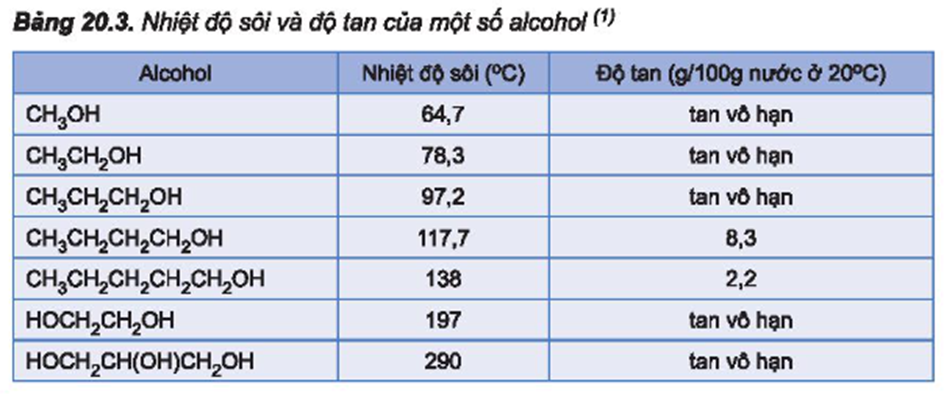
Từ số liệu ở Bảng 20.3, em hãy giải thích tại sao trong dãy alcohol no, đơn chức, mạch hở, nhiệt độ sôi của các alcohol tăng dần từ C1 đến C5 còn độ tan trong nước giảm dần từ C3 đến C5.
Đun nóng butan – 2 – ol với sulfuric acid đặc thu được các alkene nào? Sản phẩm nào là sản phẩm chính.
Viết các đồng phân cấu tạo của alcohol có công thức C4H9OH và xác định bậc của các alcohol đó.
Chuẩn bị: dung dịch CuSO4 2%, dung dịch NaOH 10%, ethanol, glycerol; 2 ống nghiệm.
Tiến hành:
- Cho vào 2 ống nghiệm, mỗi ống khoảng 1 mL dung dịch CuSO4 2% và 1 mL dung dịch NaOH 10%.
- Lắc nhẹ 2 ống nghiệm rồi nhỏ vào từng ống:
Ống nghiệm (1): 5 giọt ethanol.
Ống nghiệm (2): 5 giọt glycerol.
- Lắc đều cả 2 ống nghiệm.
Quan sát hiện tượng xảy ra ở từng ống nghiệm, giải thích và viết phương trình hoá học.
Chuẩn bị: cồn 90o (cồn y tế), bát sứ, que đóm dài khoảng 20 cm.
Tiến hành: Lấy khoảng 1 mL ethanol (chú ý không lấy nhiều hơn) cho vào bát sứ. Đốt cháy que đóm và đưa ngọn lửa vào gần miệng bát sứ để đốt cháy ethanol.
Lưu ý: Cẩn thận bỏng khi thực hiện thí nghiệm đốt cháy cồn.
Quan sát hiện tượng và viết phương trình hoá học của phản ứng xảy ra.
Viết công thức cấu tạo sản phẩm của phản ứng khi oxi hoá các alcohol sau bằng CuO đun nóng:

Viết phương trình hoá học của phản ứng giữa methanol với sodium.