Chỉ dùng quỳ tím, có thể nhận biết ba dung dịch riêng biệt nào sau đây?
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án A
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Hãy cho biết dãy các dung dịch nào sau đây có khả năng đổi màu quỳ tím sang đỏ (hồng) ?
Cho 10 ml dung dịch X chứa HCl 1M và 0,5M. Thể tích dung dịch NaOH 1M cần để trung hòa dung dịch X là
Cho các dung dịch muối: , , , , , , , .
Những dung dịch muối làm quỳ hoá xanh là :
Cho các dung dịch , và có cùng giá trị pH. Sự sắp xếp nào sau đây đúng với giá trị nồng độ mol của các dung dịch trên ?
Trộn lẫn 3 dung dịch: , và với những thể tích bằng nhau thu được dung dịch A. Lấy 300ml dung dịch A tác dụng với V ml dung dịch và thu được dung dịch có pH = 2. Giá trị của V là
Trộn lít dung dịch NaOH có pH = 13 với lít dung dịch có pH = 11, thu được dung dịch mới có pH = 12. Tỉ số có giá trị là
Khi hòa tan trong nước, chất nào sau đây làm cho quỳ tím chuyển màu xanh ?
Trộn lít dung dịchcó pH = 3 với lít dung dịch NaOH có pH = 12, thu được dung dịch mới có pH = 4. Tỉ số có giá trị là
Dung dịch A có chứa 5 ion: và 0,1 mol Cl- và 0,2 mol . Thêm dần V ml dung dịch 1M vào dung dịch A đến khi thu được lượng kết tủa lớn nhất. V có giá trị là
Trộn hai dung dịch và có cùng nồng độ mol với nhau theo tỉ lệ thể tích 1 : 1 thu được kết tủa và dung dịch. Bỏ qua sự thủy phân của các ion và sự điện li của nước, các ion có mặt trong dung dịch Y là
Trộn 200 ml dung dịch gồm HCl 0,1M và 0,15M với 300 ml dung dịch nồng độ aM, thu được m gam kết tủa và 500 ml dung dịch có pH = 1. Giá trị của a và m lần lượt là
I. Nước là chất điện li rất yếu
1. Sự điện li của nước
- Nước là chất điện li rất yếu. Thực nghiệm đã xác định được ở nhiệt độ thường cứ 555 triệu phân tử nước chỉ có 1 phân tử phân li ra ion.
- Phương trình điện li:
2. Tích số ion của nước
- Ở 25C, tích số = [H+].[OH-] được gọi là tích số ion của nước. Tích số này là hằng số ở nhiệt độ xác định. Tuy nhiên, giá trị tích số ion của nước thường được dùng trong các phép tính, khi nhiệt độ không khác nhiều so với 25C.
= [H+].[OH-] = 10^-14
⇒ [H+] = [OH-] = 10^-7 M.
- Môi trường trung tính là môi trường trong đó [H+] = [OH-] = 10^-7 M.
3. Ý nghĩa tích số ion của nước
a. Môi trường axit
- Là môi trường trong đó [H+] > [OH-] hay [H+] > 10^-7 M.
b. Môi trường kiềm
- Là môi trường trong đó [H+] < [OH-] hay [H+] < 10^-7 M.
Kết luận: Độ axit và độ kiềm của dung dịch có thể đánh giá bằng nồng độ H+.
+ Môi trường trung tính: [H+] = 10^-7 M.
+ Môi trường axit: [H+] > 10^-7 M.
+ Môi trường kiềm: [H+] < 10^-7 M.
II. Khái niệm về pH. Chất chỉ thị axit – bazơ
1. Khái niệm về pH
- pH được dùng để đánh giá độ axit và độ kiềm của dung dịch.
- Quy ước:
Tức là: thì pH = a.
Về mặt toán học:
- Thang pH thường dùng có giá trị từ 1 đến 14, trong đó:
+ pH < 7: môi trường axit.
+ pH > 7: môi trường bazơ.
+ pH = 7: môi trường trung tính.
- Giá trị của pH có ý nghĩa to lớn trong thực tế. Chẳng hạn, pH của máu người và động vật có giá trị gần như không đổi hay tốc độ ăn mòn kim mòn kim loại trong nước tự nhiên phụ thuộc rất nhiều vào giá trị pH của nước.
2. Chất chỉ thị axit – bazơ
- Là chất có màu biến đổi phụ thuộc vào giá trị pH của dung dịch.
Ví dụ: Quỳ tím, phenolphatalenin.
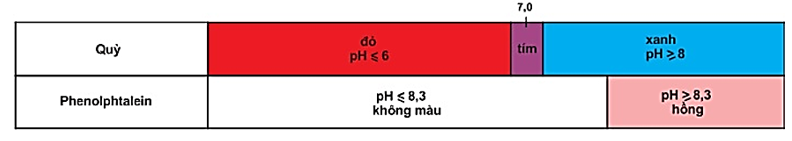
Hình 1: Màu của quỳ và phenolphtalein trong dung dịch ở các khoảng pH khác nhau
- Trộn lẫn một số chất chỉ thị có màu biến đổi kế tiếp nhau theo giá trị pH, ta được hỗn hợp chất chỉ thị vạn năng.
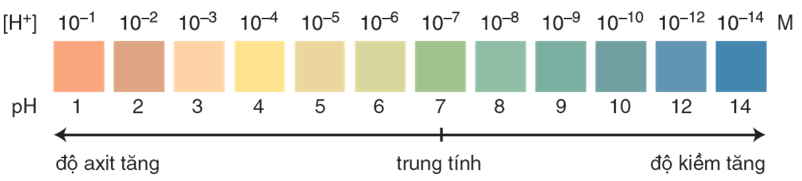
Hình 2: Màu của chất chỉ thị vạn năng (thuốc thử MERCK của Đức) ở các giá trị pH khác nhau
- Để xác định tương đối chính xác giá trị pH của dung dịch, người ta dùng máy đo pH.
3. Bảng công thức pH trong các môi trường
