Một bình kín chứa 4 mol khí N2 và 10 mol khí H2 có áp suất là 200atm. Khi đạt trạng thái cân bằng thì áp suất trong bình là 180 atm, nhiệt độ trong bình được giữ không đổi. Tính hiệu suất của phản ứng tổng hợp NH3 trên.
A. 21%
B. 17,5%
C. 50%
D. 35%
 Giải bởi Vietjack
Giải bởi Vietjack
P1V= n1RT (n1=14)
N2 + 3 H2 <-> 2NH3
có 4 10
p/u x 3x 2x
sau 4-x 10-3x 2x
4-x + 10-3x + 2x = 12,6
=> 14-2x=12,6
=> x=0,7
=> Tính theo H2 => H= 21%
Đáp án cần chọn là: A
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Cho phương trình hoá học của phản ứng tổng hợp amoniac:
N2 (k) + 3H2 (k) 2NH3 (k)
Khi tăng nồng độ của hiđro lên 2 lần, tốc độ phản ứng thuận
Hỗn hợp X gồm N2 và H2 có tỉ khối hơi so với H2 là 3,6. Cho hỗn hợp X vào bình kín với xúc tác thích hợp rồi thực hiện phản ứng tổng hợp NH3 thấy thu được hỗn hợp Y gồm N2, H2 và NH3. Biết tỉ khối hơi của Y so với H2 bằng 4. Hiệu suất phản ứng tổng hợp NH3 trong phản ứng trên là
Cho muối X vào dung dịch NaOH đun nhẹ thấy có khí mùi khai bay ra. Mặt khác, cho muối X vào dung dịch H2SO4 loãng sau đó cho Cu vào thấy Cu tan ra và có khí không màu bay lên và hóa nâu ngoài không khí. X có thể là
Các chất khí điều chế trong phòng thí nghiệm thường được thu theo phương pháp đẩy không khí (cách 1, cách 2) hoặc đẩy nước (cách 3) như hình vẽ sau đây:
Có thể dùng cách nào trong 3 cách trên để thu khí NH3?
Cho 4 mol N2 và 16 mol H2 vào bình kín. Tại thời điểm cân bằng thu được x mol hỗn hợp khí. Biết hiệu suất của phản ứng tổng hợp NH3 là 70%. Tính x?
Cho phản ứng: N2 (k) + 3H2 (k) ⇄ 2NH3 (k). Nếu ở trạng thái cân bằng nồng độ NH3 là 0,30 mol/l, N2 là 0,05 mol/l và của H2 là 0,10 mol/l thì hằng số cân bằn của phản ứng là
Cho 100 gam dung dịch NH4HSO4 11,5% phản ứng với 100 gam dung dịch Ba(OH)2 13,68%. Thể tích khí (đktc) và khối lượng kết tủa tạo ra lần lượt là:
Cho hỗn hợp gồm N2, H2 và NH3 có tỉ khối so với hiđro là 8. Dẫn hỗn hợp đi qua H2SO4 đặc, dư thì thể tích khí còn lại một nửa. Thành phần phần trăm (%) theo thể tích của mỗi khí trong hỗn hợp lần lượt là:
Cho phản ứng tổng hợp sau
Yếu tố không giúp tăng hiệu suất phản ứng là
Nung nóng bình kín chứa a mol hỗn hợp NH3 và O2 (có xúc tác Pt) để chuyển toàn bộ NH3 thành NO. Làm nguội và thêm nước vào bình, lắc đều thu được 1 lít dung dịch HNO3 có pH = 1, còn lại 0,25a mol khí O2. Biết các phản ứng xảy ra hoàn toàn. Giá trị của a là
Cho NH3 dư vào 100ml dung dịch gồm CuSO4 1M ; ZnCl2 0,5M, AgNO3 1M và AlCl3 1M. Khối lượng kết tủa sau phản ứng là
A. AMONIAC
I. Cấu tạo phân tử
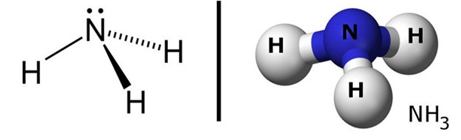
Hình 1: Sơ đồ cấu tạo và mô hình cấu tạo của phân tử N.
- Trong phân tử N, N liên kết với ba nguyên tử hiđro bằng ba liên kết cộng hóa trị có cực.
- Những đôi electron dùng chung bị lệch về phía nguyên tử N có độ âm điện lớn hơn.
- Phân tử N có cấu tạo hình chóp với nguyên tử nitơ ở đỉnh, đáy là một tam giác mà đỉnh là ba nguyên tử H.
- Nitơ còn một cặp electron hóa trị là nguyên nhân gây ra tính bazơ của N.
II. Tính chất vật lý
- Amoniac (N) là chất khí không màu, có mùi khai và xốc, nhẹ hơn không khí, tan rất nhiều trong nước.
- Ở điều kiện thường, 1 lít nước có hòa tan 800 lít amoniac.
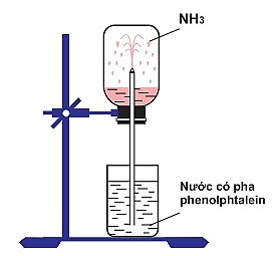
Hình 2: Sự hòa tan của amoniac trong nước
- Hòa tan N vào nước thu được dung dịch gọi là dung dịch amoniac. Dung dịch amoniac đậm đặc thường dùng trong phòng thí nghiệm có nồng độ 25% (D = 0,91g/cm3).
III. Tính chất hóa học
1. Tính bazơ yếu
a) Tác dụng với nước
N + O ⇄
⇒ Dung dịch N là một dung dịch bazơ yếu.
⇒ Có thể dùng quỳ tím ẩm để nhận biết khí amoniac, quỳ tím ẩm sẽ chuyển thành màu xanh.
b) Tác dụng với dung dịch muối
- Dung dịch amoniac có thể tác dụng với dung dịch muối của nhiều kim loại, tạo thành kết tủa hiđroxit của các kim loại đó.
AlC + 3N + 3O → Al(OH)3↓ + 3NCl
A+ + 3N + 3O → Al(OH)3↓ + 3
c) Tác dụng với axit → muối amoni:
N + HCl → NCl (amoni clorua)
2N + S → (N)2S (amoni sunfat)
2. Tính khử
- Amoniac có tính khử: phản ứng được với oxi, clo và khử một số oxit kim loại.
a) Tác dụng với oxi
N cháy trong khí oxi cho ngọn lửa màu vàng, tạo ra khí nitơ và hơi nước.
4N + 3 2 + 6O
4N + 5 4NO + 6O
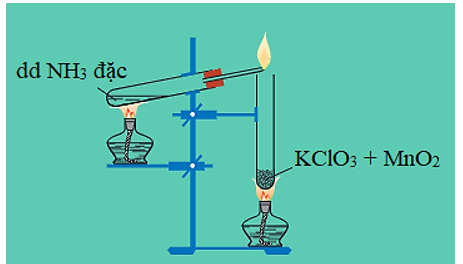
Hình 3: Khí amoniac cháy trong oxi
b) Tác dụng với clo
- Clo oxi hóa mạnh amoniac tạo ra nitơ và hiđro clorua:
2N + 3C → + 6HCl
- N kết hợp ngay với HCl vừa sinh ra tạo “khói trắng” NCl.
N + HCl → NCl
IV. Ứng dụng
- Sản xuất axit nitric, các loại phân đạm như urê (N)2CO; NN; (N)2S; …

Hình 4: Một số loại đạm
- Điều chế hiđrazin () làm nhiên liệu cho tên lửa.
- Amoni lỏng dùng làm chất gây lạnh trong thiết bị lạnh.
V. Điều chế
1. Trong phòng thí nghiệm
- Điều chế bằng cách đun nóng muối amoni (ví dụ NCl) với Ca(OH)2.
Phương trình hóa học:
2NCl + Ca(OH)2 CaC + 2N↑ + 2O
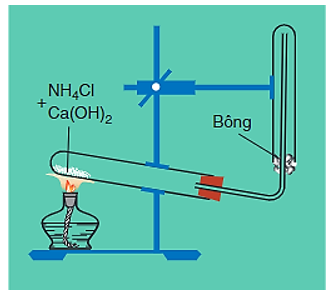
Hình 4: Điều chế khí amoniac trong phòng thí nghiệm
Lưu ý:
- Để làm khô khí, người ta cho khí amoniac vừa tạo thành có lẫn hơi nước đi qua bình đựng vôi sống (CaO).
- Khi muốn điều chế nhanh 1 lượng nhỏ khí N, người ta thường đun nóng dung dịch amoniac đậm đặc.
2. Trong công nghiệp
- Tổng hợp từ nitơ và hiđro, theo phản ứng:
+ 3 2N
- Điều kiện áp dụng:
+ Nhiệt độ: 450 – 500C.
+ Áp suất cao từ 200 – 300 atm.
+ Chất xúc tác: sắt kim loại được trộn thêm A, O, ...
- Làm lạnh hỗn hợp khí bay ra, N hóa lỏng được tách riêng.
B. MUỐI AMONI
- Là tinh thể ion gồm cation và anion gốc axit.
Thí dụ: NCl (amoni clorua), NN (amoni nitrat).
I. Tính chất vật lý
- Tất cả các muối amoni đều tan nhiều trong nước.
- Khi tan trong nước, điện li hoàn toàn thành các ion.
NCl → + Cl-
1. Tác dụng với dung dịch kiềm
- Dung dịch đậm đặc của muối amoni phản ứng với dung dịch kiềm khi đun nóng sinh ra khí amoniac.
Thí dụ:
NCl + NaOH N↑ + NaCl + O
Phương trình ion rút gọn là:
+ → N↑ + O
→ Phản ứng này để nhận biết ion amoni và điều chế amoniac trong phòng thí nghiệm.
2. Phản ứng nhiệt phân
Các muối amoni dễ bị phân hủy bởi nhiệt.
- Muối amoni chứa gốc của axit không có tính oxi hóa khi nung nóng bị phân hủy thành NH3.
Thí dụ:
NCl (r) N↑ + HCl↑
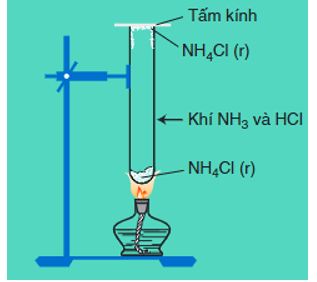
Hình 5: Sự phân hủy của NCl
- Các muối amoni cacbonat và amoni hiđrocacbonat bị phân hủy dần dần ngay ở nhiệt độ thường, khi đun nóng thì phản ứng xảy ra nhanh hơn.
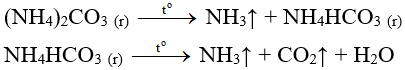
Lưu ý: NHC (bột nở) được dùng làm xốp bánh.
- Muối amoni chứa gốc của axit có tính oxi hóa như axit nitrơ, axit nitric khi bị nhiệt phân cho ra , O.
Thí dụ:
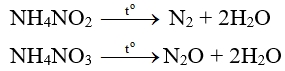
⇒ Những phản ứng này được sử dụng để điều chế các khí và O trong phòng thí nghiệm.