Cho 2 thí nghiệm sau:
Thí nghiệm 1: Cho 6,4 gam Cu phản ứng với 120 ml dung dịch HNO3 1M được a lít NO.
Thí nghiệm 2: Cho 6,4 gam Cu phản ứng với 120 ml dung dịch HNO3 1M và H2SO4 0,5M được b lít NO.
Biết NO là sản phẩm khử duy nhất của N+5. Mối liên hệ giữa a và b là
A. a = b
B. 2a = b
C. a = 2b
D. 2a = 3b
 Giải bởi Vietjack
Giải bởi Vietjack
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
TN1: nCu = 0,1 mol; nHNO3 = 0,12 mol
Xét
=> H+ hết, Cu và NO3- dư => phản ứng tính theo H+
nNO (1) = 1/4.nH+ = 1/4.0,12 = 0,03 mol
TN2: nCu = 0,1 mol; nH+ = 0,24 mol; nNO3- = 0,12 mol
Xét
=> H+ hết, Cu và NO3- dư => phản ứng tính theo H+
nNO (2) = 1/4.nH+ = 1/4.0,24 = 0,06 mol
=> nNO (2) = 2.nNO (1) => b = 2a
Đáp án cần chọn là: B
Chú ý
+ Xét dư thừa => tính NO theo chất hết
+ Ở thí nghiệm 2 cần tính tổng số mol H+
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2 thu được hỗn hợp khí X (tỉ khối của X so với khí hiđro bằng 18,8). Khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là
Cho hỗn hợp X chứa 18,6 gam gồm Fe, Al, Mg, FeO, Fe3O4 và CuO. Hòa tan hết trong dung dịch HNO3 dư thấy có 0,98 mol HNO3 tham gia phản ứng thu được 68,88 gam muối và 2,24 lít (đktc) khí NO duy nhất. Mặt khác, từ hỗn hợp X ta có thể điều chế được tối đa m gam kim loại. Giá trị của m là
Tỉ lệ số phân tử HNO3 đóng vai trò chất oxi hóa và môi trường trong phản ứng sau là : FeO + HNO3 → Fe(NO3)3 + NO + H2O
Cho hỗn hợp gồm 7,2 gam Mg và 10,2 gam Al2O3 tác dụng hết với lượng dư dung dịch HNO3. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,448 lít khí N2 duy nhất (đo ở đktc) và dung dịch Y. Khối lượng muối tan trong dung dịch Y là
Cho m gam hỗn hợp X (gồm Mg, Al, Zn và Cu) tác dụng hết với dung dịch HNO3 thu được dung dịch Y (không có muối amoni) và 11,2 lít (đktc) hỗn hợp khí Z (gồm N2, NO, N2O và NO2, trong đó N2 và NO2 có phần trăm thể tích bằng nhau) có tỉ khối đối với heli bằng 8,9. Số mol HNO3 phản ứng là
Hỗn hợp X gồm Mg(0,10 mol), Al(0,04 mol), Zn(0,15 mol). Cho X tác dụng với dung dịch HNO3 loãng dư, sau phản ứng thu được dung dịch có khối lượng tăng 13,23 gam. Số mol HNO3 tham gia phản ứng là
Hoà tan hoàn 12,4 gam hỗn hợp X gồm Fe và Cu bằng dung dịch HNO3 1M vừa đủ, sau phản ứng thu được dung dịch A gồm 2 muối Fe(NO3)3 và Cu(NO3)2 đồng thời thu được hỗn hợp khí Y gồm: 0,1 mol NO và 0,15 mol NO2 (đktc). Phần trăm theo khối lượng Fe có trong hỗn hợp là:
Cho 29 gam hỗn hợp gồm Al, Cu và Ag tác dụng vừa đủ với 950 ml dung dịch HNO3 1,5M, thu được dung dịch chứa m gam muối và 5,6 lít hỗn hợp khí X (đktc) gồm NO và N2O. Tỉ khối của X so với H2 là 16,4. Giá trị của m là
Hòa tan hỗn hợp gồm 2,8 gam Fe và 1,6 gam Cu trong 500ml dung dịch hỗn hợp HNO3 0,1M và HCl 0,4M, thu được khí NO (là sản phẩm khử duy nhất) và dung dịch X. Cho X vào dung dịch AgNO3 dư, thu được m (gam) chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là:
Nhiệt phân một lượng AgNO3 được chất rắn X và hỗn hợp khí Y. Dẫn toàn bộ Y vào một lượng dư H2O, thu được dung dịch Z. Cho toàn bộ X vào Z, X chỉ tan một phần và thoát ra khí NO (sản phẩm khử duy nhất). Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của X đã phản ứng là
Cho 4,8 gam S tan hết trong 100 gam HNO3 63% thu được NO2 (sản phẩm khử duy nhất, khí duy nhất) và dung dịch X. Dung dịch X có thể hoà tan hết tối đa bao nhiêu gam Cu (biết sản phẩm khử sinh ra là NO2)?
Hỗn hợp X gồm Al và Fe có tỉ lệ số mol tương ứng là 1:1. Cho 2,49 gam X vào dung dịch chứa 0,17 mol HCl, thu được dung dịch Y. Cho 200 ml dung dịch AgNO3 1M vào Y, thu được khí NO và m gam chất rắn. Biết các phản ứng xảy ra hoàn toàn, NO là sản phẩm khử duy nhất của N+5. Giá trị của m gần nhất với giá trị nào sau đây
Cho các phản ứng sau :
(1) nhiệt phân Cu(NO3)2;
(2) nhiệt phân NH4NO2;
(3) NH3 + O2 (t0, xt);
(4) NH3 + Cl2;
(5) nhiệt phân NH4Cl;
(6) NH3 + CuO.
Các phản ứng tạo ra được N2 là
Hòa tan hết hỗn hợp X gồm 5,6 gam Fe; 27 gam Fe(NO3)2 và m gam Al trong dung dịch chứa 0,61 mol HCl. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa 47,455 gam muối trung hòa và 2,352 lít khí (đktc) hỗn hợp khí Z gồm NO và N2O. Tỉ khối hơi của Z so với H2 là 16. Giá trị của m là
A. AXIT NITRIC
I. Cấu tạo phân tử
- Công thức cấu tạo của HN:
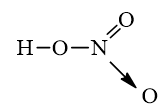
Chú ý: Mũi tên trong công thức cấu tạo trên cho biết cặp electron liên kết chỉ do nguyên tử N cung cấp.
- Trong hợp chất HN, nitơ có số oxi hóa cao nhất là +5.
II. Tính chất vật lý
- Axit nitric tinh khiết là chất lỏng không màu, bốc khói mạnh trong không khí ẩm.
- Axit nitric không bền, khi có ánh sáng phân hủy một phần sinh ra khí N. Khí này tan trong dung dịch axit, làm cho dung dịch có màu vàng.
4HN 4N↑ + ↑ + 2O
- Axit nitric tan vô hạn trong nước. Trong phòng thí nghiệm thường có loại HN đặc nồng độ 68%, D = 1,4 g/cm^3.
III. Tính chất hóa học
1. Tính axit
- Axit nitric là một trong số các axit mạnh nhất, trong dung dịch phân li hoàn toàn:
- Dung dịch axit HN có đầy đủ tính chất của một dung dịch axit: làm đỏ quỳ tím, tác dụng với oxit bazơ, bazơ, muối của axit yếu hơn.
Thí dụ:
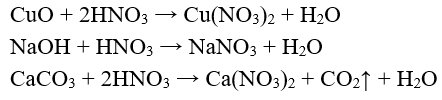
2. Tính oxi hóa
- HN có tính oxi hóa mạnh.
- Kim loại hay phi kim khi gặp axit HN đều bị oxi hóa lên trạng thái có mức oxi hóa cao nhất.
a) Tác dụng với kim loại
- HN oxi hóa hầu hết các kim loại trừ vàng (Au) và platin (Pt).
* Với những kim loại có tính khử yếu: Cu, Ag, ...
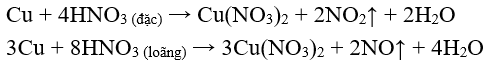
* Khi tác dụng với những kim loại có tính khử mạnh hơn: Mg, Zn, Al, ... thì HN loãng có thể bị khử đến O, hoặc NN.
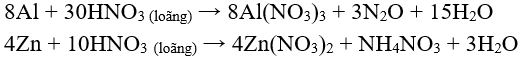
* Lưu ý: Fe, Al, Cr bị thụ động hóa trong dung dịch HN đặc, nguội.
b) Tác dụng với phi kim
- Khi đun nóng, HN đặc có thể tác dụng với phi kim: C, P, S, …(trừ và halogen).
Thí dụ:
S + 6HN (đ) → S + 6N↑ + 2O
c) Tác dụng với hợp chất
- S, HI, S, FeO, muối sắt (II), … có thể tác dụng với HN.
Thí dụ:
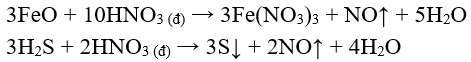
- Nhiều hợp chất hữu cơ như giấy, vải, dầu thông, … bốc cháy khi tiếp xúc với HN đặc.
IV. Ứng dụng
- Phần lớn sử dụng để điều chế phân đạm NN, …
- Ngoài ra, sử dụng sản xuất thuốc nổ, thuốc nhuộm, dược phẩm, …
V. Điều chế
1. Trong phòng thí nghiệm
Axit HN được điều chế bằng cách cho natri nitrat hoặc kali nitrat rắn tác dụng với axit S đặc, nóng:
NaN (rắn) + S (đặc) HN + NaHS
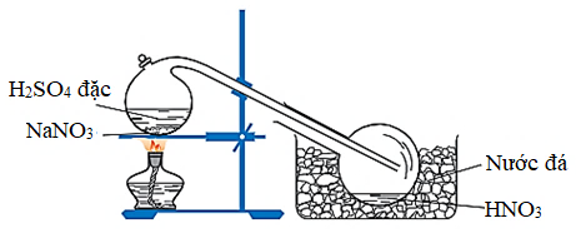
Hình 1: Điều chế axit nitric trong phòng thí nghiệm
2. Trong công nghiệp
- Được điều chế từ N qua ba giai đoạn:
N NO N HN.
a) Oxi hóa khí amoniac bằng oxi không khí
4N + 5 4NO + 6O;
b) Oxi hóa NO thành N bằng oxi không khí ở điều kiện thường
2NO + → 2N
c) Chuyển hóa N thành HN
4N + 2O + → 4HN
Dung dịch HN thu được thường có nồng độ 52 – 68%. Để có HN có nồng độ cao hơn 68% người ta thường chưng cất axit này với HN đậm đặc.
B. MUỐI NITRAT
- Muối của axit nitric được gọi là nitrat.
Thí dụ: natri nitrat NaN, bạc nitrat AgN,…
I. Tính chất vật lý
- Tất cả các muối nitrat đều dễ tan trong nước, là chất điện li mạnh trong dung dịch phân li hoàn toàn thành các ion.
Thí dụ:
Ca(N)2 → Ca2+ + 2
- Ion không màu, màu của 1 số muối nitrat là do màu của cation kim loại.
II. Tính chất hóa học
1. Nhiệt phân muối nitrat
a) Muối nitrat của các kim loại hoạt động mạnh (kali, natri,…)
Muối nitrat Muối nitrit + ↑
Thí dụ:
2NaN 2NaN + ↑
b) Muối nitrat của Mg, Zn, Fe, Pb, Cu,…
Muối nitrat Oxit kim loại + N↑ + ↑
Thí dụ:
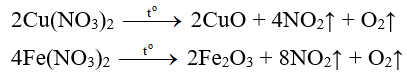
c) Muối nitrat của những kim loại Ag, Au, Hg,…
Muối nitrat Kim loại + N↑ + ↑
Thí dụ:
2AgN 2Ag + 2N↑ + ↑
2. Nhận biết ion nitrat
- Trong môi trường trung tính không có tính oxi hóa.
- Trong môi trường axit, ion thể hiện tính oxi hóa giống như HN.
⇒ Thuốc thử dùng để nhận biết ion là một ít vụn đồng và dung dịch S loãng, đun nóng.
Hiện tượng: dung dịch có màu xanh, khí không màu hóa nâu đỏ trong không khí.
3Cu + 8H+ + 2 → 3C+ + 2NO↑ + 4O
2NO + (không khí) → 2N (màu nâu đỏ)
III. Ứng dụng
- Các muối nitrat được sử dụng chủ yếu làm phân bón hóa học (phân đạm) trong nông nghiệp như NN, NaN, KN, Ca(N)2.

Hình 2: Một số loại phân đạm
- KN còn được sử dụng để chế thuốc nổ đen (thuốc nổ khói). Thuốc nổ đen chứa 75% KN, 10%S và 15% C.
C. Chu trình của nitơ trong tự nhiên
Nguyên tố nitơ rất cần cho sự sống trên Trái Đất. Trong tự nhiên, luôn luôn diễn ra các quá trình chuyển hóa nitơ từ dạng này sang dạng khác theo một chu trình tuần hoàn khép kín.
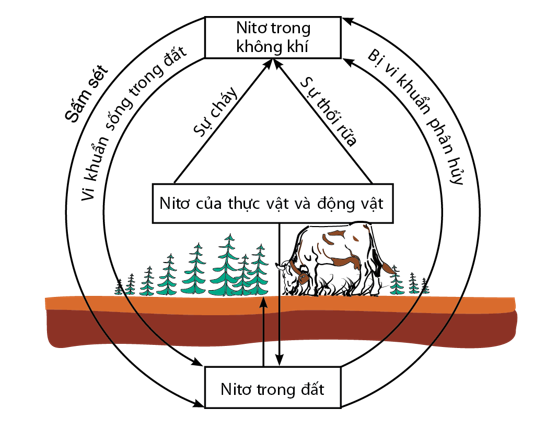
Hình 3: Chu trình của nitơ trong tự nhiên