Cho khí CO dư đi qua hỗn hợp gồm CuO, , MgO(nung nóng). Sau khi phản ứng xảy ra hoàn toàn chất rắn thu được gồm
A. Cu, Al, MgO
B.
C. Cu, Al, Mg
D.
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án B
Cho khí CO dư đi qua hỗn hợp gồm CuO, , MgO(nung nóng)→ chất rắn thu được gồm Cu, , MgO
Vì
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Cho một luồng khí CO đi qua ống đựng 10g nung nóng.Sau một thời gian thu được m gam hổn hợp X gồm 3 oxit sắt. Cho X tác dụng hết với dd 0,5M (vừa đủ) thu được dd Y và 1,12 lít NO (đktc) duy nhất. Thể tích CO đã dùng (đktc) và giá trị của m là
Từ 1 lít hỗn hợp CO và có thể điều chế tối đa bao nhiêu lít ? (H = 100%)
Thổi 0,5 mol khí vào dung dịch chứa 0,4 mol . Sau phản ứng thu được a mol kết tủa. Giá trị của a là
Khử hoàn toàn 32 gam hỗn hợp CuO và bằng khí , thấy tạo ra 9 gam nước. Tính khối lượng hỗn hợp kim loại thu được?
Dẫn 0,55 mol hỗn hợp X (gồm hơi nước và khí ) qua cacbon nung đỏ, thu được 0,95 mol hỗn hợp Y gồm CO, và . Cho Y hấp thụ vào dung dịch chứa 0,1 mol , sau khi phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là
Khử hoàn toàn 32 gam CuO bằng khí CO dư, thu được m gam kim loại. Giá trị của m là
Khử hoàn toàn 17,6 gam hỗn hợp gồm Fe, FeO, cần 4,48 lít (đktc). khối lượng sắt thu được là
Cho 2,24 lít (đktc) vào 200 ml dung dịch 1M, khối lượng kết tủa thu được là
Dẫn 0,02 mol hỗn hợp X (gồm hơi nước và khí ) qua cacbon nung đỏ, thu được 0,035 mol hỗn hợp Y gồm CO, và . Cho Y đi qua ống đựng 10 gam hỗn hợp gồm và CuO (dư, nung nóng), sau khi các phản ứng xảy ra hoàn toàn, thu được m gam chất rắn. Giá trị của m là
Khử hoàn toàn 4 gam hỗn hợp gồm CuO và PbO bằng khí CO dư ở nhiệt độ cao. Khí sinh ra được dẫn vào bình đựng nước vôi trong dư thu được 10 gam kết tủa. Khối lượng Cu và Pb thu được là:
Khi nung 200 kg đá vôi chứa 10% tạp chất. Nếu hiệu suất phản ứng đạt 90% thì lượng vôi sống thu được là
Khử hoàn toàn 14g hỗn hợp X gồm CuO và một oxit sắt bằng CO thu được 10,32g hỗn hợp Y gồm 2 kim loại. Thể tích CO (đktc) đã dùng cho quá trình trên là:
Cho hơi nước đi qua than nóng đỏ thu được 78,4 lít hỗn hợp khí X (đktc) gồm khí CO, . Khử hết 1/2 hỗn hợp X bằng CuO dư nung nóng được chất rắn Y. Hòa tan hoàn toàn Y trong dung dịch loãng thu được 22,4 lít (đktc) khí NO (sản phẩm khử duy nhất của ). Phần trăm thể tích khí CO trong X là
Đốt cháy không hoàn toàn một lượng sắt đã dùng hết 2,24 lít ở đktc, thu được hỗn hợp A gồm các oxit sắt và sắt dư. Khử hoàn toàn A bằng khí CO dư, khí đi ra sau phản ứng được dẫn vào bình đựng nước vôi trong dư. Khối lượng kết tủa thu được là
A – CACBON MONOOXIT
I. Cấu tạo phân tử và tính chất vật lí
- Cấu tạo của CO là C ≡ O (trong đó có 1 liên kết thuộc kiểu cho - nhận).
- CO là chất khí, không màu, không mùi, không vị, tan rất ít trong nước và rất bền với nhiệt, hóa lỏng ở -191,5C, hóa rắn ở -205,2C.
- CO là khí độc vì nó kết hợp với hemoglobin ở trong máu tạo thành hợp chất bền làm cho hemoglobin mất tác dụng vận chuyển khí .
II. Tính chất hóa học
- CO là oxit trung tính (oxit không có khả năng tạo muối) ⇒ không tác dụng với nước, dung dịch bazơ và dung dịch axit ở nhiệt độ thường.
- CO là chất khử mạnh:
+ Tác dụng với các phi kim
Thí dụ:
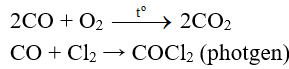
+ CO khử oxit của các kim loại đứng sau Al trong dãy hoạt động hóa học của kim loại (phản ứng xảy ra ở nhiệt độ cao).
Thí dụ:
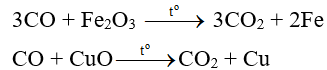
Chú ý: Dựa trên các tính chất hóa học này mà CO được ứng dụng để làm nhiên liệu khí, hay dùng trong luyện kim để khử các oxit kim loại.
III. Điều chế
1. Trong phòng thí nghiệm
- Đun nóng axit fomic (HCOOH) khi có mặt S đặc.
Phương trình hóa học:
HCOOH CO + O
2. Trong công nghiệp
- Khí CO được điều chế theo hai phương pháp:
+ Cho hơi nước đi qua than nung đỏ:
C + O CO +
⇒ Hỗn hợp khí tạo thành được gọi là khí than ướt. Ngoài CO (chiếm khoảng 44%), còn có các khí khác như C, ,…
+ Trong các lò gas, thổi không khí qua than nung đỏ:
Ở phần dưới của lò: C + C↑
Khí CO2 đi qua lớp than nung đỏ: CO2 + C 2CO
⇒ Hỗn hợp khí thu được gọi là khí lò gas (khí than khô). Trong khí lò gas, CO thường chiếm khoảng 25%, ngoài ra còn có C, ,…
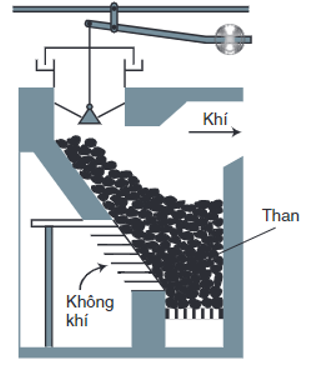
Hình 1: Sơ đồ lò gas
B – CACBON ĐIOXIT (C)
I. Cấu tạo phân tử và tính chất vật lý
1. Cấu tạo phân tử
- Cấu tạo của C là O = C = O.
- Phân tử C có cấu tạo thẳng, không phân cực.
2. Tính chất vật lý
- Là chất khí không màu, nặng gấp 1,5 lần không khí.
- Tan ít trong nước.
- C khi bị làm lạnh đột ngột chuyển sang trạng thái rắn, gọi là nước đá khô.
- Nước đá khô không nóng chảy mà thăng hoa nên được dùng để làm môi trường lạnh và khô, rất tiện lợi để bảo quản thực phẩm.

Hình 2: Đá khô
Lưu ý: Khi sử dụng đá khô phải đeo gang tay chống lạnh để tránh bị bỏng lạnh khi tiếp xúc với đá khô.
II. Tính chất hóa học
- Khí C không cháy, không duy trì sự cháy của nhiều chất.
- C là oxit axit, khi tan trong nước tạo thành axit cacbonic:
C (k) + O (l) ⇄ C (dd)
- Ngoài ra, C còn tác dụng với oxit bazơ và dung dịch kiềm.
Thí dụ:
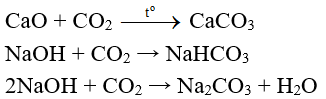
III. Điều chế
1. Trong phòng thí nghiệm
- CO2 được điều chế bằng cách cho dung dịch HCl tác dụng với đá vôi.
- Phương trình hóa học:
CaC + 2HCl → CaC + C↑ + O
2. Trong công nghiệp
- Khí C được thu hồi từ quá trình đốt cháy hoàn toàn than để cung cấp năng lượng cho các quá trình sản xuất khác.
C + C
- Ngoài ra, khí C còn được thu hồi từ quá trình chuyển hóa khí thiên nhiên, các sản phẩm dầu mỏ; quá trình nung vôi; quá trình lên men rượu từ đường glucozơ.
CaC CaO + C
2C + 2OH
C – AXIT CACBONIC VÀ MUỐI CACBONAT
I. Axit cacbonic (C)
- Là axit kém bền, chỉ tồn tại trong dung dịch loãng, dễ bị phân hủy thành C và O.
![]()
- Là axit hai nấc:
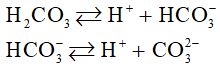
II. Muối cacbonat
Là muối của axit cacbonic (gồm muối và ).
1. Tính tan
- Muối cacbonat của các kim loại kiềm, amoni và đa số muối hiđrocacbonat dễ tan trong nước.
- Muối cacbonat của kim loại khác thì không tan.
2. Tính chất hóa học
a) Tác dụng với axit
Thí dụ:
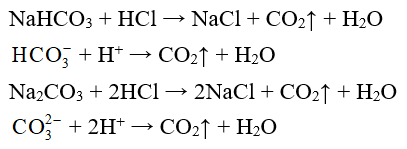
b) Tác dụng với dung dịch kiềm
- Các muối hiđrocacbonat tác dụng dễ dàng với dung dịch kiềm.
Thí dụ:
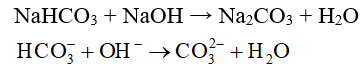
c) Phản ứng nhiệt phân
- Muối cacbonat tan không bị nhiệt phân (trừ muối amoni), muối cacbonat không tan bị nhiệt phân:
![]()
- Tất cả các muối hiđrocacbonat đều bị nhiệt phân:
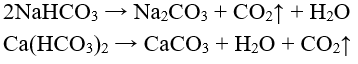
4. Ứng dụng
- Canxi cacbonat (CaC) tinh khiết là chất bột nhẹ, màu trắng, dùng làm chất độn trong cao su và 1 số ngành công nghiệp.
- Natri cacbonat (NC) khan (sođa khan) là chất bột màu trắng, tan nhiều trong nước. Dùng trong công ngiệp thủy tinh, đồ gốm, bột giặt, …
- Natri hiđrocacbonat (NaHC) là chất tinh thể màu trắng, hơi ít tan trong nước; dùng trong công nghiệp thực phẩm, trong y học dùng làm thuốc giảm đau dạ dày.