A, B, C là ba chất hữu cơ có %C, %H (theo khối lượng) lần lượt là 92,3% và 7,7%, tỉ lệ khối lượng mol tương ứng là 1: 2 : 3. Từ A có thể điều chế B hoặc C bằng một phản ứng. C không làm mất màu nước brom. Đốt 0,1 mol B rồi dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch nước vôi trong dư. Khối lượng bình tăng hay giảm bao nhiêu gam?
A. tăng 21,2 gam
B. tăng 40 gam
C. giảm 18,8 gam
D. giảm 21,2 gam
 Giải bởi Vietjack
Giải bởi Vietjack
%C : %H = 92,3% : 7,7% → nC : nH = 1 : 1
=> CTPT đơn giản nhất là (CH)n
Tỉ lệ số mol là 1:2:3, từ A có thể điều chế B hoặc C bằng 1 phản ứng; C khống làm mất màu nước brom
=> A là C2H2, B là C4H4, C là C6H6
Đốt 0,1 mol C4H4
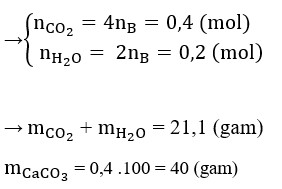
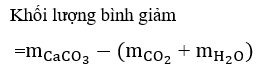
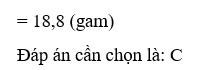
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Hỗn hợp gồm 1 mol C6H6 và 1,5 mol Cl2. Trong điều kiện có xúc tác bột Fe, to, hiệu suất 100%. Sau phản ứng thu được chất gì ? bao nhiêu mol ?
Ứng với công thức C9H12 có bao nhiêu đồng phân có cấu tạo chứa vòng benznen
Đốt cháy hoàn toàn hiđrocacbon X cho CO2 và H2O theo tỷ lệ mol 1,75 :1 về thể tích. Cho bay hơi hoàn toàn 5,06 gam X thu được một thể tích hơi đúng bằng thể tích của 1,76 gam oxi trong cùng điều kiện. Nhận xét nào sau đây là đúng đối với X?
Sử dụng thuốc thử nào để nhận biết được các chất sau: benzen, stiren, toluen và hex-1-in
Đốt cháy hết 9,18 gam hai đồng đẳng kế tiếp thuộc dãy đồng đẳng của stiren A, B thu được H2O và 30,36 gam CO2. Công thức phân tử của A và B lần lượt là :
Tiến hành trùng hợp 10,4 gam stiren được hỗn hợp X gồm polistiren và stiren dư. Cho X tác dụng với 200 ml dung dịch Br2 0,15M, sau đó cho dung dịch KI dư vào thấy xuất hiện 1,27 gam iot. Hiệu suất trùng hợp stiren là
Số lượng đồng phân chỉ chứa vòng benzen ứng với công thức phân tử C9H10 là :
Cho 100 ml benzen (d = 0,879 g/ml) tác dụng với một lượng vừa đủ brom lỏng (xúc tác bột Fe, đun nóng) thu được 80 ml brombenzen (d = 1,495 g/ml). Hiệu suất brom hóa đạt
1,3 gam chất hữu cơ A cháy hoàn toàn thu được 4,4 gam CO2 và 0,9 gam H2O. Tỷ khối hơi của A đối với oxi là d thỏa mãn điều kiện 3 < d < 3,5. Công thức phân tử của A là
A - Benzen và đồng đẳng
I - Đồng đẳng, đồng phân, danh pháp, cấu tạo
1. Dãy đồng đẳng của benzen
- Dãy đồng đẳng của benzen có công thức chung là CnH2n – 6 (n ≥ 6).
2. Đồng phân, danh pháp
- Cách đọc tên theo danh pháp hệ thống:
Tên = số chỉ vị trí nhánh + tên nhánh + benzen
Lưu ý:
+ Đánh số trên vòng sao cho tổng vị trí nhánh trên vòng là nhỏ nhất.
+ Nếu 2 nhóm thế trên vòng benzen ở vị trí: 1,2 – ortho; 1,3 – meta; 1,4 – para.
Thí dụ:
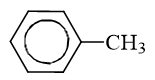 : có tên thông thường là toluen, tên thay thế là metylbenzen.
: có tên thông thường là toluen, tên thay thế là metylbenzen.
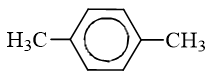 : có tên thông thường là p-xilen, tên thay thế là 1,4-đimetylbenzen (p-đimetylbenzen).
: có tên thông thường là p-xilen, tên thay thế là 1,4-đimetylbenzen (p-đimetylbenzen).
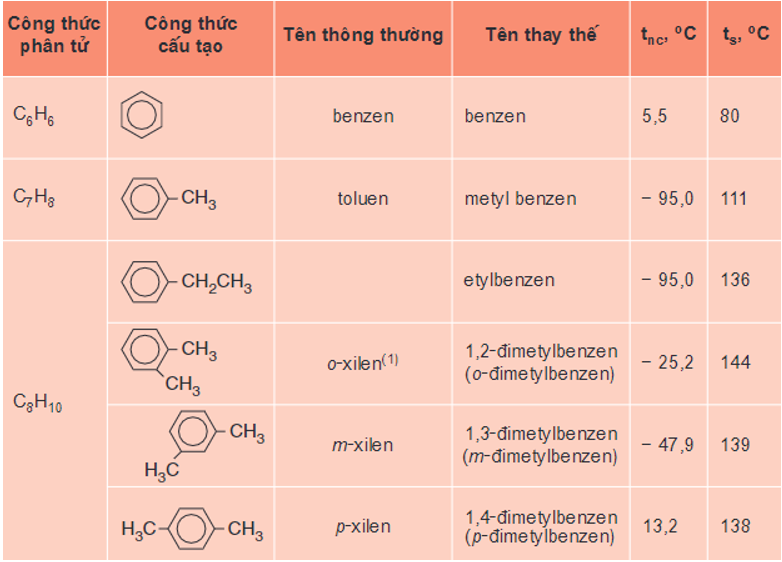
Bảng 1: Tên và hằng số vật lí của một số hiđrocacbon thơm đầu dãy đồng đẳng
- Từ trở đi có các đổng phân về vị trí tương đối của các nhóm ankyl xung quanh vòng benzen và về cấu tạo mạch cacbon của mạch nhánh.
3. Cấu tạo
- Công thức cấu tạo của benzen () là: 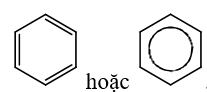
II. TÍNH CHẤT VẬT LÍ
- Các hiđrocacbon thơm đều là chất lỏng hoặc rắn ở điều kiện thường, chúng có nhiệt độ sôi tăng theo chiều tăng của phân tử khối.
- Các hiđrocacbon thơm ở thể lỏng có mùi đặc trưng, không tan trong nước và nhẹ hơn nước, có khả năng hoà tan nhiều chất hữu cơ.
III. TÍNH CHẤT HOÁ HỌC
Các đồng đẳng của benzen có tính chất của vòng benzen và có tính chất của mạch nhánh ankyl.
1. Phản ứng thế
a) Thế nguyên tử H của vòng benzen
* Phản ứng với halogen
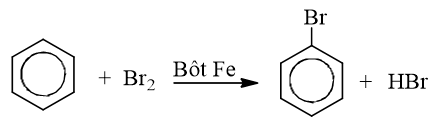
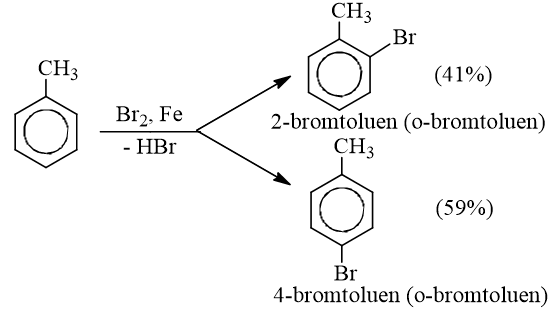
- Nếu cho các ankylbenzen phản ứng với brom trong điều kiện có bột sắt sẽ thu được hỗn hợp sản phẩm thế brom chủ yếu vào vị trí para và ortho so với nhóm ankyl:
* Phản ứng với axit nitric
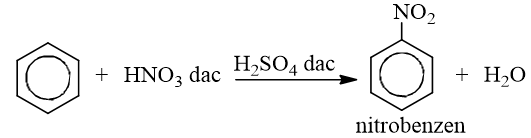
* Quy tắc thế: Các ankylbenzen dễ tham gia phản ứng thế nguyên tử H của vòng benzen hơn benzen và sự thế ưu tiên ở vị trí ortho và para so với nhóm ankyl.
b) Thế nguyên tử H của mạch nhánh
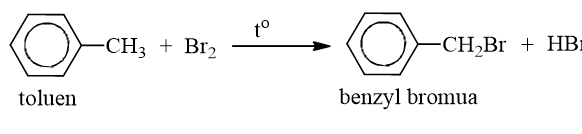
- Nếu đun toluen hoặc các ankylbenzen với brom, sẽ xảy ra phản ứng thế nguyên tử H của mạch nhánh tương tự ankan.
Thí dụ:
2. Phản ứng cộng
a) Cộng hiđro
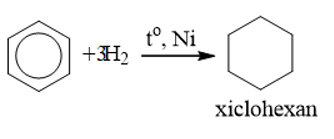
b) Cộng clo
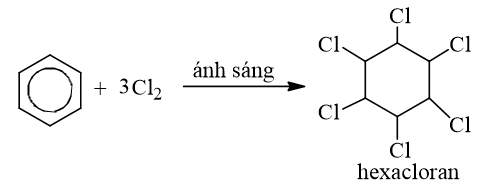
3. Phản ứng oxi hoá
a) Phản ứng oxi hoá không hoàn toàn
- Benzen và các ankylbenzen không làm mất màu dung dịch thuốc tím ở nhiệt độ thường.
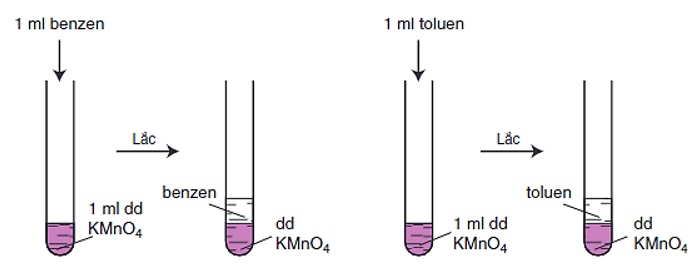
Hình 1: Benzen và toluen không làm mất màu dung dịch KMnO4 ở nhiệt độ thường
- Khi đun nóng, benzen không làm mất màu dung dịch thuốc tím nhưng ankylbenzen làm mất màu dung dịch thuốc tím
Thí dụ: Toluen làm mất màu dung dịch kali pemanganat.
Phương trình hóa học:
![]()
b) Phản ứng oxi hoá hoàn toàn
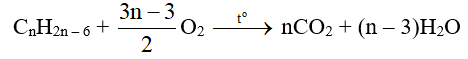
B - Một vài hiđrocacbon thơm khác
I. Stiren
1. Cấu tạo và tính chất vật lí
- Công thức phân tử:
- Công thức cấu tạo:
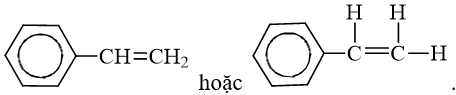
- Stiren (còn gọi là vinylbenzen) là chất lỏng không màu, sôi ở 146C, tan nhiều trong dung môi hữu cơ.
2. Tính chất hoá học
a) Phản ứng với dung dịch brom
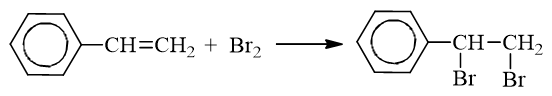
b) Phản ứng với hiđro
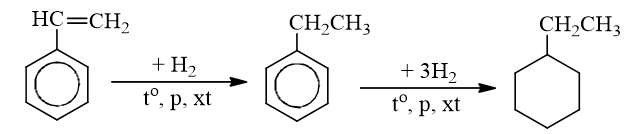
c) Phản ứng trùng hợp
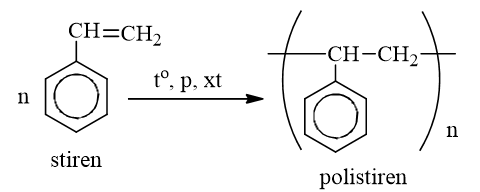
II. Naphtalen
1. Cấu tạo và tính chất vật lí
- Công thức phân tử:
- Phân tử naphtalen có cấu tạo phẳng:
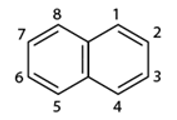
- Naphtalen (băng phiến) là chất rắn, nóng chảy ở 80C, tan trong benzen, ete,... và có tính thăng hoa.
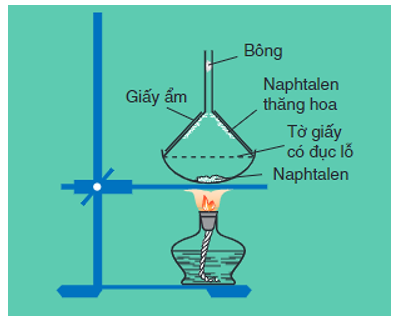
Hình 2: Thí nghiệm naphtalen thăng hoa
2. Tính chất hoá học
- Naphtalen không làm mất màu dung dịch KMn ở điều kiện thường.
- Naphtalen có tính chất hóa học tương tự benzen.
a) Phản ứng thế
- Naphtalen tham gia phản ứng thế tương tự benzen, nhưng phản ứng xảy ra dễ dàng hơn và thường ưu tiên thế vào vị trí số 1.
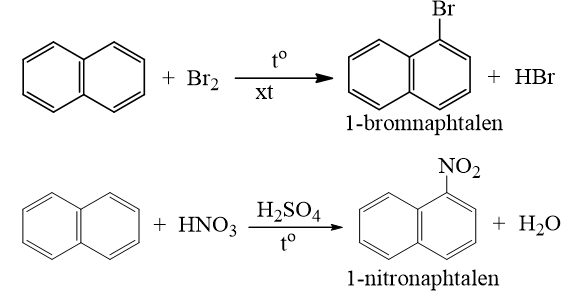
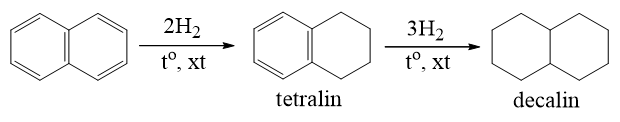
b) Phản ứng cộng
- Khi có chất xúc tác, naphtalen cộng hiđro tạo ra đecalin:
C - Ứng dụng của một số hiđrocacbon thơm
- Benzen và toluen là nguyên liệu rất quan trọng cho công nghiệp hoá học.
- Nguồn cung cấp benzen, toluen chủ yếu là từ nhựa than đá và từ sản phẩm đề hiđro đóng vòng hexan, heptan tương ứng.

Hình 3: Một số ứng dụng của hiđrocacbon thơm