Điện phân (với cực điện trơ, màng ngăn xốp) dung dịch gồm 0,2 mol , 0,2 mol và 0,4 mol NaCl. Biết rằng hiệu suất điện phân đạt 100%. Điều khẳng định nào sau đây là đúng ?
A. Khi khối lượng catot tăng 12,8 gam thì dung dịch hoàn toàn chỉ có màu nâu vàng
B. Khi khối lượng catot tăng lên 6,4 gam thì đã có 19300 culong chạy qua bình điện phân
C. Khi có 4,48 lít khí (đktc) thoát ra ở anot thì khối lượng catot không thay đổi
D. Khi có khí bắt đầu thoát ra ở catot thì đã có 8,96 lít khí (đktc) thoát ra ở anot
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án C
Trong dung dịch ban đầu có 0,4 mol , 0,2 mol , 0,4 mol và các ion khác không tham gia phản ứng điện phân
- Khi catot tăng 12,8 gam, tức là Cu2+ vừa hết, phản ứng (2) vừa kết thúc. Khi đó dung dịch chỉ có màu trắng xanh của Fe2+ nên phương án A sai
- Khi khối lượng catot tăng lên 6,4 gam, tức là đã có 0,1 mol Cu2+ bị điện phân. Vậy phản ứng (1) đã xảy ra hết, phản ứng (2) xảy ra một phần
Áp dụng công thức :
Trong đó ni là số mol chất i (phân tử hoặc ion) bị điện phân, zi là số e của chất i trao đổi ở điện cực
Ta có: q = (0,4.1 + 0,1.2).96500= 57900 (C)
Phương án B sai
- Khi có 4,48 lít khí thoát ra ở anot, tức là có 0,2 mol khí thoát ra suy ra phản ứng (a) xảy ra hoàn toàn và vừa đủ. Tại anot có 0,4 mol e trao đổi
Đông thời tại catot phản ứng (1) xảy ra hoàn toàn và vừa đủ. Chưa có kim loại kết tủa trên điện cực. Phương án C đúng
- Khi có khí bắt đầu thoát ra ở catot tức là các phản ứng (1) (2) (3 ) (4) đã xảy ra hoàn toàn. Số e trao đổi ở catot là 1,4 mol.
Tại anot, phản ứng (a) đã xảy ra hoàn toàn và có 0,4 mol e đã tiêu thụ trong phản ứng (a), sinh ra 0,2 mol Clo
Số e tiêu thụ cho phản ứng (b) sẽ là 1 mol. Vậy có 0,25 mol khí oxi sinh ra.
Tổng số mol khí sinh ra tại anot trong trường hợp này là 10,08 lít. Phương án D sai
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Một học sinh đã đưa ra các phương án để điều chế đồng như sau :
(1) Điện phân dung dịch .
(2) Dùng kali cho vào dung dịch .
(3) Dùng cacbon khử CuO ở nhiệt độ cao.
(4) Dùng nhôm khử CuO ở nhiệt độ cao.
Trong các phương án điều chế trên, có bao nhiêu phương án có thể áp dụng đề điều chế đồng ?
Điện phân một dung dịch chứa đồng thời các cation . Thứ tự các kim loại sinh ra ở catot lần lượt là
Cho các kim loại : Li, Na, Ca, Al, Fe, Cu, Ag, Pt, bằng phương pháp điện phân có thể điều chế được bao nhiêu kim loại trong số các kim loại trên ?
Một nhóm học sinh đã đề xuất các cách điều chế Ag từ như sau :
(1) Cho kẽm tác dụng với dung dịch
(2) Điện phân dung dịch
(3) Cho dung dịch tác dụng với dung dịch NaOH sau đó thu lấy kết tủa đem nhiệt phân.
(4) Nhiệt phân
Trong các cách điều chế trên, có bao nhiêu cách có thể áp dụng để điều chế Ag từ ?
Những kim loại nào sau đây có thể được điều chế từ oxit bằng phương pháp nhiệt luyện nhờ chất khử CO?
Cho các chất sau đây : NaOH, , NaCl, và . Có bao nhiêu chất điều chế được Na chỉ bằng 1 phản ứng ?
Cho hơi nước qua than nóng đỏ thu được 2,24 lít hỗn hợp khí X gồm , CO và (đo ở đktc). Dẫn X qua hỗn hợp gồm CuO và dư nung nóng thu dược m gam chất rắn và hỗn hợp khí và hơi Y. Dẫn Y qua dung dịch dư, lọc bỏ kết tủa thấy khối lượng dung dịch giảm 1,16 gam. Khối lượng kim loại có trong m là
Điện phân 1 lit dung dịch có chứa 18,8 gam và 29,8 gam KCl bằng điện cực trơ, có màng ngăn xốp. Sau 1 thời gian thấy khối lượng dung dịch giảm 34,3 gam so với ban đầu. Coi thể tích dung dịch không đổi trong quá trình điện phân, Nồng độ các chất trong dung dịch sau khi điện phân là
Cho khí CO (dư) đi qua ống sứ nung nóng đựng hỗn hợp X gồm: , CuO thu được chất rắn Y. Cho Y vào dung dịch NaOH (dư), khuấy kĩ, thấy còn lại phần không tan Z. Giả sử các phản ứng xảy ra hoàn toàn. Phần không tan Z gồm:
Trong quá trình điện phân dung dịch với các điện cực trơ, ion di chuyển về:
Trộn 0,54 gam bột nhôm với hỗn hợp gồm bột và CuO rồi tiến hành phản ứng nhiệt nhôm thu được hỗn hợp A. Hòa tan hoàn toàn A trong dung dịch thu được hỗn hợp khí gồm NO và có tỉ lệ số mol tương ứng là 1 : 3. Thể tích khí NO (ở đktc) là
Để điều chế Al kim loại ta có thể dùng phương pháp nào trong các phương pháp sau đây ?
I. Nguyên tắc điều chế kim loại
Nguyên tắc điều chế kim loại là khử ion kim loại thành nguyên tử.
Mn+ + ne → M
II. Phương pháp điều chế kim loại
Tùy thuộc vào độ hoạt động hóa học của kim loại mà người ta lựa chọn phương pháp điều chế phù hợp.
1. Phương pháp nhiệt luyện
- Nguyên tắc: Khử ion kim loại trong hợp chất ở nhiệt độ cao bằng các chất khử như C, CO, H2 hoặc các kim loại hoạt động (như Al).
- Phạm vi áp dụng: Sản xuất các kim loại có tính khử trung bình (Zn, Fe, Sn, Pb,…) trong công nghiệp.
- Ví dụ:
Fe2O3 + 3CO 2Fe + 3CO2
2. Phương pháp thuỷ luyện
- Nguyên tắc: Dùng những dung dịch thích hợp như: H2SO4, NaOH, NaCN,… để hoà tan kim loại hoặc các hợp chất của kim loại và tách ra khỏi phần không tan có ở trong quặng. Sau đó khử những ion kim loại này trong dung dịch bằng những kim loại có tính khử mạnh hơn như Fe, Zn,…
- Phạm vi áp dụng: Thường sử dụng để điều chế các kim loại có tính khử yếu.
- Ví dụ dùng Fe để khử ion Cu2+ trong dung dịch muối đồng.
Fe + CuSO4→ FeSO4 + Cu↓
Fe + Cu2+ → Fe2+ + Cu↓
3. Phương pháp điện phân
a. Điện phân hợp chất nóng chảy
- Nguyên tắc: Khử các ion kim loại bằng dòng điện bằng cách điện phân nóng chảy hợp chất của kim loại.
- Phạm vi áp dụng: Điều chế các kim loại hoạt động hoá học mạnh như K, Na, Ca, Mg, Al…
- Ví dụ điện phân Al2O3 nóng chảy là phương pháp sản xuất nhôm trong công nghiệp.
+ Ở catot (cực âm): Al3+ + 3e → Al
+ Ở anot (cực dương): 2O2- → O2 + 4e
Phương trình điện phân: 2Al2O3 4Al + 3O2
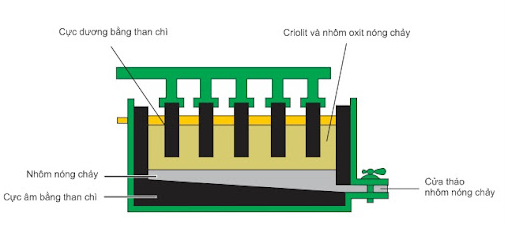
Sơ đồ thùng điện phân Al2O3 nóng chảy
b. Điện phân dung dịch
- Nguyên tắc: Khử các ion kim loại bằng dòng điện bằng cách điện phân dung dịch muối của kim loại.
- Phạm vi áp dụng: Điều chế các kim loại có độ hoạt động hoá học trung bình hoặc yếu như Zn, Cu …
- Ví dụ điện phân dung dịch CuCl2 để điều chế Cu:
+ Ở catot: Cu2+ + 2e → Cu
+ Ở anot: 2Cl- → Cl2 + 2e
Phương trình điện phân: CuCl2 Cu + Cl2
c) Tính lượng chất thu được ở các điện cực
Dựa vào công thức Farađây, có thể tính được khối lượng các chất thu được ở điện cực:
trong đó:
m: Khối lượng chất thu được ở điện cực (gam).
A: Khối lượng mol nguyên tử của chất thu được ở điện cực.
n: Số electron mà nguyên tử hoặc ion đã cho hoặc nhận.
I: Cường độ dòng điện (ampe)
t: Thời gian điện phân (giây)
F: Hằng số Farađây (F = 96500).