Có các hỗn hợp chất rắn
(1) FeO, BaO, Al2O3 (tỉ lệ mol 1: 1 : 1)
(2) Al, K, Al2O3 (tỉ lệ mol 1: 2: 1)
(3) Na2O, Al (tỉ lệ mol 1: 1)
(4) K2O, Zn (tỉ lệ mol 1: 1)
Số hỗn hợp tan hết trong nước (dư) là :
A. 0
B. 3
C. 4
D. 2
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án D
(1) không tan hết vì có FeO
(2) nKOH = nK = 2 mol
=> hỗn hợp không tan hết
(3) nNaOH = 2nNa2O = 2 mol
Vì nNaOH > nAl => hỗn hợp tan hết
(4) nKOH = 2nK2O = 2 mol
2KOH + Zn → K2ZnO2 + H2
2 mol 1 mol
=> hỗn hợp tan hết
Nhận xét: nếu nK ≥ nAl hoặc nK ≥ 2nZn thì hỗn hợp tan hết
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Cho bốn hỗn hợp, mỗi hỗn hợp gồm hai chất rắn có số mol bằng nhau: Na2O và Al2O3; Cu và Fe2(SO4)3; BaCl2 và CuCl2 ; Ba và NaHSO4. Số hỗn hợp có thể tan hoàn toàn trong nước (dư) chỉ tạo ra dung dịch là
Cho các phát biểu sau:
a, Al tan được trong dung dịch HCl và dung dịch NaOH.
b, Al khử được Cu2+ trong dung dịch.
c, Al3+ bị khử bởi Na trong dung dịch AlCl3.
d, Al2O3 là hợp chất kém bền với nhiệt.
Số phát biểu đúng là
Trộn 10,8 gam bột nhôm với 34,8 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng dư thu được 10,752 lít H2 (đktc). Giả sử Fe3O4 chỉ bị khử thành Fe. Hiệu suất phản ứng nhiệt nhôm là
Cho Al lần lượt vào các dung dịch : H2SO4 loãng, HNO3 (đậm đặc, to), Ba(OH)2, HNO3 loãng, H2SO4 đặc, thấy sinh ra khí B có tỉ khối so với O2 nhỏ hơn 0,8. Số dung dịch có thể phù hợp là :
Cho 10,8 gam bột Al và m gam hỗn hợp X gồm CuO và Fe3O4 vào bình chân không rồi nung nóng, thu được hỗn hợp rắn Y. Chia Y thành hai phần bằng nhau. Phần một cho tác dụng với dung dịch NaOH dư thấy thoát ra 0,06 mol khí H2, đồng thời thu được 18,08 gam hỗn hợp chất rắn không tan. Phần hai cho tác dụng hết với dung dịch HNO3 dư, thu được dung dịch Z chứa 106,16 gam muối và thoát ra 0,18 mol khí NO duy nhất. Khối lượng Fe3O4 có trong m gam X là
Cho các phương trình phản ứng sau đây
X + Y + 2H2O → Z + T (1)
T + NaOH → X + 2H2O (2)
Y + 2NaOH → E + H2O (3)
Y + E + H2O → 2Z (4)
Các chất Z, T, E là
Trộn 21,6 gam bột Al với m gam hỗn hợp X gồm (FeO, Fe2O3 và Fe3O4) được hỗn hợp Y. Nung Y ở nhiệt độ cao trong điều kiện không có không khí đến phản ứng hoàn toàn thu được chất rắn Z. Cho Z tác dụng vớii dung dịch NaOH dư thu được 6,72 lít khí. Nếu cho Z tác dụng với HNO3, loãng dư thì thu được 19,04 lít khí NO là sản phẩm khử duy nhất. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Giá trị của m là
Cho các chất : Al, Al2O3, Al2(SO4)3, Zn(OH)2, NaHS, KHSO3, (NH4)2CO3. Số chất có tính lưỡng tính là :
Tiến hành phản ứng nhiệt nhôm hỗn hợp X gồm 0,03mol Cr2O3; 0,04mol FeO và a mol Al. Sau một thời gian phản ứng, trộn đều thu được hỗn hợp chất rắn Y. Chia Y thành 2 phần bằng nhau. Phần I phản ứng vừa đủ với 400ml dung dịch NaOH 0,1M (loãng). Phần II phản ứng với dung dịch HCl loãng, nóng (dư) thu được 1,12 lít khí H2 (đktc). Giả sử trong phản ứng nhiệt nhôm, Cr2O3 chỉ bị khử thành Cr. % khối lượng Cr2O3 đã phản ứng là:
A. Nhôm (Al)
I. Vị trí trong bảng tuần hoàn và cấu hình electron nguyên tử
- Nhôm có số hiệu nguyên tử 13, thuộc nhóm IIIA, chu kì 3 của bảng tuần hoàn.
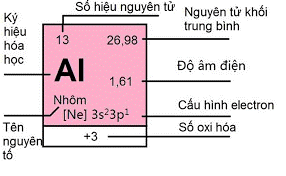
- Cấu hình electron: 1s22s22p63s23p1, hay [Ne]3s23p1 .
- Nhôm dễ nhường cả 3 electron hóa trị nên có số oxi hóa +3 trong các hợp chất.
II. Tính chất vật lý
- Nhôm là kim loại màu trắng bạc, nóng chảy ở 660oC, khá mềm, dễ kéo sợi, dễ dát mỏng.
- Nhôm là kim loại nhẹ (D = 2,7 g/cm3); dẫn điện, dẫn nhiệt tốt.

Nhôm
III. Tính chất hóa học
Nhôm là kim loại có tính khử mạnh (chỉ sau kim loại kiềm và kim loại kiềm thổ):
Al → Al3++ 3e
1. Tác dụng với phi kim
Nhôm khử dễ dàng các phi kim thành ion âm.
- Với oxi: Ở điều kiện thường, nhôm bền trong không khí do có lớp oxit rất mỏng, bền bảo vệ. Khi đốt, bột nhôm cháy trong không khí với ngọn lửa sáng chói, tỏa nhiều nhiệt:
4Al + 3O2 2Al2O3

Bột nhôm cháy trong không khí
- Bột nhôm tự bốc cháy khi tiếp xúc với clo
2Al + 3Cl2 → 2AlCl3
2. Tác dụng với axit
- Nhôm khử dễ dàng ion H+ trong dung dịch HCl và H2SO4 loãng thành H2.
2Al + 6HCl → 2AlCl3 + 3H2
- Al tác dụng mạnh với axit HNO3 loãng, H2SO4 đặc, nóng; HNO3 đặc, nóng.
Ví dụ:
Al + 4HNO3 loãng → Al(NO3)3 + NO + H2O
2Al + 6H2SO4 đặc Al2(SO4)3 + 3SO2 + 6H2O
- Nhôm không tác dụng với axit H2SO4 đặc, nguội; HNO3 đặc, nguội.
3. Tác dụng với oxit kim loại – Phản ứng nhiệt nhôm
- Ở nhiệt độ cao, Al khử được nhiều ion kim loại trong oxit như (Fe2O3, Cr2O3,CuO…) thành kim loại tự do.
- Ví dụ:
2Al + Fe2O3 Al2O3 + 2Fe.
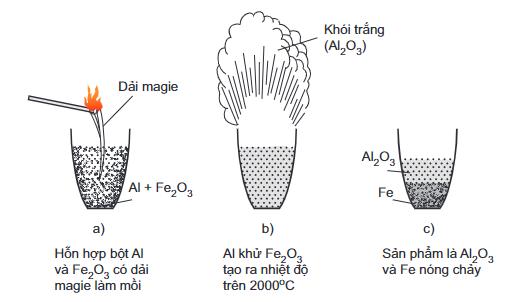
Phản ứng nhiệt nhôm
4. Tác dụng với nước
- Vật bằng nhôm không tác dụng với H2O ở bất kì nhiệt độ nào vì có lớp oxit bảo vệ. Nếu phá bỏ lớp bảo vệ, nhôm khử được nước ở nhiệt độ thường, nhưng phản ứng nhanh chóng dừng lại vì tạo kết tủa Al(OH)3.
5. Tác dụng với dung dịch kiềm
2Al + 2NaOH + 6H2O →2Na[(Al(OH)4] + 3 H2↑
Phương trình ion thu gọn:
2Al + 2OH- + 6H2O → 2[(Al(OH)4]- + 3 H2↑
Với chương trình cơ bản có thể viết:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3 H2 ↑
IV. Ứng dụng và trạng thái tự nhiên
1. Ứng dụng
- Nhôm và hợp kim của nhôm có ưu điểm nhẹ, bền đối với không khí và nước nên được dùng làm vật liệu chế tạo tên lửa, máy bay, ô tô, tàu vũ trụ …
- Nhôm và hợp kim của nhôm có màu trắng bạc, đẹp nên dùng để xây dựng nhà cửa, trang trí nội thất.
- Nhôm nhẹ, dẫn điện tốt nên được dùng làm dây dẫn điện.
- Nhôm dẫn điện tốt, ít bị gỉ, không độc nên được dùng làm dụng cụ nhà bếp.
- Bột nhôm trộn với oxit sắt (hỗn hợp tecmit) dùng để hàn đường ray.
2. Trạng thái tự nhiên
- Trong tự nhiên nhôm chỉ tồn tại dưới dạng hợp chất.
- Nhôm là nguyên tố phổ biến thứ 3 trong vỏ trái đất, sau oxi và silic.
- Hợp chất của nhôm có trong đất sét, mica, boxit, criolit …

Quặng boxit
V. Sản xuất nhôm
Trong công nghiệp nhôm được sản xuất bằng cách điện phân nhôm oxit nóng chảy.
1. Nguyên liệu
Quặng boxit, thành phần chính: Al2O3.2H2O
2. Điện phân nhôm oxit nóng chảy
+ Ở catot (cực âm): Al3+ + 3e → Al
+ Ở anot (cực dương): 2O2- → O2 + 4e
Phương trình điện phân: 2Al2O3 4Al + 3O2
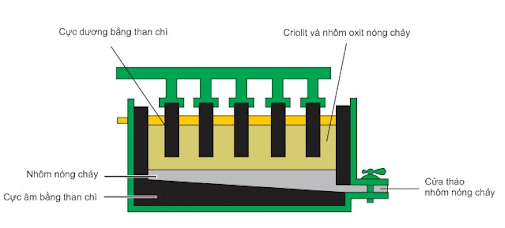
Sơ đồ thùng điện phân Al2O3 nóng chảy
Vai trò của criolit:
+ Giảm nhiệt độ nóng chảy của Al2O3.
+ Tăng khả năng dẫn điện của dung dịch điện phân.
+ Tạo lớp xỉ trên bề mặt, ngăn cản quá trình oxi hóa Al bởi oxi không khí.
B. Một số hợp chất quan trọng của nhôm
I. Nhôm oxit: Al2O3
1. Tính chất vật lý
Nhôm oxit là chất rắn màu trắng, không tan trong nước, không tác dụng với nước, nóng chảy ở nhiệt độ trên 2050oC.
2. Tính chất hóa học
Nhôm oxit là oxit lưỡng tính, vừa tác dụng với dung dịch axit, vừa tác dụng với dung dịch kiềm.
Al2O3 + 2NaOH → 2NaAlO2 + H2O
Al2O3 + 6HCl → 2AlCl3 + 3H2O
3. Ứng dụng
Trong tự nhiên, nhôm oxit tồn tại cả ở dạng ngậm nước và dạng khan.
- Dạng oxit ngậm nước là thành phần chủ yếu của quặng boxit dùng để sản xuất nhôm.
- Dạng oxit khan, có cấu tạo tinh thể là đá quý được dùng làm đồ trang sức, chế tạo đá mài …
- Bột nhôm oxit dùng trong công nghiệp sản xuất chất xúc tác cho tổng hợp hữu cơ.

Mẫu vật saphia
II. Nhôm hiđroxit: Al(OH)3
1. Tính chất vật lý
Nhôm oxit là chất rắn, màu trắng, kết tủa ở dạng keo.
2. Tính chất hóa học
+ Dễ bị nhiệt phân thành nhôm oxit:
2Al(OH)3 Al2O3 + 3H2O
+ Là hợp chất lưỡng tính, tan trong axit và bazơ:
Al(OH)3 + 3H+ → Al3+ + 3H2O
Al(OH)3 + OH- → AlO2- + 2H2O
III. Nhôm sunfat (Al2SO4)
- Muối nhôm sunfat khan tan trong nước tỏa nhiệt làm dung dịch nóng lên do bị hiđrat hóa.
- Muối nhôm sunfat có nhiều ứng dụng nhất là muối sunfat kép của nhôm và kali ngậm nước gọi là phèn chua, công thức K2SO4. Al2(SO4)3. 24H2O hay viết gọn KAl(SO4)2.12H2O.
- Phèn chua được sử dụng trong ngành thuộc da, công nghiệp giấy, chất cầm màu trong nhuộm vải, chất là trong nước…
IV. Cách nhận biết ion Al3+ trong dung dịch
Cho từ từ dung dịch NaOH đến dư vào dung dịch thí nghiệm, nếu thấy có kết tủa keo xuất hiện rồi tan trong NaOH dư chứng tỏ có Al3+:
Al3+ + 3OH- → Al(OH)3↓
Al(OH)3 ↓ + OH- dư → AlO2- + 2H2O