Nêu một số điểm cần chú ý trong quá trình chuẩn độ.
 Giải bởi Vietjack
Giải bởi Vietjack
Một số điểm cần lưu ý trong quá trình chuẩn độ:
- Tránh để các hoá chất như dung dịch HCl, dung dịch NaOH bắn vào tay, mắt.
- Các dụng cụ thuỷ tinh (bình tam giác, burette, pipette …) dễ vỡ, cần cẩn thận.
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Kết quả thử tính dẫn điện với dung dịch HCl 0,1 M và dung dịch CH3COOH 0,1 M cho thấy trường hợp cốc đựng dung dịch HCl 0,1 M bóng đèn sáng hơn.
Thực hiện yêu cầu sau:
Hãy so sánh số ion mang điện trong hai dung dịch trên, từ đó cho biết acid nào phân li mạnh hơn.
Một học sinh làm thí nghiệm xác định độ pH của đất như sau: Lấy một lượng đất cho vào nước rồi lọc lấy phần dung dịch. Dùng máy đo pH đo được giá trị pH là 4,52.
a) Hãy cho biết môi trường của dung dịch là acid, base hay trung tính.
b) Loại đất trên được gọi là đất chua. Hãy đề xuất biện pháp để giảm độ chua, tăng độ pH của đất.
Nước Javel (chứa NaClO và NaCl) được dùng làm chất tẩy rửa, khử trùng. Trong dung dịch, ion ClO- nhận proton của nước để tạo thành HClO.
a) Viết phương trình hoá học của phản ứng xảy ra và xác định chất nào là acid, chất nào là base trong phản ứng trên.
b) Dựa vào phản ứng, hãy cho biết môi trường của nước Javel là acid hay base.
Thí nghiệm thử tính dẫn điện của nước, muối ăn và dung dịch muối ăn được thực hiện như mô tả trong Hình 2.2.
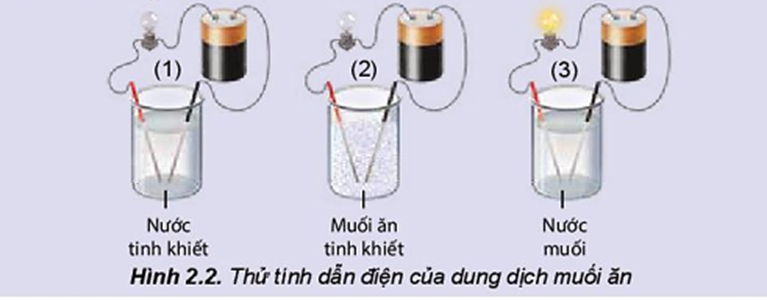
Thực hiện yêu cầu:
a) Hãy nhắc lại khái niệm dòng điện.
b) Đèn sáng cho thấy dung dịch NaCl dẫn điện, chứng tỏ dung dịch có hạt mang điện. Đó có thể là loại hạt nào (electron, phân tử NaCl, cation hay anion)?
c) Hãy giải thích sự tạo thành các hạt mang điện đó.
Dựa vào thuyết acid – base của Br∅nsted – Lowry, hãy xác định chất nào là acid, chất nào là base trong các phản ứng sau:
a) CH3COOH + H2O ⇌ CH3COO- + H3O+
b) S2- + H2O ⇌ HS- + OH-
Chuẩn bị:
- Hoa đậu biếc (khoảng 50 g) hoặc bắp cải tím thái nhỏ (khoảng 100 g).
- Cốc thuỷ tinh 250 mL, nước sôi, đũa thuỷ tinh, lưới/ vải lọc.
- Các cốc (đã được dán nhãn) đựng giấm ăn, nước C sủi, nước rửa bát, nước soda, nước muối.
- Giấy pH hoặc máy đo pH.
Tiến hành:
– Ngâm khoảng 50 g hoa đậu biếc/100 g bắp cải tím đã được chuẩn bị vào 100 mL nước sôi trong khoảng 10 phút. Lọc bằng lưới lọc hoặc vải lọc, thu được dung dịch. Dung dịch này được sử dụng làm chất chỉ thị.
– Dùng máy đo pH (hoặc giấy pH) xác định pH của các dung dịch.
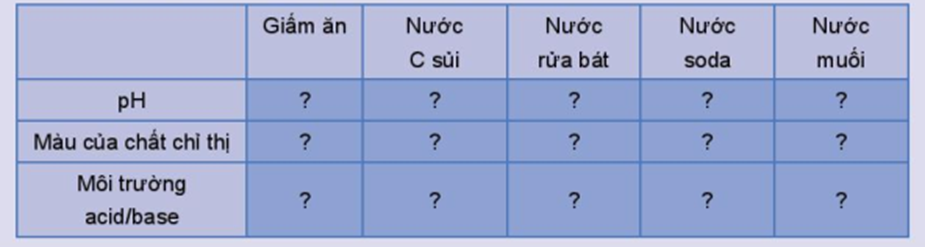
- Cho vài giọt chất chỉ thị lần lượt vào các dung dịch: giấm ăn, nước C sủi, nước rửa bát, nước soda, nước muối và khuấy đều. Quan sát sự đổi màu của các dung dịch.
Hoàn thành thông tin theo mẫu bảng sau vào vở:
Một loại dầu gội đầu có nồng độ ion OH- là 10-5,17 mol/ L.
a) Tính nồng độ ion H+, pH của loại dầu gội nói trên.
b) Môi trường của loại dầu gội trên là acid, base hay trung tính?
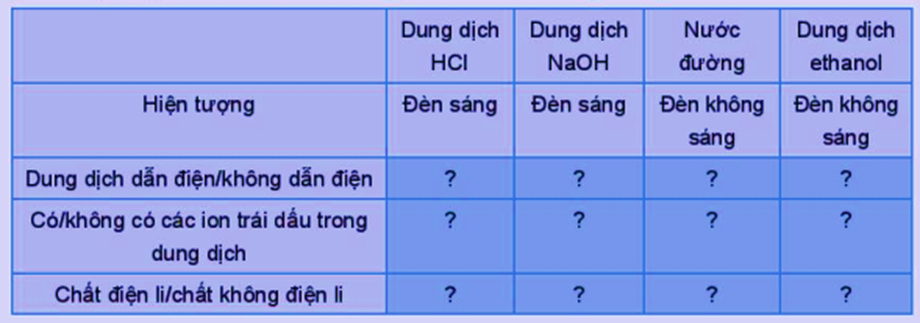
Kết quả thử tính dẫn điện với các dung dịch hydrochloric acid (HCl), sodium hydroxide (NaOH), saccharose (C12H22O11), ethanol (C2H5OH) được trình bày trong bảng dưới đây. Hãy hoàn thành các thông tin còn thiếu trong bảng vào vở:
Nêu một số nguyên nhân có thể dẫn đến sai số trong quá trình chuẩn độ.
Viết phương trình điện li của các chất sau: HF, HI, Ba(OH)2, KNO3, Na2SO4.
Cho các dung dịch sau: Na2CO3, AlCl3, FeCl3.
1. Dùng giấy pH xác định giá trị pH gần đúng của các dung dịch trên.
2. Nhận xét và giải thích về môi trường của các dung dịch trên.
c) Theo khái niệm acid – base trong môn Khoa học tự nhiên ở lớp 8, trong những chất cho ở trên: Chất nào là acid? Chất nào là base?
Hình 2.1 cho thấy giá trị pH của dung dịch một số chất thông dụng. Vậy pH là gì? pH có ảnh hưởng gì đến đời sống? Xác định pH như thế nào?

Đo PH của một cốc nước chanh được giá trị pH bằng 2,4. Nhận định nào sau đây không đúng?