Cho 2 dung dịch axit là HNO3 và HClO có cùng nồng độ. Vậy sự so sánh nào sau đây là đúng?
 Giải bởi Vietjack
Giải bởi Vietjack
Vì HNO3 phân li hoàn toàn, còn HClO phân li ít nên lượng
[H+]HNO3 > [H+]HClO
Đáp án cần chọn là: D
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Hòa tan hoàn toàn m gam Al2(SO4)3 vào nước thu được dung dịch A chứa 0,6 mol Al3+
Hòa tan 14,2 gam Na2SO4 trong nước thu được dung dịch A chứa số mol ion SO42- là:
Dung dịch amoniac trong nước có chứa các ion nào sau đây (bỏ qua sự phân li của nước):
Trong số những chất sau : H2S; FeCl3; Cl2; CO2; Ba(OH)2 có bao nhiêu chất khi tan trong nước là chất điện li?
Trong dung dịch axit axetic (bỏ qua sự phân li của H2O) có những phần tử nào?
Đối với dung dịch axit yếu HNO2 0,01M, nếu bỏ qua sự điện li của nước thì đánh giá nào sau đây là đúng?
Độ điện li α của chất điện li phụ thuộc vào những yếu tố nào sau đây?
Cho dãy các chất: KAl(SO4)2.12H2O, C2H5OH, C12H22O11 (saccarozơ), SO2, CH3COOH, N2O5, CuO, Ca(OH)2, CH3COONH4. Số chất điện li là
Nồng độ mol của cation và anion trong dung dịch Ba(NO3)2 0,02 M là:
Nồng độ ion H+ trong 200 ml dung dịch H2SO4 0,25M là (coi H2SO4 là chất điện li hoàn toàn):
Cho 2 dung dịch axit là HNO3 và HClO có cùng nồng độ. Vậy sự so sánh nào sau đây là đúng?
Dung dịch H2SO4 và HNO3 là axit mạnh còn HNO2 là axit yếu có cùng nồng độ 0,01 mol/l và ở cùng nhiệt độ. Nồng độ ion H+ trong mỗi dung dịch được sắp xếp theo chiều tăng dần là:
Trong dung dịch Fe2(SO4)3 loãng có chứa 0,45 mol SO42- thì trong dung dịch có chứa:
I. Hiện tượng điện li
1. Thí nghiệm
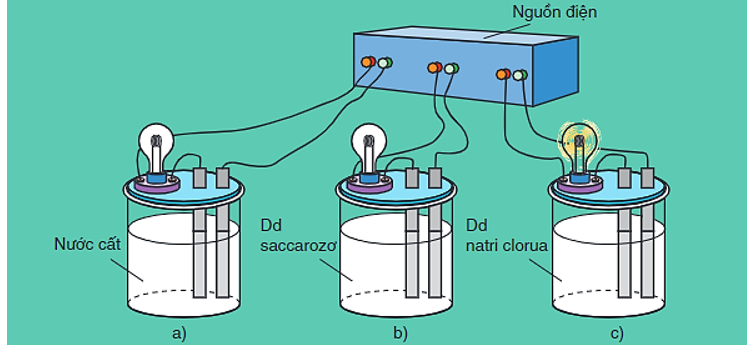
Hình 1: Bộ dụng cụ chứng minh tính dẫn điện của dung dịch
- Khi nối các đầu dây dẫn điện với cùng một nguồn điện, ta chỉ thấy bóng đèn ở cốc đựng dung dịch NaCl bật sáng.
⇒ Dung dịch NaCl dẫn điện, còn nước cất và dung dịch saccarozơ không dẫn điện.
- Nếu làm các thí nghiệm tương tự, người ta thấy:
+ NaCl rắn, khan; NaOH rắn, khan; các dung dịch ancol etylic (OH), glixerol ((OH)3) không dẫn điện.
+ Các dung dịch axit, bazơ và muối đều dẫn điện.
2. Nguyên nhân tính dẫn điện của các dung dịch axit, bazơ và muối trong nước
Nguyên nhân: Các dung dịch axit, bazơ và muối dẫn điện được là do trong dung dịch của chúng có các tiểu phân mang điện tích chuyển động tự do được gọi là các ion.
3. Các khái niệm cần nắm vững
- Sự điện li là quá trình phân li các chất trong nước ra ion.
- Chất điện li là những chất khi tan trong nước phân li ra ion.
⇒ Axit, bazơ và muối là những chất điện li.
- Sự điện li được biểu diễn bằng phương trình điện li.
Ví dụ:
- Muối phân li thành cation kim loại (hoặc cation amoni) và anion gốc axit:
NCl → N+ + Cl-
- Axit phân li thành cation H+ và anion gốc axit:
- Bazơ phân li thành cation kim loại và anion hiđroxit:
Chú ý: Nhiều chất khi nóng chảy cũng phân li ra ion, nên ở trạng thái nóng chảy các chất này dẫn điện được.
II. Phân loại các chất điện li
Dựa vào mức độ phân li ra ion, chất điện li được chia thành hai loại:
1. Chất điện li mạnh
- Chất điện li mạnh là chất khi tan trong nước, các phân tử hoà tan đều phân li ra ion.
- Những chất điện li mạnh là:
+ Các axit mạnh như HCl, HN, HCl, S, ...;
+ Các bazơ mạnh như NaOH, KOH, Ba(OH)2 ,...
+ Hầu hết các muối.
- Phương trình điện li, người ta dùng một mũi tên chỉ chiều của quá trình điện li.
Ví dụ:
Ba →
2. Chất điện li yếu
- Chất điện li yếu là chất khi tan trong nước chỉ có một phần số phân tử hoà tan phân li ra ion, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch.
- Những chất điện li yếu là:
+ Các axit yếu như CCOOH, HClO, S, HF, S, ... ;
+ Các bazơ yếu như Bi, Mg, ...
+ Một số muối: HgC; Hg; …
+ Nước (O).
- Trong phương trình điện li của chất điện li yếu, người ta dùng hai mũi tên ngược chiều nhau.
- Sự phân li của chất điện li yếu là quá trình thuận nghịch, khi nào tốc độ phân li và tốc độ kết hợp các ion tạo thành phân tử bằng nhau cân bằng của quá trình điện li được thiết lập.
Ví dụ:
CCOOH
Lưu ý: Cân bằng điện li là cân bằng động và tuân theo nguyên lí chuyển dịch cân bằng Lơ Sa-tơ-li-ê.