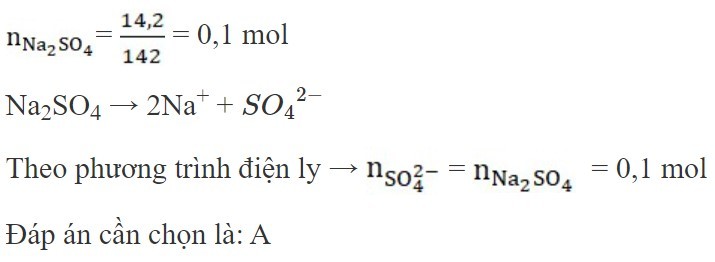Trắc nghiệm Sự điện li có đáp án (Thông hiểu)
-
1021 lượt thi
-
17 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Dung dịch nào dưới đây dẫn điện tốt nhất ?
 Xem đáp án
Xem đáp án
Cùng là muối NaCl điện li mạnh, dung dịch nào chứa nhiều ion nhất là dung dịch dẫn điện tốt nhất
Đáp án cần chọn là: C
Câu 2:
Trong số những chất sau : H2S; FeCl3; Cl2; CO2; Ba(OH)2 có bao nhiêu chất khi tan trong nước là chất điện li?
 Xem đáp án
Xem đáp án
Cl2; CO2 tan trong nước tạo thành HCl, HClO và H2CO3 là chất điện li nhưng không phải là Cl2 và CO2 ban đầu do đó không phải là chất điện li.
Đáp án cần chọn là: C
Câu 3:
Cho dãy các chất: KAl(SO4)2.12H2O, C2H5OH, C12H22O11 (saccarozơ), SO2, CH3COOH, N2O5, CuO, Ca(OH)2, CH3COONH4. Số chất điện li là
 Xem đáp án
Xem đáp án
Chất điện li gồm các muối, axit và bazo: KAl(SO4)2.12H2O, CH3COOH, Ca(OH)2, CH3COONH4.
Đáp án cần chọn là: B
Câu 4:
Trong dung dịch axit axetic (bỏ qua sự phân li của H2O) có những phần tử nào?
 Xem đáp án
Xem đáp án
CH3COOH là chất điện li yếu: CH3COOH ⇆ H+ + CH3COO-
Do vậy phần tử thu được gồm: CH3COOH, H+, CH3COO-, H2O.
Đáp án cần chọn là: C
Câu 5:
Dung dịch amoniac trong nước có chứa các ion nào sau đây (bỏ qua sự phân li của nước):
 Xem đáp án
Xem đáp án
NH3 + H2O ⇆ NH+4 + OH−
Đáp án cần chọn là: D
Câu 6:
Cho 2 dung dịch axit là HNO3 và HClO có cùng nồng độ. Vậy sự so sánh nào sau đây là đúng?
 Xem đáp án
Xem đáp án
Vì HNO3 phân li hoàn toàn, còn HClO phân li ít nên lượng
[H+]HNO3 > [H+]HClO
Đáp án cần chọn là: D
Câu 7:
Cho 2 dung dịch axit là HNO3 và HClO có cùng nồng độ. Vậy sự so sánh nào sau đây là đúng?
 Xem đáp án
Xem đáp án
HClO là một chất điện li yếu, HNO3 là chất điện li mạnh do đó
[H+]HNO3 > [H+]HClO
Đáp án cần chọn là: B
Câu 8:
Dung dịch H2SO4 và HNO3 là axit mạnh còn HNO2 là axit yếu có cùng nồng độ 0,01 mol/l và ở cùng nhiệt độ. Nồng độ ion H+ trong mỗi dung dịch được sắp xếp theo chiều tăng dần là:
 Xem đáp án
Xem đáp án
*H2SO4 → 2H+ + SO42-
0,01M → 0,02M
*HNO3 → H+ + NO3-
0,01M → 0,01M
*HNO2 → H+ + NO2-
0,01M => [H+] < 0,01M (do HNO2 là chất điện li yếu)
Đáp án cần chọn là: B
Câu 9:
Ion Na+.nH2O được hình thành khi :
 Xem đáp án
Xem đáp án
A đúng vì khi hòa tan trong nước NaCl phân li ra Na+ và Cl-. Khi đó Na+ sẽ kéo lấy các phần tử tích điện âm của nước tạo thành Na+.nH2O
Đáp án cần chọn là: A
Câu 10:
Nồng độ mol của cation và anion trong dung dịch Ba(NO3)2 0,02 M là:
 Xem đáp án
Xem đáp án
Ba(NO3)2 → Ba2+ + 2NO3−
[Ba2+]=0,02 M ; [NO3−] = 2. 0,02 = 0,04 M
Đáp án cần chọn là: B
Câu 12:
Hòa tan hoàn toàn m gam Al2(SO4)3 vào nước thu được dung dịch A chứa 0,6 mol Al3+
 Xem đáp án
Xem đáp án
Al2(SO4)3 → 2Al3+ + 3
Theo phương trình điện ly:
![]() = 1/2 .
= 1/2 .![]() = 0,3 mol
= 0,3 mol
=> ![]() = 0,3.342 = 102,6 gam
= 0,3.342 = 102,6 gam
Đáp án cần chọn là: A
Câu 13:
Trong dung dịch Fe2(SO4)3 loãng có chứa 0,45 mol SO42- thì trong dung dịch có chứa:
 Xem đáp án
Xem đáp án
Fe2(SO4)3 → 2Fe3+ + 3SO42-
0,15 ← 0,3 ← 0,45 (Mol)
Đáp án cần chọn là: C
Câu 14:
Nồng độ ion H+ trong 200 ml dung dịch H2SO4 0,25M là (coi H2SO4 là chất điện li hoàn toàn):
 Xem đáp án
Xem đáp án
Do H2SO4 là chất điện li hoàn toàn nên phương trình điện li là:
H2SO4 → 2H+ + SO42-
0,25M → 0,5M
Đáp án cần chọn là: D
Câu 15:
Độ điện li α của chất điện li phụ thuộc vào những yếu tố nào sau đây?
 Xem đáp án
Xem đáp án
Độ điện li α của chất điện li phụ thuộc vào những yếu tố:
+ Bản chất của chất điện li
+ Bản chất của dung môi
+ Nhiệt độ và nồng độ của chất tan
Đáp án cần chọn là: D
Câu 16:
Câu nào sau đây nói không đúng về độ điện li alpha (anpha)?
 Xem đáp án
Xem đáp án
Câu không đúng là: Độ điện li của các chất khác nhau là giống nhau
Đáp án cần chọn là: B
Câu 17:
Đối với dung dịch axit yếu HNO2 0,01M, nếu bỏ qua sự điện li của nước thì đánh giá nào sau đây là đúng?
 Xem đáp án
Xem đáp án
HNO2 ⇆ H+ + NO2−
HNO2 là axit yếu nên độ điện li α < 1
=> [H+] < 0,01M
Đáp án cần chọn là: C