200 ml dung dịch Na2SO40,1M. Số mol của ion Na+và SO42-lần lượt là
A.0,02 và 0,02
B.0,04 và 0,02
C.0,2 và 0,4
D.0,02 và 0,01
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án B
Số mol của dung dịch Na2SO4là n = CM.V = 0,1.0,2 = 0,02 mol
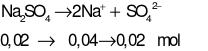
Vậy số mol của ion Na+và SO42-lần lượt là 0,04 và 0,02.
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Dãy ion nào sau đây có thể tồn tại đồng thời trong cùng một dung dịch:
Dãy gồm các ion (không kể đến sự phân li của nước) cùng tồn tại trong một dung dịch là:
Cho phản ứng: Ag + HNO3 AgNO3+ NO2+ H2O. Tổng hệ số tối giản các chất tham gia trong phương trình khi cân bằng là
Cho dung dịch A chứa các ion K+(0,01 mol), M+, SO42-, CO32-. Cho dung dịch A tác dụng với BaCl2dư thu được 8,96 gam kết tủa. Mặt khác cho dung dịch A tác dụng với H2SO4loãng dư thu được 0,224 lít khí (đktc). Khi cô cạn dung dịch A thu được 5,48 gam muối khan. Tìm ion M+( biết M+không kết tủa với ion Cl-).
Hoàn thành phương trình phân tử và viết phương trình ion thu gọn của các phản ứng sau:
a. MgCl2 + NaOH →
b. HNO3 + KOH →
Trộn các dung dịch HCl 0,75M, HNO30,15M; H2SO40,3M với các thể tích bằng nhau thì thu được dung dịch X. Trộn 150ml dung dịch X với 350ml dung dịch Ba(OH)20,1M thì thu được dung dịch Y có pH = x. Tìm x?
Cho các chất sau: Zn, Na2CO3, Cu(OH)2, Mg, NH3. Số chất tác dụng được với dung dịch HNO3là
Phản ứng của NH3dư với HCl tạo ra “khói trắng“, chất này có công thức hoá học là