Đốt một mẩu than chì chứa tạp chất lưu huỳnh trong oxi. Cho hỗn hợp khí thoát ra tác dụng với lượng dư dung dịch brom, thấy dung dịch brom nhạt màu. Cho khí thoát ra khỏi dung dịch brom đi qua nước vôi trong dư thấy có vẩn đục. Hỗn hợp khí thoát ra là:
A.
B.
C.
D.
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án A
Khí làm mất màu dung dịch brom là
Khí làm vẩn đục nước vôi trong là
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Cho các chất: , HCl (6), CaO (7), . Cacbon phản ứng trực tiếp được với bao nhiêu chất?
Cho 3,60 gam cacbon tác dụng với 8,10 gam nhôm. Khối lượng nhôm cacbua tạo thành nếu hiệu suất của phản ứng 70% là
Cho các nhận định sau, nhận định nào sai
1. Kim cương có cấu trúc tinh thể, rất cứng
2. Than chì: cấu trúc thành từng lớp, có màu đen, mềm, thường dùng làm bút chì, pin
3. Than hoạt tính có khả năng hấp phụ tốt
4. Than chì có cấu trúc tinh thể
5. Than gỗ, than hoạt tính là cacbon vô định hình
Các nhận định đúng là:
Cho cacbon tác dụng với các chất sau trong điều kiện thích hợp: (hơi), Al, , Ca, (đặc), (đặc), . Số phản ứng khi xảy ra, cacbon đóng vai trò chất khử là
Một loại than đá chứa 2% lưu huỳnh dùng cho một nhà máy nhiệt điện. Nếu nhà máy đốt hết 100 tấn than trong một ngày đêm thì khối lượng do nhà máy xả vào khí quyển trong một năm là :
Thể tích khí thoát ra ở đktc khi cho 0,12 gam cacbon tác dụng hết với đặc nguội (coi phản ứng xảy ra hoàn toàn) là
Cho các chất: , HCl (5), CaO (6), , KCl (10). Cacbon phản ứng trực tiếp được với bao nhiêu chất?
Đốt một mẩu than chì chứa tạp chất lưu huỳnh trong oxi. Cho hỗn hợp khí thoát ra tác dụng với lượng dư dung dịch brom, thấy có 0,32 gam brom đã tham gia phản ứng. Cho khí thoát ra khỏi dung dịch brom tác dụng với lượng dư nước vôi trong, thu được 10 gam kết tủa. Phần trăm khối lượng của cacbon trong than chì là:
Đốt cháy hỗn hợp lưu huỳnh và cacbon (thể tích không đáng kể) trong bình kín đựng oxi dư, thu được hỗn hợp ba khí . Sau đó đưa bình về nhiệt độ ban đầu thì áp suất trong bình so với trước khi đốt sẽ thay đổi như thế nào?
I. Vị trí, cấu hình electron và tính chất vật lý
1. Vị trí và cấu hình electron nguyên tử

Hình 1: Ô nguyên tố C
- Cacbon ở ô thứ 6, chu kỳ 2, nhóm IVA của bảng tuần hoàn.
- Cấu hình e: 1s^22s^22p^2 ⇒ C có 4 electron lớp ngoài cùng. Vì vậy C có thể tạo được tối đa 4 liên kết cộng hóa trị với các nguyên tử khác.
- Các số oxi hóa của C là: -4, 0, +2 và +4.
2. Tính chất vật lý
- C có ba dạng thù hình chính: Kim cương, than chì và fuleren.

Hình 2: Một số thù hình của cacbon
+ Kim cương là chất tinh thể trong suốt, không màu, không dẫn điện, dẫn nhiệt kém. Kim cương có cấu trúc tinh thể nguyên tử và cứng nhất trong tất cả các chất.
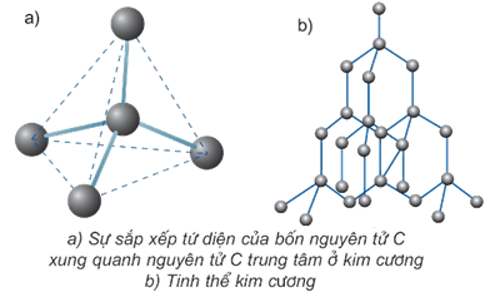
Hình 3: Mô hình cấu trúc tinh thể kim cương
+ Than chì là tinh thể màu xám đen, dẫn điện tốt nhưng kém kim loại. Tinh thể than chì có cấu trúc lớp.
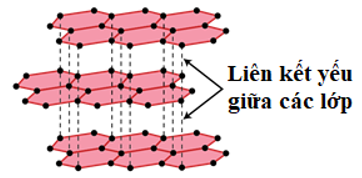
Hình 4: Tinh thể than chì
+ Fuleren gồm các phân tử , , … Phân tử C60 có cấu trúc rỗng, gồm 32 mặt, với 60 đỉnh là 60 nguyên tử C.
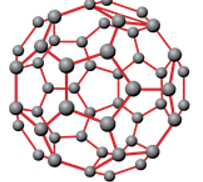
Hình 5: Phân tử fuleren .
- Ngoài ra, các than được điều chế nhân tạo (than gỗ, than xương,…) được gọi là cacbon vô định hình.
II. Tính chất hóa học
- Trong các dạng tồn tại của cacbon, cacbon vô định hình hoạt động hơn cả về mặt hóa học. Tuy nhiên, ở nhiệt độ thường cacbon khá trơ.
- Trong các phản ứng hóa học, cacbon thể hiện hai tính chất: Tính oxi hóa và tính khử. Tuy nhiên tính khử vẫn là chủ yếu của cacbon.
1. Tính khử
a) Tác dụng với oxi
Ở nhiệt độ cao, cacbon lại khử CO2 theo phản ứng:
b) Tác dụng với oxit kim loại
- C khử được oxit của các kim loại đứng sau Al trong dãy hoạt động hóa học của kim loại:
CuO + C Cu + CO
Fe2O3 + 3C 2Fe + 3CO
- Với CaO và A:
CaO + 3C CaC2 + CO (trong lò điện)
2A + 9C A + 6CO
c) Tác dụng với các chất oxi hóa mạnh
- Cacbon tác dụng được với S đặc, HN, KCl, C, ... trong các phản ứng này, C bị oxi hóa đến mức +4 (C).
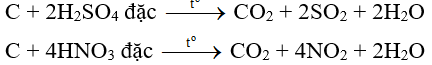
d) Khi nhiệt độ cao, C tác dụng được với hơi nước:
![]()
2. Tính oxi hóa
a) Tác dụng với hiđro
b) Tác dụng với kim loại
(nhôm cacbua)
III. Trạng thái tự nhiên
- Kim cương và than chì là cacbon ở dạng tự do gần như tinh khiết.
- Cacbon còn có trong các khoáng vật như canxit (đá vôi, đá hoa, đá phấn đều chứa CaC), magiezit (MgC), đolomit (CaC.MgC).

Hình 6: Một số khoáng vật chứa cacbon
- Dầu mỏ, khí thiên nhiên là hỗn hợp của các chất khác nhau chứa cacbon.
- Cơ thể động thực vật cũng chứa nhiều hợp chất của cacbon.
IV. Ứng dụng và điều chế
1. Ứng dụng
- Kim cương được dùng làm đồ trang sức. Trong kĩ thuật, kim cương được dùng làm mũi khoan, dao cắt thuỷ tinh, bột mài.

Hình 7: Một số ứng dụng của kim cương
- Than chì được dùng làm điện cực; làm nồi, chén để nấu chảy các hợp kim chịu nhiệt; chế tạo chất bôi trơn; làm bút chì đen.

Hình 8: Một số ứng dụng của than chì
- Than cốc được dùng làm chất khử trong luyện kim để luyện kim loại từ quặng.

Hình 9: Than cốc
- Than gỗ được dùng để chế thuốc nổ đen, thuốc pháo,...

Hình 10: Than gỗ (than củi)
- Than hoạt tính là than có tính hấp phụ mạnh, được dùng trong mặt nạ phòng độc và công nghiệp hóa chất.

Hình 11: Than hoạt tính
- Than muội được dùng làm chất độn khi lưu hoá cao su, để sản xuất mực in, xi đánh giày.

Hình 12: Than muội
2. Điều chế
- Kim cương nhân tạo được điều chế bằng cách nung than chì ở 2000C, áp suất từ 50 đến 100 nghìn atm, xúc tác là Fe, Cr, Ni.
- Than chì nhân tạo được điều chế bằng cách nung than cốc ở 2500 - 3000C trong lò điện, không có không khí.
- Than cốc được điều chế bằng cách nung than mỡ khoảng 1000oC trong lò cốc, không có không khí.
- Than gỗ được tạo nên khi đốt cháy gỗ trong điều kiện thiếu không khí.
- Than mỏ được khai thác trực tiếp từ các vỉa than nằm sâu dưới mặt đất.
- Than muội được tạo nên khi nhiệt phân metan có chất xúc tác:
C C + 2↑