Cho một số phát biểu về đặc điểm chung của các phân tử hợp chất hữu cơ
Các câu đúng là
A. 1, 2, 5, 6
B. 1, 2, 3, 5
C. 1, 2, 3, 7
D. 1, 2, 4, 6
 Giải bởi Vietjack
Giải bởi Vietjack
Đặc điểm chung của các phân tử hợp chất hữu cơ là
Đáp án cần chọn là: C
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Cho các chất: CaC2, CO2, HCOOH, C2H6O, CH3COOH, CH3Cl, NaCl, K2CO3. Số hợp chất hữu cơ trong các chất trên là bao nhiêu?
Tiến hành thí nghiệm theo mô hình sau:
Bông trộn CuSO4 khan chuyển sang màu:
Cho các hợp chất: CaC2, CO2, HCHO, CH3COOH, C2H5OH, NaCN, CaCO3. Số hợp chất hữu cơ trong các hợp chất đã cho là:
Cho các chất: nhôm cacbua (Al4C3), axetilen (C2H2), natri cacbonat (Na2CO3), đường saccarozơ (C12H22O11), PVC ([C2H3Cl]n). Số chất không phải là hợp chất hữu cơ là
Đặc điểm chung của các phân tử hợp chất hữu cơ là
Nhóm các ý đúng là:
Cho thí nghiệm như hình vẽ:
Chọn phát biểu đúng về thí nghiệm trên:
Nung một hợp chất hữu cơ X với lượng dư chất oxi hóa CuO người ta thấy thoát ra khí CO2, hơi H2O và khí N2. Chọn kết luận chính xác nhất trong các kết luận sau:
I. Hợp chất hữu cơ và hóa học hữu cơ
1. Khái niệm
- Hợp chất hữu cơ là các hợp chất của cacbon trừ oxit của cacbon, muối cacbua, muối cacbonat, muối xianua…
- Hoá học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ.
2. Phân loại hợp chất hữu cơ.
- Hợp chất hữu cơ được chia thành hiđrocacbon và dẫn xuất hiđrocacbon.
a/ Hiđrocacbon là loại hợp chất hữu cơ đơn giản nhất, trong thành phần phân tử chỉ chứa hai nguyên tố là cacbon và hiđro. Hiđrocacbon lại được chia thành:
+ Hiđrocacbon no
+ Hiđrocacbon không no
+ Hiđrocacbon thơm.
b/ Dẫn xuất của hiđrocacbon là những hợp chất mà trong phân tử ngoài C, H ra còn có một số hay nhiều nguyên tố khác như O, N, S, halogen...
+ Dẫn xuất halogen: R – X ( R là gốc hiđrocacbon)
+ Hợp chất chứa nhóm chức:
- OH : ancol; - O - : ete; - COOH: axit......
- Ngoài ra, người ta cũng phân loại hợp chất hữu cơ theo mạch cacbon:
+ Hợp chất hữu cơ mạch vòng.
+ Hợp chất hữu cơ mạch hở.
3/ Đặc điểm chung
a) Đặc điểm cấu tạo
- Hợp chất hữu cơ nhất thiết phải chứa C, hay có H thường gặp O ngoài ra còn có halogen, N, P...
- Liên kết chủ yếu trong hợp chất hữu cơ là liên kết cộng hóa trị.
b) Tính chất vật lí
- Các hợp chất hữu cơ thường dễ bay hơi, dễ cháy, kém bền nhiệt.
- Phần lớn các hợp chất hữu cơ không tan trong nước, tan nhiều trong các dung môi hữu cơ.
c) Tính chất hóa học
- Các hợp chất hữu cơ thường kém bền với nhiệt và dễ cháy.
- Các phản ứng trong hoá học hữu cơ thường chậm, không hoàn toàn, xảy ra theo nhiều hướng thường phải đun nóng và có xúc tác.
II. Phân tích nguyên tố
Để xác định công thức phân tử hợp chất hữu cơ người ta phải xác định:
- Thành phần định tính nguyên tố.
- Thành phần định lượng nguyên tố.
1. Phân tích định tính
- Mục đích: Phân tích định tính nguyên tố để xác định thành phần các nguyên tố hóa học chứa trong một chất.
- Nguyên tắc: Muốn xác định thành phần các nguyên tố, người ta chuyển các nguyên tố trong hợp chất hữu cơ thành các hợp chất vô cơ đơn giản rồi nhận biết các sản phẩm đó bằng các phản ứng đặc trưng.
a. Xác định cacbon và hiđro
- Phương pháp: Trong phòng thí nghiệm, để xác định định tính C và H, người ta nung hợp chất hữu cơ với CuO để chuyển C → C, H → O.
+ Xác nhận có H: dùng CuS khan để hấp thụ nước.
+ Xác định có C: dẫn khí C qua dung dịch Ca(OH)2.
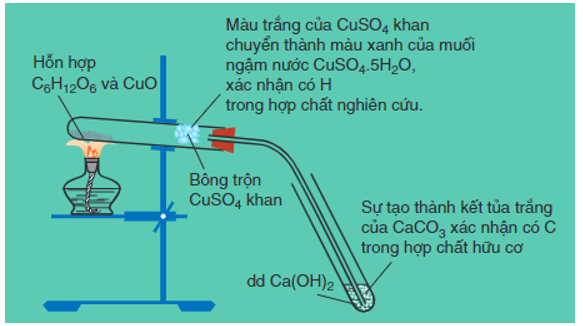
Hình 1: Thí nghiệm xác định định tính C, H có trong glucozơ
b. Xác định nitơ và oxi.
- Xác định N: Đốt cháy hợp chất hữu cơ, nếu có mùi khét thì hợp chất đó có nitơ. Hoặc đun hợp chất hữu cơ với S đặc (NaOH đặc) có mùi khai N thì hợp chất đó có chứa nitơ.
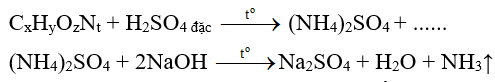
- Xác định O: Khó phân tích định tính trực tiếp, thường xác định nhờ định lượng:
mO = mhợp chất – tổng khối lượng các nguyên tố
c. Xác định halogen.
Khi đốt cháy hợp chất hữu cơ chứa clo bị phân hủy, clo tách ra dưới dạng HCl, ta dùng dung dịch AgNO3 để nhận biết.
HCl + AgN → AgCl↓ + HN
2. Phân tích định lượng các nguyên tố
- Mục đích: Phân tích định lượng các nguyên tố xác định khối lượng của mỗi nguyên tố hóa học chứa trong hợp chất hữu cơ.
- Nguyên tắc: Muốn định lượng nguyên tố, người ta chuyển các nguyên tố trong hợp chất hữu cơ thành các hợp chất vô cơ đơn giản, định lượng chúng, từ đó suy ra thành phần % khối lượng từng nguyên tố.
a. Định lượng cacbon và hiđro
Thí dụ: Đốt cháy chất hữu cơ A thu được C và O và .
b. Định lượng nitơ
c. Định lượng oxi
mO = mA – ( mC + mH + mN ).
3. Thành phần nguyên tố
→ %O = 100% - %C - %H - %N.