Mô hình điều chế khí clo trong phòng thí nghiệm được cho như hình vẽ bên (Hình 1). Quy trình thí nghiệm xảy ra như sau:
Nhỏ từ từ dung dịch (1) xuống bình cầu có chứa chất rắn màu đen (2). Đun nóng hỗn hợp thì thoát ra khí clo (màu vàng lục). Khí clo sinh ra di chuyển theo hệ thống bình (3); (4); (5). Tại bình số (5), khí clo được giữ lại. Để tránh việc clo thoát ra ngoài không khí, người ta tẩm vào (6) dung dịch T. Vậy (6) là:
A. HCl
B. NaOH
C.
D. NaCl
 Giải bởi Vietjack
Giải bởi Vietjack
Để tránh thoát ra ngoài không khí, người ta tẩm NaOH vào (6). Vì Cl2 có phản ứng với NaOH do đó bị giữ lại
PTPƯ
Đáp án: B
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Dung dịch hỗn hợp hai muối natri clorua và natri hipoclorit được gọi là gì?
Có 4 lọ đựng 4 khí riêng biệt: oxi, hiđro, clo và khí cacbonic. Bằng cách nào trong các cách sau đây để phân biệt mỗi khí trên (tiến hành theo trình tự sau):
Có 3 khí đựng riêng biệt trong 3 lọ là oxi, clo, hiđroclorua. Để phân biệt các khí đó có thể dùng một hóa chất là
Cho dung dịch NaOH 1M tác dụng vừa đủ với 1,12 lít khí clo (đktc). Nồng độ mol của muối natri clorua thu được là
Nguyên liệu được dùng để điều chế khí clo trong phòng thí nghiệm là:
Hòa tan hoàn toàn 52,2 gam trong dung dịch HCl đặc, nóng, dư thì sau phản ứng thu được bao nhiêu lít khí (đktc)?
I. Tính chất vật lí
- Clo là chất khí, màu vàng lục, mùi hắc, nặng gấp 2,5 lần không khí
( ) và tan được trong nước.
- Ở 20oC, một thể tích nước hòa tan được 20 thể tích khí clo.
- Tác dụng sinh lí: Clo là một khí độc.

Hình 1: Bình chứa khí clo
II. TÍNH CHẤT HÓA HỌC
1. Clo có những tính chất hóa học của phi kim
a) Tác dụng kim loại → muối clorua
- Clo phản ứng với với hầu hết kim loại tạo thành muối clorua
- Ví dụ:

Hình 2: Sắt tác dụng với clo
b) Tác dụng hiđro → khí hiđro clorua
- Phương trình hóa học:
![]()
- Khí hiđro clorua tan nhiều trong nước tạo thành dung dịch axit clohiđric.
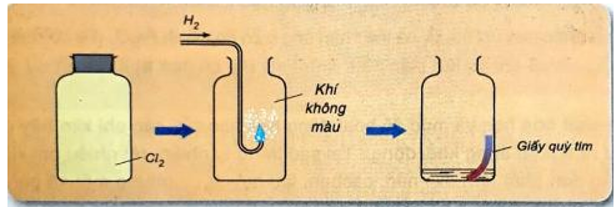
Hình 3: Khí hiđro tác dụng với khí clo.
Chú ý: Clo không phản ứng trực tiếp với oxi.
2. Tính chất hóa học khác của clo
a) Tác dụng với nước
- Phương trình hóa học:
![]()
- Nước clo là dung dịch hỗn hợp các chất , HCl, HClO có màu vàng lục, mùi hắc.
- Khi cho quỳ tím vào nước clo, lúc đầu dung dịch làm quỳ tím hóa đỏ, sau đó nhanh chóng mất màu do tác dụng oxi hóa mạnh của axit hipoclorơ HClO.
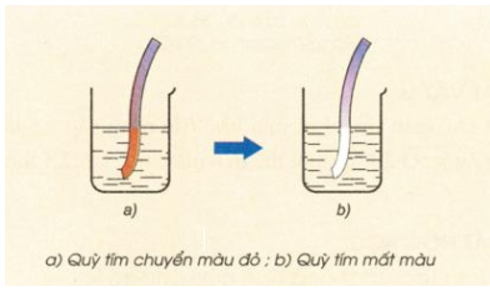
Hình 4: Nhúng giấy quỳ tím vào nước clo
- Nước clo có tính tẩy màu, sát trùng.
b) Tác dụng với dung dịch kiềm (NaOH, KOH, …)
- Khí clo có thể tác dụng với dung dịch kiềm.
Ví dụ:
![]()
- Dung dịch hỗn hợp hai muối natri clorua (NaCl) và natri hipoclorit (NaClO) được gọi là nước Gia - ven. Dung dịch này có tính tẩy màu tương tự nước clo, vì NaClO cũng là chất oxi hóa mạnh tương tự HClO.
III. Ứng dụng của clo
- Nước clo dùng khử trùng nước sinh hoạt.
- Tẩy trắng vải sợi, bột giấy....
- Điều chế nước Gia - ven, clorua vôi...
- Điều chế nhựa PVC, chất dẻo, chất màu...
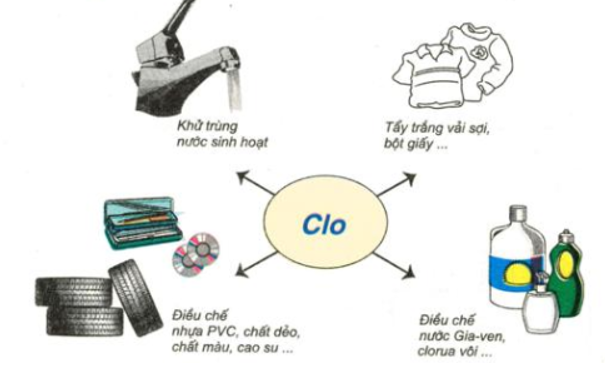
Hình 5: Sơ đồ về một số ứng dụng của khí clo
IV. ĐIỀU CHẾ KHÍ CLO
1. Trong phòng thí nghiệm
- Phương pháp: Đun nóng nhẹ dung dịch HCl đậm đặc với các chất oxi hóa mạnh như MnO2, KMnO4,...
- Ví dụ:
![]()
- Thu khí clo bằng cách đẩy không khí.
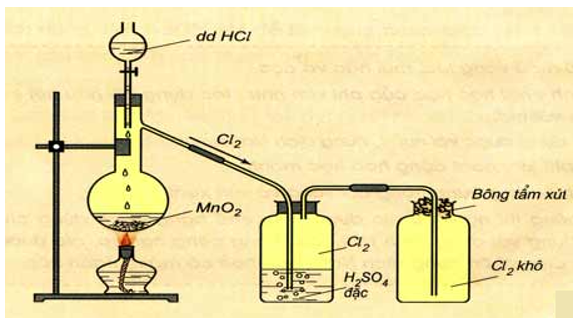
Hình 6: Điều chế clo trong phòng thí nghiệm
2. Trong công nghiệp
Phương pháp: Điện phân dung dịch NaCl bão hòa (có màng ngăn xốp ngăn không cho khí C thoát ra tác dụng với NaOH tạo thành nước Gia-ven)
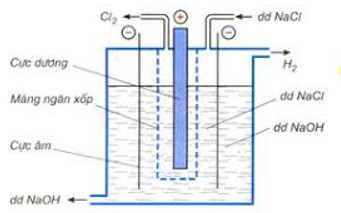
Hình 7: Sơ đồ thùng điện phân dung dịch NaCl