Kim cương và than chì là 2 dạng thù hình của cacbon vì
A. đều có cấu tạo tinh thể như nhau
B. đều do nguyên tố cacbon tạo nên
C. đều có tính chất vật lí tương tự nhau
D. cả A và B đều đúng
 Giải bởi Vietjack
Giải bởi Vietjack
Kim cương và than chì là 2 dạng thù hình của cacbon vì đều do nguyên tố cacbon tạo nên.
Đáp án: B
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Khi mở các chai nước giải khát có ga thấy xuất hiện hiện tượng sủi bọt vì:
Để chứng minh sự có mặt của khí CO và trong hỗn hợp, người ta dẫn hỗn hợp khí qua (1) thấy xuất hiện kết tủa trắng, sau đó dẫn khí còn lại qua (2) thấy có chất rắn màu đỏ xuất hiện. Hoá chất đem sử dụng ở (1), (2) lần lượt là:
Tính nhiệt lượng tỏa ra khi đốt cháy 5 kg than có chứa 90% cacbon. Biết 1 mol cacbon cháy tỏa ra 394 kJ
Cho 1,6 gam hỗn hợp gồm CuO và phản ứng hoàn toàn với bột cacbon ở nhiệt độ cao thu được 0,28 lít khí (đktc). Thành phần % khối lượng từng chất trong hỗn hợp trên là
Trong luyện kim, người ta sử dụng cacbon và hoá chất nào để điều chế kim loại ?
I. Các dạng thù hình của cacbon
- Dạng thù hình của một nguyên tố hóa học là những đơn chất khác nhau do nguyên tố đó tạo nên.
Ví dụ: oxi (), ozon () là hai dạng thù hình của nguyên tố oxi.
- Nguyên tố cacbon có 3 dạng thù hình chính là:
+ Kim cương: cứng, trong suốt, không dẫn điện.
+ Than chì: mềm, dẫn điện.
+ Cacbon vô định hình (than đá, than gỗ, than xương, mồ hóng …): xốp, không dẫn điện.

Hình 1: Các dạng thù hình của cacbon
III. Tính chất của cacbon
1. Tính chất hấp phụ
- Than gỗ có khả năng giữ trên bề mặt của nó các chất khí, chất hơi, chất tan trong dung dịch. Than gỗ có tính hấp phụ.
- Than gỗ, than xương … mới điều chế có tính hấp phụ cao được gọi là than hoạt tính. Than hoạt tính có tính hấp phụ cao được dùng để làm trắng đường, chế tạo mặt nạ phòng độc...
2. Tính chất hóa học
Cacbon có những tính chất hóa học của phi kim. Tuy nhiên cacbon là phi kim hoạt động yếu.
Dưới đây là hai tính chất hóa học có nhiều ứng dụng trong thực tế của cacbon:
a) Tác dụng với oxi tạo thành cacbon đioxit CO2 (C là chất khử)
Phương trình hóa học: C + C
Phản ứng tỏa nhiều nhiệt, do đó C được dùng làm nhiên liệu trong sản xuất và đời sống.

Hình 2: Cacbon cháy trong khí oxi
b) Tác dụng với oxit kim loại tạo thành C và kim loại
Ở nhiệt độ cao, C khử được một số oxit kim loại như PbO, ZnO,...thành kim loại.
Ví dụ:
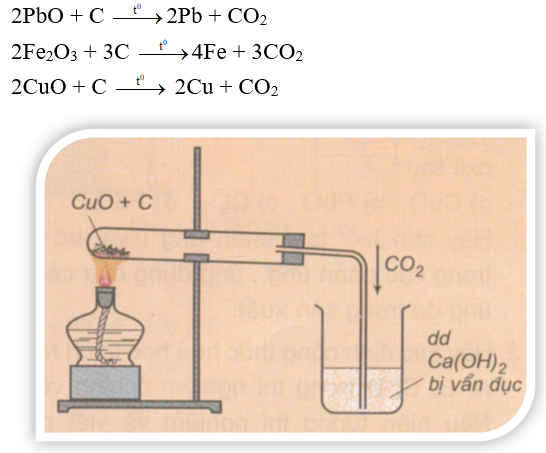
Hình 3: Phản ứng của cacbon với CuO ở nhiệt độ cao
Trong luyện kim người ta sử dụng tính chất này của cacbon để điều chế kim loại.
III. ỨNG DỤNG CỦA CACBON
Tùy thuộc vào tính chất của mỗi dạng thù hình, người ta sử dụng cacbon trong đời sống, sản xuất và trong kĩ thuật.
Ví dụ:
- Than chì được dùng làm điện cực, chất bôi trơn, ruột bút chì…

Hình 4: Một số ứng dụng của than chì
- Kim cương được dùng làm đồ trang sức quý hiếm, mũi khoan, dao cắt kính...

Hình 5: Một số ứng dụng của kim cương
- Cacbon vô định hình dùng làm mặt nạ phòng độc, chất khử mùi…

Hình 6: Một số ứng dụng của cacbon hoạt tính
- Than gỗ, than đá … được dùng làm nhiên liệu (chất đốt) trong công nghiệp, làm chất khử để điều chế một số kim loại.