Giải Hóa 10 Cánh diều Bài 3: Nguyên tố hóa học
Hamchoi.vn trân trọng giới thiệu: lời giải bài tập Hóa lớp 10 Bài 3: Nguyên tố hóa học sách Cánh diều hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa 10 Bài 3. Mời các bạn đón xem:
Giải bài tập Hóa lớp 10 Bài 3: Nguyên tố hóa học
Video giải bài tập Hóa lớp 10 Bài 3: Nguyên tố hóa học
Mở đầu trang 16 Hóa học 10: Những nguyên tử nào dưới đây thuộc cùng một nguyên tố hóa học?
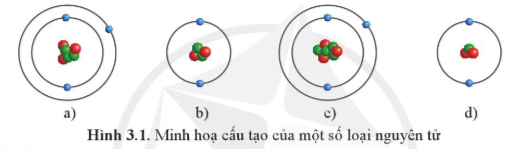
Trả lời:
Các nguyên tử mà hạt nhân có cùng số proton thuộc cùng một nguyên tố hóa học.
⇒ Nguyên tử ở hình a) và c) thuộc cùng một nguyên tố hóa học vì cùng có 3 proton (hạt màu đỏ) trong hạt nhân.
Nguyên tử ở hình b) và d) thuộc cùng một nguyên tố hóa học vì cùng có 2 proton (hạt màu đỏ) trong hạt nhân.
I. Nguyên tố hóa học
1. Khái niệm nguyên tố hóa học
Câu hỏi 1 trang 16 Hóa học 10: Nguyên tử lithium (Li) có 3 proton trong hạt nhân. Khi Li tác dụng với khí chlorine (Cl2) sẽ thu được muối lithium chloride (LiCl), trong đó, Li tồn tại ở dạng ion Li+. Ion Li+ có bao nhiêu proton trong hạt nhân?
Trả lời:
Khi hình thành muối lithium chloride (LiCl) nguyên tử Li cho đi 1 electron ở lớp ngoài cùng trở thành ion mang điện tích dương, kí hiệu là Li+.
Như vậy nguyên tử Li chỉ nhường electron ở lớp vỏ, số proton không thay đổi. Hay ion Li+ có 3 proton trong hạt nhân.
2. Số hiệu nguyên tử, số khối, kí hiệu nguyên tử
Luyện tập 1 trang 17 Hóa học 10: Phân tử S8 có 128 electron, hỏi số hiệu nguyên tử của lưu huỳnh (S) là bao nhiêu?
Trả lời:
Số hiệu nguyên tử = số proton = số electron = .
Luyện tập 2 trang 17 Hóa học 10: Một nguyên tử có Z hạt proton, Z hạt electron và N hạt neutron. Tính khối lượng (gần đúng theo amu) và số khối của nguyên tử này. Nhận xét về kết quả thu được.
Trả lời:
Khối lượng nguyên tử (gần đúng) ≈ khối lượng hạt nhân nguyên tử = Z + N (amu)
Số khối = Z + N
Ta thấy: Khối lượng nguyên tử xấp xỉ bằng số khối.
Câu hỏi 2 trang 17 Hóa học 10: Một loại nguyên tử lithium có 3 proton và 4 neutron. Viết kí hiệu nguyên tử của lithium đó.
Trả lời:
Lithium có:
+ Số hiệu nguyên tử (Z) = số proton = 3.
+ Số khối (A) = 3 + 4 = 7.
Kí hiệu nguyên tử Li là
Luyện tập 3 trang 17 Hóa học 10: Hoàn thành bảng sau:
|
Nguyên tử |
Số p |
Số n |
Kí hiệu nguyên tử |
|
C |
6 |
6 |
? |
|
? |
? |
? |
|
Trả lời:
Chú ý:
+ Số hiệu nguyên tử (Z) = số proton
+ Số neutron = số khối (A) – số proton.
|
Nguyên tử |
Số p |
Số n |
Kí hiệu nguyên tử |
|
C |
6 |
6 |
|
|
Na |
11 |
12 |
|
II. Đồng vị, nguyên tử khối trung bình
1. Đồng vị
Câu hỏi 3 trang 18 Hóa học 10: Cho các nguyên tử sau: . Những nguyên tử nào là đồng vị của nhau?
Trả lời:
Nguyên tử và là đồng vị của nhau vì cùng có 5 proton trong hạt nhân nhưng khác nhau về số neutron (M có 6 neutron còn T có 7 neutron).
Vận dụng 1 trang 18 Hóa học 10: Nguyên tố oxygen có 17 đồng vị, bắt đầu từ kết thúc là . Các đồng vị oxygen có tỉ lệ giữa số hạt neutron (N) và số hiệu nguyên tử thỏa mãn 1 ≤ ≤ 1,25 thì bền vững. Hỏi trong tự nhiên thường gặp những đồng vị nào của oxygen?
Trả lời:
Ta có: 1 ≤ ≤ 1,25
⇔ Z ≤ N ≤ 1,25Z
⇔ Z + Z ≤ N + Z ≤ 1,25Z + Z
⇔ 8 + 8 ≤ A ≤ 1,25.8 + 8
⇔ 16 ≤ A ≤ 18
Vậy trong tự nhiên thường gặp các đồng vị: của oxygen.
Vận dụng 2 trang 18 Hóa học 10: Em hãy tìm hiểu đồng vị nào của oxygen chiếm tỉ lệ lớn nhất trong tự nhiên.
Trả lời:
Trong tự nhiên oxygen có các đồng vị là . Trong đó đồng vị chiếm nhiều nhất trong tự nhiên (khoảng 99,762%).
2. Nguyên tử khối trung bình
Luyện tập 4 trang 18 Hóa học 10: Trong tự nhiên, argon có các đồng vị , , chiếm tương ứng khoảng 99,604%, 0,063% và 0,333% số nguyên tử. Tính nguyên tử khối trung bình của Ar.
Trả lời:
Nguyên tử khối trung bình của argon là:
≈ 39,99
Câu hỏi 4 trang 18 Hóa học 10: Chlorine có hai đồng vị bền là và . Nguyên tử khối trung bình của chlorine là 35,45. Tính tỉ lệ phần trăm số nguyên tử mỗi đồng vị của chlorine trong tự nhiên.
Trả lời:
Đặt phần trăm số nguyên tử của đồng vị là x
Đặt phần trăm số nguyên tử của đồng vị là y
Ta có: x + y = 100 (1)
Nguyên tử khối trung bình của chlorine là:
(2)
Giải hệ (1) và (2) ta được: x = 77,5 và y = 22,5
Vậy phần trăm số nguyên tử của đồng vị là 77,5%
Phần trăm số nguyên tử của đồng vị là 22,5%
Bài tập (trang 20)
Bài 1 trang 20 Hóa học 10: Hoàn thành bảng sau đây:
|
Kí hiệu |
Số hiệu nguyên tử |
Số khối |
Số proton |
Số electron |
Số neutron |
|
|
? |
? |
? |
? |
? |
|
? |
? |
39 |
19 |
? |
? |
|
? |
16 |
? |
? |
? |
20 |
Trả lời:
Chú ý:
+ Số hiệu nguyên tử (Z) = số proton = số electron.
+ Số neutron (N) = số khối (A) – số hiệu nguyên tử (Z)
+ Kí hiệu nguyên tử:
|
Kí hiệu |
Số hiệu nguyên tử |
Số khối |
Số proton |
Số electron |
Số neutron |
|
|
18 |
40 |
18 |
18 |
22 |
|
|
19 |
39 |
19 |
19 |
20 |
|
|
16 |
36 |
16 |
16 |
20 |
Bài 2 trang 20 Hóa học 10: Phát biểu nào sau đây là đúng?
A. Những nguyên tử có cùng số electron thuộc cùng một nguyên tố hóa học.
B. Hai nguyên tử A và B đều có số khối là 14. Vậy hai nguyên tử này thuộc cùng một nguyên tố hóa học.
C. Những nguyên tử có cùng số neutron thì thuộc cùng một nguyên tố hóa học.
Trả lời:
Đáp án đúng là: A
A. Đúng. Những nguyên tử có cùng số proton thì thuộc cùng một nguyên tố hóa học.
Mà nguyên tử trung hòa về điện nên số proton = số electron
Bài 3 trang 20 Hóa học 10: Trong tự nhiên, đồng có hai đồng vị bền là và . Nguyên tử khối trung bình của đồng là 63,54. Tính số mol mỗi loại đồng vị có trong 6,354 gam đồng.
Trả lời:
Đặt phần trăm số nguyên tử của đồng vị là x
Đặt phần trăm số nguyên tử của đồng vị là y
Ta có: x + y = 100 (1)
(2)
Giải hệ (1) và (2) ta được: x = 73 và y = 27
Vậy phần trăm số nguyên tử của đồng vị là 73%
Phần trăm số nguyên tử của đồng vị là 27%
Số mol tương ứng với 6,354 gam đồng là = 0,1 mol
Số mol đồng vị trong 6,354 gam đồng là = 0,073 mol
Số mol đồng vị trong 6,354 gam đồng là = 0,027 mol
Bài 4 trang 20 Hóa học 10: Phổ khối lượng (MS: Mass Spectrum) chủ yếu được sử dụng để xác định phân tử khối, nguyên tử khối của các chất và hàm lượng các đồng vị bền của một nguyên tố. Phổ khối của neon được biểu diễn như ở Hình 3.5.
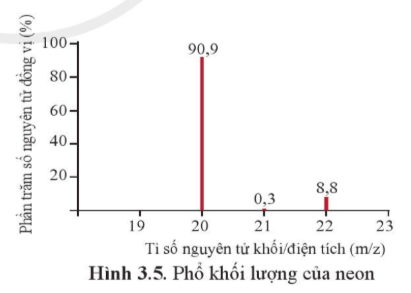
Trục tung biểu thị hàm lượng phần trăm về số nguyên tử của từng đồng vị, trục hoành biểu thị tỉ số của nguyên tử khối (m) của mỗi đồng vị với điện tích của các ion đồng vị tương ứng (điện tích z của các ion đồng vị neon đều bằng +1).
a) Neon có bao nhiêu đồng vị bền?
b) Tính nguyên tử khối trung bình của neon.
Trả lời:
a) Neon có 3 đồng vị bền:
b) Nguyên tử khối trung bình của neon là
= 20,179
Xem thêm lời giải bài tập Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Bài viết liên quan
- Chủ đề 7: Nguyên tố nhóm VIIA (nhóm halogen)
- Giải Hóa 10 Cánh diều Bài 2: Thành phần của nguyên tử
- Giải Hóa 10 Cánh diều Bài 4: Mô hình nguyên tử và orbital nguyên tử
- Giải Hóa 10 Cánh diều Bài 5: Lớp, phân lớp và cấu hình electron
- Giải Hóa 10 Cánh diều Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
