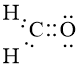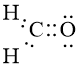Giải Hóa 10 Cánh diều Bài 11: Liên kết cộng hóa trị
Hamchoi.vn trân trọng giới thiệu: lời giải bài tập Hóa lớp 10 Bài 11: Liên kết cộng hóa trị sách Cánh diều hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa 10 Bài 11. Mời các bạn đón xem:
Giải bài tập Hóa lớp 10 Bài 11: Liên kết cộng hóa trị
Video giải bài tập Hóa lớp 10 Bài 11: Liên kết cộng hóa trị
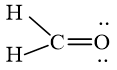
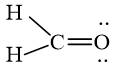
Mở đầu trang 57 Hóa học 10: Công thức của CH2O có thể biểu diễn ở dạng công thức (1) hoặc ở dạng công thức (2). Hãy viết công thức của N2 theo dạng (2) và cho biết công thức này có thể hiện được quy tắc octet không.
|
Phân tử |
Công thức (1) |
Công thức (2) |
|
CH2O |
|
|
|
N2 |
|
? |
Trả lời:
|
Phân tử |
Công thức (1) |
Công thức (2) |
|
CH2O |
|
|
|
N2 |
|
|
Công thức (2) của nguyên tử N có thể hiện được quy tắc octet. Mỗi nguyên tử N trong phân tử N2 có 8 electron lớp ngoài cùng, trong đó có 3 cặp electron chung giữa hai nguyên tử.
I. Liên kết cộng hóa trị
Câu hỏi 1 trang 57 Hóa học 10: Mỗi nguyên tử trong phân tử HF (Hình 11.1) có bao nhiêu electron chung, bao nhiêu electron hóa trị riêng (electron thuộc về một nguyên tử).
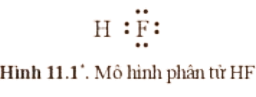
Trả lời:
Trong phân tử HF có 2 electron dùng chung.
Nguyên tử H không có electron hóa trị riêng.
Nguyên tử F có 6 electron hóa trị riêng.
Câu hỏi 2 trang 58 Hóa học 10: Trong phân tử HCl, lớp electron ngoài cùng của Cl và H lần lượt là bao nhiêu electron?
Trả lời:
H có cấu hình electron là 1s1 ⇒ Có 1 electron lớp ngoài cùng.
Cl có cấu hình electron là [Ne]3s23p5 ⇒ Có 7 electron lớp ngoài cùng.
Để đạt được cấu hình electron bền vững của khí hiếm gần nhất, mỗi nguyên tử này đều cần thêm 1 electron. Vì vậy, mỗi nguyên tử H và Cl cùng góp 1 electron chung cho cả hai nguyên tử.
Khi đó trong phân tử HCl, lớp electron ngoài cùng của Cl và H lần lượt là 8 và 2 electron.
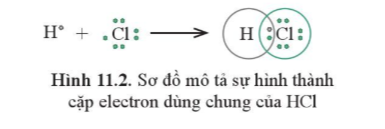
Câu hỏi 3 trang 58 Hóa học 10: Nguyên tử fluorine (F) có cấu hình electron là [He]2s22p5. Khi các nguyên tử F liên kết với nhau, để thỏa mãn quy tắc octet, một bạn học sinh đề xuất như sau: Một nguyên tử F nhường 7 electron, tạo ion F7+ có cấu hình là [He]; 7 nguyên tử F khác, mỗi nguyên tử nhận 1 electron tạo 7 ion F- có cấu hình [Ne]. Sau đó 8 ion này hút nhau tạo thành chất có công thức (F7+)(F-)7. Vì sao đề xuất này không hợp lí trong thực tế? Hãy mô tả hình thành liên kết trong phân tử F2.
Trả lời:
- Mô hình này không hợp lí trong thực tế. Để tạo ion F7+ cần một năng lượng rất lớn so với tạo F-.
- Mô tả hình thành liên kết trong phân tử F2:
Nguyên tử F có cấu hình electron: 1s22s22p5. Để đạt được cấu hình electron của khí hiếm gần nhất, mỗi nguyên tử này đều cần thêm 1 electron. Vì vậy mỗi nguyên tử F cùng góp 1 electron để tạo nên một cặp electron chung cho cả phân tử.
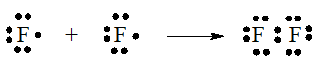
Luyện tập 1 trang 58 Hóa học 10:Hãy biểu diễn sự hình thành các cặp electron chung cho phân tử NH3. Từ đó, viết công thức Lewis của phân tử này.
Trả lời:
Nguyên tử N (Z = 7) có cấu hình electron là 1s22s22p3
Nguyên tử H (Z = 1) có cấu hình electron là 1s1
Để đạt được cấu hình của khí hiếm gần nhất, nguyên tử N cần thêm 3 electron, nguyên tử H cần thêm 1 electron. Vì vậy mỗi nguyên tử H sẽ góp chung 1 electron với nguyên tử N để tạo thành 3 cặp electron chung.
Công thức electron:
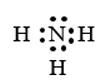
Công thức Lewis:
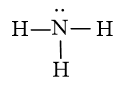
Câu hỏi 4 trang 58 Hóa học 10: Viết công thức Lewis của CO2. Giữa nguyên tử carbon và mỗi nguyên tử oxygen có bao nhiêu cặp electron chung?
Trả lời:
Công thức Lewis của CO2
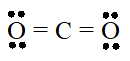
Giữa nguyên tử carbon và mỗi nguyên tử oxygen có 2 cặp electron chung.
Câu hỏi 5 trang 59 Hóa học 10: Mô tả sự hình thành phân tử N2 từ hai nguyên tử N. Phân tử N2 có bao nhiêu cặp electron chung? Viết công thức Lewis của N2.
Trả lời:
Nguyên tử N (Z = 7) có cấu hình electron là: 1s22s22p3
Để đạt được cấu hình của khí hiếm gần nhất, mỗi nguyên tử N đều cần thêm 3 electron. Vì vậy, mỗi nguyên tử N góp chung 3 electron để tạo nên 3 cặp electron chung cho cả hai nguyên tử.
Công thức Lewis của N2
![]()
Câu hỏi 6 trang 59 Hóa học 10: Những nguyên tử nào trong cation ammonium thỏa mãn quy tắc octet?
Trả lời:
Cả nguyên tử N và các nguyên tử H đều thỏa mãn quy tắc octet.
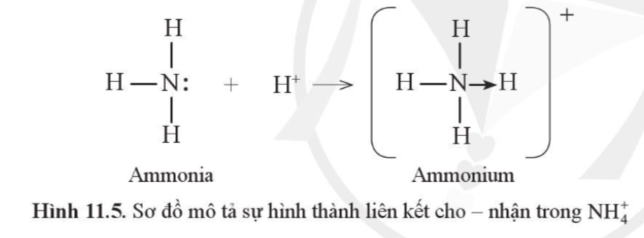
Câu hỏi 7 trang 59 Hóa học 10: Liên kết giữa nguyên tử N trong NH3 với H+ có phải là liên kết ion hay không? Vì sao?
Trả lời:
Chú ý:
- Liên kết ion được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
- Liên kết cho nhận là liên kết mà cặp electron chung được đóng góp từ một nguyên tử (liên kết cho nhận là trường hợp đặc biệt của liên kết cộng hóa trị)
Liên kết giữa nguyên tử N trong NH3 với H+ không phải là liên kết ion vì cặp electron vẫn được dùng chung cho cả nguyên tử N và H chưa bị lệch hoàn toàn về phía nguyên tử nào.
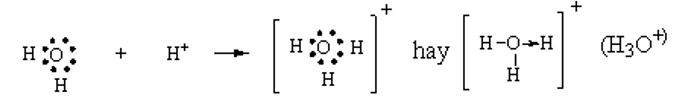
Luyện tập 2 trang 59 Hóa học 10: Trình bày sự hình thành ion hydronium (H3O+) từ H2O và H+.
Trả lời:
Trên nguyên tử O còn 2 cặp electron riêng, khi hình thành H3O+, O sẽ sử dụng 1 cặp electron riêng này trở thành cặp electron chung cho cả O và H, cả O và các H đều thỏa mãn quy tắc octet. Như vậy, liên kết đơn giữa nguyên tử O trong H2O và H+ được tạo thành bởi một cặp electron góp chung của nguyên tử O.
II. Phân loại liên kết theo độ âm điện
Luyện tập 3 trang 60 Hóa học 10: Dựa theo độ âm điện, hãy cho biết loại liên kết trong các phân tử: H2S, CH4, K2O, F2O, NaBr.
Trả lời:
|
Phân tử |
Hiệu độ âm điện (∆χ) |
Loại liên kết |
|
H2S |
χ(S) – χ(H) = 2,58 – 2,20 = 0,38 |
cộng hóa trị không cực |
|
CH4 |
χ(C) – χ(H) = 2,55 – 2,20 = 0,35 |
cộng hóa trị không cực |
|
K2O |
χ(O) – χ(K) = 3,44 – 0,82 = 2,62 |
ion |
|
F2O |
χ(F) – χ(O) = 3,98 – 3,44 = 0,54 |
cộng hóa trị có cực |
|
NaBr |
χ(Br) – χ(Na) = 2,96 – 0,93 = 2,03 |
ion |
III. Liên kết sigma (σ) và liên kết pi (π)
Luyện tập 4 trang 61 Hóa học 10: Viết ô orbital của lớp electron ngoài cùng cho nguyên tử H và F. Từ đó chỉ ra AO nào có thể xen phủ tạo liên kết đơn trong các phân tử H2, F2 và HF.
Trả lời:
Ô orbital lớp ngoài cùng của H (Z = 1) là:
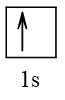
Ô orbital lớp ngoài cùng của F (Z = 9) là:
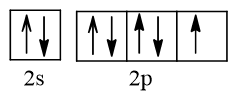
Hai AOs của H xen phủ trục với nhau tạo liên kết đơn trong các phân tử H2
Hai AOp của F xen phủ trục với nhau tạo liên kết đơn trong các phân tử F2
Một AOs của H xen phủ trục với một AOp của F tạo liên kết đơn trong phân tử HF
Luyện tập 5 trang 61 Hóa học 10: Viết ô orbital của lớp ngoài cùng cho nguyên tử N. Từ đó chỉ ra những AO nào có thể xen phủ tạo liên kết ba trong phân tử N2.
Trả lời:
Nguyên tử N (Z = 7) có cấu hình electron là 1s22s22p3
Ô orbital lớp ngoài cùng của N (Z = 7) là:
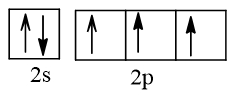
Mỗi nguyên tử N có 3 AOp. Khi hình thành liên kết trong phân tử N2, 2 AO pz xen phủ trục với nhau tạo 1 liên kết σ, 2 AO py xen phủ bên với nhau tạo 1 liên kết π, 2AO px xen phủ bên với nhau tạo 1 liên kết π.
Như vậy hai nguyên tử N liên kết với nhau bằng một liên kết ba tạo phân tử N2 trong đó có 1 liên kết σ và 2 liên kết π.
IV. Năng lượng liên kết cộng hóa trị
Vận dụng trang 62 Hóa học 10: Xây dựng mô hình phân tử
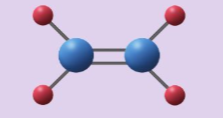
Sử dụng đất sét nặn (hoặc hộp xây dựng mô hình) để tạo hình nguyên tử và các đoạn ống hút để biểu diễn liên kết hóa học. Xây dựng mô hình các phân tử: CH2=CH2, CHCl=CHCl. Biết rằng các nguyên tử đều nằm trên cùng một mặt phẳng
Trả lời:
Học sinh tự thiết kế theo mô hình được minh họa như sau:
Mô hình phân tử CH2=CH2:
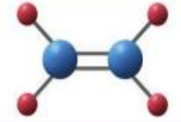
Mô hình phân tử CHCl=CHCl:

Luyện tập 6 trang 62 Hóa học 10: Sắp xếp năng lượng của các loại liên kết: liên kết đơn, liên kết đôi, liên kết ba của cùng một cặp nguyên tố theo chiều tăng dần. Giải thích
Trả lời:
- Chiều tăng dần năng lượng của các loại liên kết của cùng một cặp nguyên tố:
Năng lượng liên kết đơn < năng lượng liên kết đôi < liên kết ba
- Giải thích: Do liên kết đơn chỉ gồm các liên kết sigma, liên kết đôi gồm 1 liên kết sigma và 1 liên kết pi còn liên kết ba gồm 1 liên kết sigma và 2 liên kết pi.
Bài tập (trang 63)
Bài 1 trang 63 Hóa học 10: Những phát biểu nào sau đây là đúng?
(a) Nếu cặp electron dùng chung bị lệch về phía một nguyên tử khi đó là liên kết cộng hóa trị không cực.
(b) Nếu cặp electron dùng chung bị lệch về phía một nguyên tử thì đó là liên kết cộng hóa trị có cực.
(c) Cặp electron dùng chung luôn được tạo nên từ 2 electron của cùng một nguyên tử.
(d) Cặp electron dùng chung được tạo nên từ 2 electron hóa trị.
Trả lời:
Phát biểu đúng là: (b), (d)
(a) Sai vì: Nếu cặp electron chung bị lệch về phía một nguyên tử khi đó là liên kết cộng hóa trị có cực.
(b) Đúng.
(c) Sai vì: Cặp electron chung có thể được tạo nên từ 2 electron của cùng một nguyên tử (liên kết cho nhận) hoặc được tạo nên từ 2 electron của hai nguyên tử khác nhau, trong đó mỗi nguyên tử góp chung 1 electron.
(d) Đúng.
Bài 2 trang 63 Hóa học 10: Những phát biểu nào sau đây là đúng?
(a) Liên kết đôi được tạo nên từ hai liên kết σ.
(b) Liên kết ba được tạo nên từ 2 liên kết σ và 1 liên kết π.
(c) Liên kết đôi được tạo nên từ 1 liên kết σ và 1 liên kết π.
(d) Liên kết ba được tạo nên từ 1 liên kết σ và 2 liên kết π.
Trả lời:
Phát biểu đúng: (c), (d)
Liên kết đôi được tạo nên từ 1 liên kết σ và 1 liên kết π.
Liên kết ba được tạo nên từ 1 liên kết σ và 2 liên kết π.
Bài 3 trang 63 Hóa học 10: Viết công thức Lewis cho các phân tử H2O và CH4. Mỗi phân tử này có bao nhiêu cặp electron hóa trị riêng?
Trả lời:
Công thức Lewis của H2O:
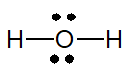
Phân tử H2O có 2 cặp electron hóa trị riêng.
Công thức Lewis của CH4
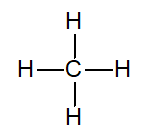
Phân tử CH4 không có cặp electron hóa trị riêng.
Bài 4 trang 63 Hóa học 10: Sử dụng bảng giá trị năng lượng liên kết ở phụ lục 2:
a) Hãy tính tổng năng lượng liên kết trong mỗi phân tử H2S và H2O.
b) Nhiệt độ để bắt đầu phá vỡ liên kết (nhiệt độ phân hủy) mỗi chất trong hai chất trên ứng với một trong hai nhiệt độ sau: 400oC hoặc 1 000oC. Em hãy dự đoán nhiệt độ phân hủy của chất nào cao hơn. Vì sao?
Trả lời:
a)
- Công thức phân tử của H2S là H-S-H
⇒ Phân tử H2S gồm hai liên kết S-H.
Tổng năng lượng liên kết trong phân tử H2S là: 2.368 = 736 kJ mol-1
- Công thức phân tử của H2O là H-O-H
⇒ Phân tử H2O gồm hai liên kết O-H
Tổng năng lượng liên kết trong phân tử H2O là: 2.464 = 928 kJ mol-1
b) Năng lượng liên kết trong phân tử H2O lớn hơn H2S (928 kJ mol-1 > 736 kJ mol-1)
⇒ Nhiệt độ để bắt đầu phá vỡ liên kết (nhiệt độ phân hủy) H2O lớn hơn H2S
⇒ Nhiệt độ phân hủy của H2O là 1000oC, của H2S là 400oC
Bài 5* trang 63 Hóa học 10: Khi phản ứng với H2, các phân tử như F2, N2 cần phải phá vỡ liên kết giữa các nguyên tử. Dựa vào năng lượng liên kết, em hãy dự đoán phản ứng của F2 hay của N2 với H2 sẽ thuận lợi hơn (dễ xảy ra hơn)?
Trả lời:
Năng lượng liên kết F-F là 159 kJ mol-1
Năng lượng liên kết N≡N là 946 kJ mol-1
⇒ Năng lượng cần để phá vỡ liên kết N≡N lớn hơn năng lượng cần để phá vỡ liên kết
F-F
⇒ Phản ứng của F2 với H2 sẽ thuận lợi hơn.
Xem thêm lời giải bài tập Hóa học lớp 10 Cánh diều hay, chi tiết khác: