b. Cho từ từ đến dư dung dịch Ba(OH)2 vào dung dịch Al2(SO4)3.
 Giải bởi Vietjack
Giải bởi Vietjack
b. Hiện tượng: Xuất hiện kết tủa trắng sau đó kết tủa tan dần một phần.
Phương trình hóa học:
3Ba(OH)2 + Al2(SO4)3 → 3BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Nung nóng 20 gam một mẩu quặng malachit có thành phần chính là Cu(OH)2.CuCO3 (còn lại là tạp chất trơ) trong không khí. Hòa tan toàn bộ lượng CuO thu được bằng dung dịch H2SO4 20% vừa đủ, sau đó làm lạnh dung dịch đến 10oC thì có 24,6 gam tinh thể CuSO4.5H2O tách ra. Biết các phản ứng đều xảy ra hoàn toàn và độ tan của CuSO4 ở 10oC là 17,4 gam. Tính hàm lượng phần trăm của Cu(OH)2.CuCO3 có trong mẩu quặng.
Giải thích các trường hợp sau và viết phương trình hóa học của các phản ứng xảy ra (nếu có):
a. Than hoạt tính được dùng làm mặt nạ phòng độc, làm chất khử màu, khử mùi, …
Hỗn hợp X gồm metan, etilen và axetilen. Đốt cháy hoàn toàn 9,6 gam X bằng lượng oxi vừa đủ, thu được hỗn hợp Y. Dẫn toàn bộ Y vào bình đựng dung dịch NaOH, thu được dung dịch chỉ chứa 74,2 gam Na2CO3. Khi sục từ từ 11,2 lít X vào dung dịch brom dư thì có tối đa 100 gam brom phản ứng. Tính phần trăm thể tích của các chất trong X.
Đốt nóng m gam bột Fe trong không khí, thu được hỗn hợp A gồm ba oxit. Hòa tan hoàn toàn A bằng dung dịch HCl, thu được dung dịch D chỉ chứa hai muối. Cho lượng dư dung dịch AgNO3 vào D, sau khi các phản ứng xảy ra hoàn toàn, thu được 20,46 gam chất rắn E. Mặt khác, dung dịch D có khả năng hòa tan tối đa 0,64 gam Cu. Tính giá trị m.
c. Cho canxi cacbua vào nước có pha sẵn vài giọt phenolphtalein, thu được dung dịch màu hồng và thấy sủi bọt khí.
b. Khí hiđro được sử dụng làm nhiên liệu thay thế cho than đá, dầu mỏ, khí thiên nhiên, …
Đốt cháy 11,075 gam trieste T trong không khí, rồi hấp thụ toàn bộ sản phẩm cháy vào bình đựng dung dịch nước vôi trong dư, thu được 71,25 gam kết tủa, đồng thời khối lượng dung dịch giảm 27,975 gam so với ban đầu. Mặt khác, đun nóng 26,58 gam T với 17,1 ml dung dịch NaOH 20% (có khối lượng riêng bằng 1,2 g/ml), thu được glixerol và m gam hỗn hợp muối của axit béo. Biết các phản ứng đều xảy ra hoàn toàn và số mol NaOH dùng dư a% so với lượng phản ứng. Tính giá trị của m và a.
Hỗn hợp E gồm Al, FexOy và CuO, trong đó tỉ lệ khối lượng của FexOy và CuO tương ứng là 29:35. Nung nóng m gam E trong bình kín (không có không khí), thu được hỗn hợp Z. Cho toàn bộ Z tác dụng với lượng dư dung dịch NaOH, thu được 0,336 lít khí H2 và còn lại 3,92 gam hỗn hợp rắn T. Hòa tan 3,92 gam T bằng lượng dư dung dịch H2SO4 đặc, nóng, thu được V lít khí SO2 (sản phẩm khử duy nhất). Hấp thụ toàn bộ V lít khí SO2 vào 120 ml dung dịch Ba(OH)2 0,5M thu được 8,68 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Xác định công thức FexOy và tính phần trăm khối lượng của Al có trong E.
Nêu hiện tượng quan sát được và viết các phương trình hóa học của các phản ứng xảy ra (nếu có) khi tiến hành các thí nghiệm sau:
a. Cho một ít bột Mg vào dung dịch KHSO4.
Thủy phân 270 gam tinh bột bằng dung dịch H2SO4 loãng, đun nóng (hiệu suất phản ứng là 72%), thu được dung dịch X. Trung hòa toàn bộ X bằng dung dịch NaHCO3 vừa đủ, thu được dung dịch Y. Thực hiện phản ứng lên men toàn bộ Y với hiệu suất 75%, thu được V ml dung dịch rượu etylic 40o. Biết khối lượng riêng của rượu etylic nguyên chất là 0,8 g/ml. Nếu đem toàn bộ lượng rượu này lên men giấm với hiệu suất H% thì thu được 1,5 lít dung dịch Z (giả sử chỉ xảy ra phản ứng lên men giấm). Để trung hòa 10 ml dung dịch Z, cần vừa đủ 14,4 ml dung dịch NaOH 0,5M. Tính giá trị của V và H.
Hình vẽ sau mô tả thí nghiệm điều chế và thu khí clo trong phòng thí nghiệm.
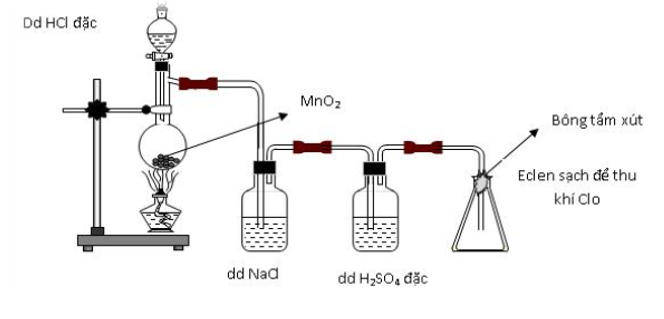
a. Nêu vai trò của bình chứa dung dịch H2SO4 đặc và bông tẩm dung dịch NaOH. Viết các phương trình hóa học của các phản ứng đã xảy ra.
d. Cho bột NaHCO3 vào cốc thủy tinh đựng dung dịch CH3COOH. Nghiêng miệng cốc về phía ngọn nến nhỏ đang cháy thì ngọn nến bị tắt.
d. Đốt cháy rượu etylic, dùng ống nghiệm úp phía trên ngọn lửa. Sau đó, rót nước vôi trong vào ống nghiệm, lắc nhẹ.
c. Đun nóng ống nghiệm chứa nước ép quả nho chín và dung dịch bạc nitrat trong amoniac.
Xác định các chất X1, X2, X3, X4 và viết các phương trình hóa học (ghi rõ điều kiện xảy ra, nếu có) của các phản ứng theo sơ đồ sau: