Vùng xen phủ giữa các orbital càng lớn thì
A. liên kết càng bền.
B. liên kết càng kém bền.
C. liên kết tạo thành thường là liên kết s.
D. liên kết tạo thành thường là liên kết p.
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là: A
Vùng xen phủ giữa các orbital càng lớn thì liên kết càng bền.
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Các liên kết trong phân tử nitrogen (N2) được tạo thành là do sự xen phủ của
Liên kết sigma (s) là loại liên kết cộng hóa trị được hình thành do
Liên kết cộng hóa trị được hình thành từ cặp electron dùng chung. Để tạo nên một cặp electron chung,
Trong phân tử: CHCl=CHCl, số liên kết s và liên kết p lần lượt là
Khi hình thành phân tử giữa hai nguyên tử, vị trí của các AO như sau:
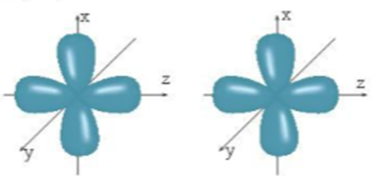
Sự xen phủ giữa hai orbital p trong trường hợp nào sẽ tạo thành liên kết s? Trong trường hợp nào sẽ tạo thành liên kết p?