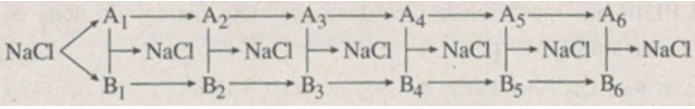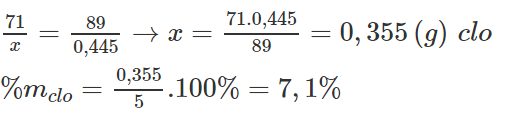Giải SBT Bài 21: Khái quát về nhóm halogen
-
2874 lượt thi
-
11 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Những nguyên tố ở nhóm nào sau đây có cấu hình electron lớp ngoài cùng là ns2np5
 Xem đáp án
Xem đáp án
Đáp án D
Câu 3:
Đặc điểm nào dưới đây là đặc điểm chung của các nguyên tố halogen (F, Cl, Br, I)
 Xem đáp án
Xem đáp án
Đáp án B
Câu 4:
Tính chất nào sau đây không phải là tính chất chung của các nguyên tử halogen
 Xem đáp án
Xem đáp án
Đáp án C
Câu 5:
Trong các phản ứng hóa học, để chuyển thành anion, nguyên tử của các nguyên tố halogen đã nhận hay nhường bao nhiêu electron
 Xem đáp án
Xem đáp án
Đáp án A
Câu 6:
Xác định các chất trong sơ đồ chuyển hoá sau :
 Xem đáp án
Xem đáp án
A1, B1 là Na, Cl2
A2, B2 là Na2O, HCl
A3, B3 là NaOH, CaCl2
A4, B4 là Na2CO3, ZnCl2
A5, B5 là Na3PO4, MgCl2
A6, B6 là Na2SO4, BaCl2
Câu 7:
Một nguyên tố halogen có cấu hình electron lớp ngoài cùng của nguyên tử là 4s24p5
a) Viết cấu hình electron đầy đủ của nguyên tử nguyên tố đó.
b) Cho biết tên, kí hiệu hoá học và cấu tạo phân tử của đơn chất halogen này.
c) Nêu tính hoá học cơ bản của nguyên tố trên.
d) So sánh tính chất hoá học của nguyên tố này với 2 nguyên tố halogen khác đứng trên và dưới nó trong nhóm halogen.
 Xem đáp án
Xem đáp án
a) 1s22s22p63s23p64s24p5
b) Đó là brom, kí hiệu hoá học là Br, phân tử gồm 2 nguyên tử liên kết với nhau bằng 1 liên kết cộng hoá trị.
c) Tính chất hoá học cơ bản là tính oxi hoá mạnh.
d) Brom có tính oxi hoầ yếu hơn clo nhưng mạnh hơn iot.
Cl2 + 2NaBr → 2NaCl + Br2
Br2 + 2NaI → 2NaBr + I2
Câu 8:
Viết PTHH của các phản ứng xảy ra khi cho clo và iot lần lượt tác dụng với dung dịch KOH ở nhiệt độ thường. Giải thích vì sao có sự khác nhau ở 2 phản ứng đó
 Xem đáp án
Xem đáp án
Cl2 + 2KOH → KCl + KClO + H2O
3I2 + 6KOH → 5KI + KIO3 + 3H2O
Trong môi trường kiềm, ion XO- phân huỷ theo phản ứng sau :
3XO- → 2X- + XO3- (kí hiệu X là halogen)
Ion ClO- phân huỷ rất chậm ở nhiệt độ thường, phân huỷ nhanh ở nhiệt độ trên 75°C
Ion IO- phân huỷ ở tất cả các nhiệt độ trên, do đó ở nhiệt độ thường, ta có 2 phản ứng trên.
Câu 9:
Cho 5 gam brom có lẫn tạp chất là clo vào một dung dịch chứa 1,600 gam KBr. Sau phản ứng làm bay hơi dung dịch thì thu được 1,155 gam chất rắn khan. Xác định % về khối lượng của clo trong 5 gam brom đem phản ứng.
 Xem đáp án
Xem đáp án
Khi cho 5g Br2 có lẫn Cl2 phản ứng với KBr thì khối lượng muối giảm là :
1,600 - 1,155 = 0,445 (g)
Cl2 + 2KBr → 2KCl + Br2
Lý thuyết 71 g 238 g 149 g khối lượng muối giảm đi 238 – 149 = 89 g
Thực tế: x g 0,445 g khối lượng muối giảm
Ta có:
Câu 10:
Khi cho 20m3 không khí có chứa khí clo đi qua một ống đựng muối KBr, khối lượng của muối đó giảm bớt 178 mg. Xác-định làm lượng của khí clo (mg/m3) trong không khí.
 Xem đáp án
Xem đáp án
Cl2 + 2KBr → 2KCl + Br2
1 mol 238 g 149 g 1 mol; khối lượng muối giảm 89 g
x mol
0,178g
x = 0,178/89 = 0,002 mol
Lượng khí clo có trong 20m3 không khí là :
71.0,002 = 0,142 (g) = 142 mg
Hàm lượng của khí clo trong không khí là: 142/20 = 7,1 (mg/m3)
Câu 11:
Có 2 khí không màu, dễ tan trong nước, dung dịch thu được cho tác dụng với dung dịch AgNO3 tạo ra kết tủa màu vàng
a) Cho biết tên 2 khí đó.
b) Hãy phân biệt 2 khí đó bằng phương pháp hoá học.
 Xem đáp án
Xem đáp án
a) Hai khí đó là HBr và HI
HBr + AgNO3 → AgBr + HNO3
HI + AgNO3 → AgI + HNO3
b) Dẫn từng khí đó đi qua nước clo có pha sẵn hồ tinh bột, chất nào tạo ra chất mới có màu xanh là HI.
Cl2 + HI → 2HCl + I2