Điện phân 200 ml dung dịch hỗn hợp Cu(NO3)2 xM, NaCl yM (điện cực trơ, màng ngăn) đến khi nước bắt đầu điện phân ở cả 2 điện cực thì dừng lại. Dung dịch sau điện phân có khối lượng giảm 14 gam so với dung dịch ban đầu và dung dịch này phản ứng tối đa 6,72 gam NaHCO3. Biết thời gian điện phân là 19300 giây. Giá trị x, y và cường độ dòng điện (Ampere) lần lượt là:
 Giải bởi Vietjack
Giải bởi Vietjack
nCu(NO3)2 = 0,2x; nNaCl = 0,2y; nNaHCO3 = 0,08
TH1: Chất phản ứng với NaHCO3 là H+ (0,08)
Catot: nCu = 0,2x
Anot: nCl2 = 0,1y và nO2 = nH+/4 = 0,02
Bảo toàn electron: 2.0,2x = 2.0,1y + 0,02.4
m giảm = 0,2x.64 + 0,1y.71 + 0,02.32 = 14
→ x = 0,6; y = 0,8
ne = 2.0,2x = It/F → I = 1,2A
TH2: Chất phản ứng với NaHCO3 là OH- (0,08)
Catot: nCu = 0,2x; nH2 = nOH-/2 = 0,04
Anot: nCl2 = 0,1y
Bảo toàn electron: 2.0,2x + 0,04.2 = 2.0,1y
m giảm = 0,2x.64 + 0,1y.71 + 0,04.2 = 14
→ x = 0,4104; y = 1,2207
ne = 2.0,1x = It/F → I = 1,2207A
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Khí Biogas là loại khí sinh học, thành phần chính gồm hỗn hợp khí metan (CH4 chiếm khoảng 50% - 60%), CO2 (>30%) và một số chất khác được phát sinh từ sự phân hủy hợp chất hữu cơ như hơi nước, N2, O2, H2S, CO. Muốn nâng nhiệt độ của 1 gam nước lên 1°C cần tiêu tốn 4,18 J và khi 1,00 gam metan cháy, nhiệt tỏa ra là 55,6 kJ. Thể tích tối thiểu khí biogas (lít) cần dùng để đun 2,5 lít nước (D = 1,00 g/ml) từ 25°C lên 100°C gần nhất với giá trị nào sau đây? (Giả sử có 65% lượng nhiệt sinh ra khi đốt cháy biogas được sử dụng để tăng nhiệt độ của nước)
Thủy phân hoàn toàn 7,4 gam este đơn chức X bằng dung dịch NaOH dư, đun nóng, thu được 8,2 gam muối Y và m gam ancol Z. Giá trị của m là
Cho sơ đồ chuyển hóa:
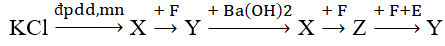
Biết: X, Y, Z, E, F là các hợp chất khác nhau, mỗi mũi tên ứng với một phương trình hóa học. Các chất Y, Z thỏa mãn sơ đồ trên lần lượt là
Hoà tan hết 14,6 gam hỗn hợp X gồm kim loại R (chỉ có hoá trị II) và oxit của kim loại R cần vừa đủ 400ml dung dịch HCl 1M, sau phản ứng hoàn toàn thu được 2,24 lít khí ở đktc. Kim loại R là
Hỗn hợp T gồm hai triglixerit X và Y có tỉ lệ mol tương ứng là 2 : 3. Tiến hành các thí nghiệm sau:
• Thí nghiệm 1: Xà phòng hóa hoàn toàn T bằng dung dịch NaOH dư, thu được hỗn hợp muối gồm C15H31COONa, C17H31COONa và C17H33COONa.
• Thí nghiệm 2: Đốt cháy hoàn toàn m gam T, thu được 5,3 mol CO2 và 4,96 mol H2O.
• Thí nghiệm 3: Cho m gam T tác dụng với H2 dư (xúc tác Ni, t°) thì số mol H2 phản ứng tối đa là 0,14 mol. Phần phần trăm khối lượng của X trong m gam T là
Phân bón đa yếu tố NPK 4.12.7 (kí hiệu này cho biết tỉ lệ khối lượng N, P2O5, K2O trong phân) thân thiện với môi trường, quá trình tan trong nước không tự phân hủy sinh khí độc, sử dụng rất an toàn cho người, động vật và thực vật. Nếu chúng ta có 3 mẫu phân bón (NH4)2SO4, Ca(H2PO4)2 và KCl, đem trộn chúng lần lượt theo tỉ lệ khối lượng gần đúng nào để có loại phân bón NPK 4.12.7 nêu trên? (Xem phần trăm tạp chất trong phân không đáng kể.)
Chất hữu cơ E có công thức đơn giản nhất là CHO; chất hữu cơ F có cùng số nguyên tử cacbon với E. Tổng số nguyên tử trong E và F là 27. Khi cho 1 mol E hoặc 1 mol F tác dụng hết với Na dư đều thu được 1 mol khí H2. Từ E và F thực hiện các phản ứng sau:
(1) E + 2NaOH (t°) → X + 2H2O
(2) F + 2NaOH (t°) → 2Y + H2O
(3) Y + HCl → NaCl + T
Trong đó các chất X, Y, Z, T là các hợp chất hữu cơ. Cho các phát biểu sau:
(a) Chất E là axit cacboxylic và có hai đồng phân cấu tạo.
(b) F là hợp chất no, mạch hở.
(c) Phân tử chất F có chứa 3 loại nhóm chức.
(d) Đốt cháy hoàn toàn a mol E hoặc a mol X đều cho kết quả nCO2 - nH2O = 2a
(e) Trong công nghiệp, chất T điều chế trực tiếp từ metanol.
(g) Chất E cộng hợp Br2 trong CCl4 theo tỉ lệ mol 1 : 1.
Số phát biểu đúng là
Cho các phát biểu sau:
(a) Dầu ăn và mỡ động vật có chứa nhiều triglixerit.
(b) Các polime thuộc loại tơ tổng hợp đều điều chế từ phản ứng trùng ngưng.
(c) Chất béo nhẹ hơn nước và không tan trong nước.
(d) Nhỏ dung dịch iot vào vết cắt quả chuối xanh, xuất hiện màu xanh tím.
(e) Trong phân tử peptit mạch hở Gly-Ala-Glu có 4 nguyên tử oxi.
Số phát biểu đúng là
Cho x mol axit glutamic tác dụng vừa đủ với dung dịch HBr 1,0 M, thu được dung dịch X. Dung dịch X tác dụng vừa đủ với dung dịch chứa y mol KOH. Biểu thức liên hệ giữa x và y là
Thực hiện các thí nghiệm sau:
(a) Đun sôi nước có tính cứng vĩnh cửu.
(b) Hòa tan phèn chua vào nước rồi thêm dung dịch NH3 dư.
(c) Cho dung dịch H2SO4 dư vào dung dịch Ba(AlO2)2.
(d) Cho mẩu nhỏ Na vào dung dịch gồm CaCl2 và NaHCO3.
(e) Cho nước vôi trong vào dung dịch KHCO3.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được có kết tủa là
Cho các phát biểu sau:
(a) Khi cho dung dịch KOH vào dung dịch K2Cr2O7 thì dung dịch chuyển từ màu da cam sang màu vàng.
(b) Khi cho dung dịch NaOH dư vào dung dịch Ba(HCO3)2 thu được kết tủa.
(c) Ở nhiệt độ cao, tất cả kim loại kiềm thổ đều tác dụng với nước.
(d) Khi cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư thu được dung dịch chứa hai muối.
(e) Hỗn hợp gồm Al, Al2O3, Al(OH)3 không tan được hết trong dung dịch NaOH dư.
Số phát biểu đúng là
Cho 3,48 gam hỗn hợp gồm Fe2O3, K2O tác dụng vừa đủ với 200ml dung dịch H2SO4 0,25M. Sau phản ứng thu được dung dịch chứa m gam hỗn hợp muối. Giá trị của m là
Nhúng thanh sắt lần lượt vào các dung dịch sau: CuSO4, AgNO3 dư, ZnSO4, Fe2(SO4)3, HCl, HNO3 loãng dư. Biết các thí nghiệm không tiếp xúc với không khí. Số trường hợp xảy ra phản ứng tạo hợp chất sắt (II) là