30 đề thi THPT Quốc gia môn Hóa năm 2022 có lời giải (Đề số 1)
-
45338 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Kim loại nào sau đây có khối lượng riêng nhỏ nhất (nhẹ nhất)?
 Xem đáp án
Xem đáp án
Cần nắm một số tính chất vật lý riêng của một số kim loại:
- Nhẹ nhất: Li (0,5g/cm3)
- Nặng nhất Os (22,6g/cm3).
- Nhiệt độ nc thấp nhất: Hg (−390C)
- Nhiệt độ cao nhất W (34100C).
- Kim loại mềm nhất là Cs (K, Rb) (dùng dao cắt được)
- Kim loại cứng nhất là Cr (có thể cắt được kính).
Đáp án B.
Câu 2:
Kim loại nào sau đây tác dụng với dung dịch FeCl3 nhưng không tác dụng với dung dịch HCl?
 Xem đáp án
Xem đáp án
Nhớ tính chất dãy hoạt động hóa học
K+ Na+ Mg2+ Al3+ Zn2+ Fe2+ Ni2+ Sn2+ Pb2+ H+ Cu2+ Fe3+ Ag+ Hg2+ Pt2+ Au3+
Tính oxi hóa tăng dần
K Na Mg Al Zn Fe Ni Sn Pb H2 Cu Fe2+ Ag Hg Pt Au
Tính khử giảm dần
Đáp án C.
Câu 3:
Ở trạng thái cơ bản, cấu hình electron của nguyên tử Na (Z = 11) là
 Xem đáp án
Xem đáp án
Nắm cách viết cấu hình theo mức năng lượng: 1s 2s 2p 3s 3p 4s,...
Đáp án D.
Câu 4:
Kim loại phản ứng được với H2SO4 loãng là
 Xem đáp án
Xem đáp án
Nhớ tính chất dãy hoạt động hóa học: kim loại tác dụng với H2SO4 loãng phải đứng trước H
K Na Mg Al Zn Fe Ni Sn Pb H2 Cu Fe2+ Ag Hg Pt Au
Đáp án D
Câu 5:
Trong số các kim loại Na, Mg, Al, Fe, kim loại có tính khử mạnh nhất là
 Xem đáp án
Xem đáp án
K Na Mg Al Zn Fe Ni Sn Pb H2 Cu Fe2+ Ag Hg Pt Au
Tính khử giảm dần
Đáp án D.
Câu 6:
Có thể điều chế Cu bằng cách dùng H2 để khử
 Xem đáp án
Xem đáp án
Phương pháp nhiệt luyện: Dùng chất khử (CO, H2; C; Al) để khử ion kim loại trong các oxit.
Đáp án B.
Câu 7:
Kim loại Al không tan trong dung dịch nào sau đây?
 Xem đáp án
Xem đáp án
Al, Fe, Cr bị thụ động hóa trong HNO3 và H2SO4 đặc nguội
Đáp án D.
Câu 8:
Canxi cacbonat được dùng sản xuất vôi, thủy tinh, xi măng. Công thức của canxi cacbonat là
 Xem đáp án
Xem đáp án
Lưu ý một số tên gọi của hợp chất quan trọng canxi: đá vôi (CaCO3), vôi sống (CaO), dung dịch nước vôi trong (Ca(OH)2),...
Đáp án C.
Câu 9:
Bột nhôm trộn với bột sắt oxit (hỗn hợp tecmit) để thực hiện phản ứng nhiệt nhôm dùng
 Xem đáp án
Xem đáp án
Xem phần ứng dụng của nhôm trong skg 12
Đáp án D.
Câu 10:
Sắt có số oxi hoá +3 trong hợp chất nào sau đây?
 Xem đáp án
Xem đáp án
Dễ dàng xác định được số oxi hóa của sắt trong hợp chất là +3
Đáp án C.
Câu 12:
X là chất khí gây ra hiệu ứng nhà kính. X tham gia vào quá trình quang hợp của cây xanh tạo tinh bột. Chất X là
 Xem đáp án
Xem đáp án
CO2 và CH4 là những tác nhân gây hiệu ứng nhà kính
Đáp án D.
Câu 13:
Thủy phân este CH3CH2COOCH3 thu được ancol có công thức là
 Xem đáp án
Xem đáp án
CH3CH2COOCH3 (RCOOR’) gốc ancol là gốc R’ (CH3-) nên tạo ancol là CH3OH
Đáp án C
Câu 14:
Thủy phân triolein trong dung dịch NaOH, thu được glixerol và muối X. Công thức của X là
 Xem đáp án
Xem đáp án
Nhớ các gốc của các axit béo:
(C15H31COO)3C3H5: (806) tripanmitin
(C17H35COO)3C3H5 (890) tristearin.
(C17H33COO)3C3H5: (884) triolein.
Đáp án A.
Câu 15:
Số nguyên tử cacbon trong phân tử saccarozơ là
 Xem đáp án
Xem đáp án
Cần nắm một số CTPT các cacbohiđrat: glucozơ, fructozơ (C6H12O6), saccarozơ (C12H22O11),...
Đáp án C.
Câu 16:
Chất nào dưới đây cho phản ứng tráng bạc?
 Xem đáp án
Xem đáp án
Các chất có dạng HCOOR’ sẽ tham gia phản ứng tráng bạc
Đáp án C.
Câu 17:
Chất nào dưới đây tạo phức màu tím với Cu(OH)2?
 Xem đáp án
Xem đáp án
Đa số peptit có khả năng tạo được dung dịch phức màu tím với Cu(OH)2 (trừ đipeptit)
Đáp án C.
Câu 18:
Polietilen (PE) được điều chế từ phản ứng trùng hợp chất nào sau đây?
 Xem đáp án
Xem đáp án
Xem bảng gọi tên polime từ skg 12
Đáp án A.
Câu 19:
Muối nào sau đây dễ bị nhiệt phân khi đun nóng?
 Xem đáp án
Xem đáp án
Các muối cacbonat, hiđrocacbonat dễ bị nhiệt phân (trừ muối cacbonat của kim loại kiềm ví dụ Na2CO3, K2CO3,...)
Đáp án D.
Câu 20:
Công thức của anđehit axetic là
 Xem đáp án
Xem đáp án
Nắm một số tên của hợp chất hữu cơ thông dụng HCHO (anđehit fomic), CH3CHO (anđehit axetic),...
Đáp án A.
Câu 21:
Để khử ion Fe3+ trong dung dịch thành ion Fe2+ có thể dùng một lượng dư kim loại sau đây?
 Xem đáp án
Xem đáp án
Cu có dư cũng chỉ chuyển Fe3+ thành Fe2+
Đáp án B.
Câu 22:
Este nào sau đây khi đốt cháy thu được số mol CO2 bằng số mol H2O?
 Xem đáp án
Xem đáp án
Este thuộc dạng no, đơn chức, mạch hở (CnH2nO2) đốt cháy cho mol CO2 bằng mol H2O
Đáp án B.
Câu 24:
Cho hỗn hợp Cu và Fe3O4 vào dung dịch H2SO4 loãng dư. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch X và một lượng kim loại không tan. Muối trong dung dịch X là
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 25:
Dẫn khí CO dư qua ống sứ đựng 16 gam Fe2O3 nung nóng, sau khi phản ứng xảy ra hoàn toàn thu được m gam kim loại. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 26:
Cho dãy các chất: phenyl axetat, metyl axetat, etyl fomat, tripanmitin, vinyl axetat. Số chất trong dãy khi thủy phân trong dung dịch NaOH loãng, đun nóng sinh ra ancol là
 Xem đáp án
Xem đáp án
Este RCOOR' thủy phân sinh ra ancol khi nhóm COO liên kết với nguyên tử C no của gốc R'.
- Phenyl axetat:
CH3COOC6H5 + 2NaOH CH3COONa + C6H5ONa + H2O
- Metyl axetat:
CH3COOCH3 + NaOH CH3COONa + CH3OH
- Etyl fomat:
HCOOC2H5 + NaOH HCOONa + C2H5OH
- Tripanmitin:
(C15H31COO)3C3H5 + 3NaOH 3C15H31COONa + C3H5(OH)3
- Vinyl axetat:
CH3COOCH=CH2 + NaOH CH3COONa + CH3CHO
Vậy có 3 chất thỏa mãn: metyl axetat, etyl fomat, tripanmitin.
Đáp án D.
Câu 27:
Polisaccarit X là chất rắn dạng sợi, màu trắng, không mùi vị. X có nhiều trong bông nõn, gỗ, đay, gai... Thủy phân X thu được monosaccarit Y. Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Polisaccarit X là chất rắn dạng sợi, màu trắng, không mùi vị. X có nhiều trong bông nõn, gỗ, đay, gai… X là xenlulzơ.
Thủy phân X thu được monosaccarit Y Y là glucozơ.
A. Sai, Y tan tốt.
B. Sai, X có mạch không nhánh
C. Sai, X có M = 162n
D. Đúng
Đáp án D.
Câu 29:
Đốt cháy hoàn toàn 0,15 mol một amin X no, đơn chức, mạch hở bằng khí oxi vừa đủ thu được 1,2 mol hỗn hợp gồm CO2, H2O và N2. Số đồng phân bậc 1 của X là
 Xem đáp án
Xem đáp án
CTTQ của amin no, đơn chức, mạch hở là CnH2n+3N.
Phản ứng đốt cháy: CnH2n+3N + (1,5n + 0,75) O2 nCO2 + (n + 1,5) H2O + 0,5 N2
Từ đề bài ⟹ ⟹ n = 3 ⟹ Amin X là C3H9N.
Có 2 đồng phân amin bậc 1 có CTPT C3H9N là CH3CH2CH2NH2 và CH3CH(NH2)CH3.
Đáp án A.
Câu 30:
Phát biểu nào sau đây là sai?
 Xem đáp án
Xem đáp án
Sai vì poliamit có liên kết –CONH- kém bền trong môi trường axit và kiềm mạnh
Đáp án D.
Câu 31:
Dung dịch X chứa 0,375 mol K2CO3 và 0,3 mol KHCO3. Thêm từ từ dung dịch chứa 0,525 mol HCl và dung dịch X được dung dịch Y và V lít CO2 (đktc). Thêm dung dịch nước vôi trong dư vào Y thấy tạo thành m gam kết tủa. Giá trị của V và m là
 Xem đáp án
Xem đáp án
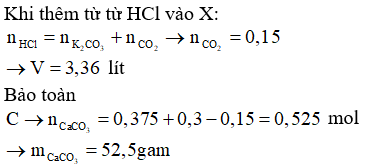
Đáp án B.
Câu 32:
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch Ba(HCO3)2 vào dung dịch KHSO4.
(b) Cho K vào dung dịch CuSO4 dư.
(c) Cho dung dịch NH4NO3 vào dung dịch Ba(OH)2.
(d) Cho dung dịch HCl tới dư vào dung dich C6H5ONa.
(e) Cho dung dịch CO2 tới dư vào dung dịch gồm NaOH và Ca(OH)2.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được cả chất rắn và khí là
 Xem đáp án
Xem đáp án
(a)
(b)
(c)
(d)
(e) CO2 dư + Ca(OH)2
CO2 dư + NaOH
Đáp án A.
Câu 33:
Thủy phân hoàn toàn hỗn hợp E chứa hai triglixerit X và Y trong dung dịch NaOH (đun nóng, vừa đủ), thu được 3 muối C15H31COONa, C17H33COONa, C17H35COONa với tỉ lệ mol tương ứng 2,5 : 1,75 : 1 và 6,44 gam glixerol. Mặt khác đốt cháy hoàn toàn 47,488 gam E cần vừa đủ a mol khí O2. Giá trị của a là
 Xem đáp án
Xem đáp án
Quy đổi E thành
và
và
Đốt 47,488 gam E cần
Đáp án B.
Câu 34:
Cho các phát biểu sau:
(a). Ở điều kiện thường, chất béo (C17H33COO)3C3H5 ở trạng thái lỏng.
(b). Fructozơ là monosaccarit duy nhất có trong mật ong.
(c). Thành phần dầu mỡ bôi trơn xe máy có thành phần chính là chất béo.
(d). Thành phần chính của giấy chính là xenlulozơ.
(e). Amilozơ và amilopectin đều cấu trúc mạch phân nhánh.
(f). Dầu chuối (chất tạo hương liệu mùi chuối chín) có chứa isoamyl axetat.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(a) Đúng, là chất béo không no nên ở trạng thái lỏng.
(b) Sai, mật ong chứa nhiều fructozo và glucozo.
(c) Sai, dầu mỡ bôi trơn có thành phần hidrocacbon
(d) Đúng
(e) Sai, amilozo không nhánh
(f) Đúng
Đáp án A.
Câu 35:
Cho 17,82 gam hỗn hợp gồm Na, Na2O, Ba, BaO (trong đó oxi chiếm 12,57% về khối lượng) vào nước dư, thu được a mol khí H 2 và dung dịch X. Cho dung dịch CuSO4 dư vào X, thu được 35,54 gam kết tủa. Giá trị của a là.
 Xem đáp án
Xem đáp án

Đáp án A
Câu 39:
Este X hai chức mạch hở, tạo bởi một ancol no với hai axit cacboxylic no, đơn chức. Este Y ba chức, mạch hở, tạo bởi glixerol với một axit cacboxylic không no, đơn chức (phân tử có hai liên kết pi). Đốt cháy hoàn toàn m gam hỗn hợp E gồm X và Y cần vừa đủ 0,5 mol O2 thu được 0,45 mol CO2. Mặt khác, thủy phân hoàn toàn 0,16 mol E cần vừa đủ 210 ml dung dịch NaOH 2M, thu được hai ancol (có cùng số nguyên tử cacbon trong phân tử) và a gam hỗn hợp ba muối. Phần trăm khối lượng của muối không no trong a gam là
 Xem đáp án
Xem đáp án

Đáp án B.
Câu 40:
Thí nghiệm xác định định tính nguyên tố cacbon và hiđro trong phân tử glucozơ được tiến hành theo các bước sau:
Bước 1: Trộn đều khoảng 0,2 gam glucozơ với 1 đến 2 gam đồng (II) oxit, sau đó cho hỗn hợp ống nghiệm khô (ống số 1) rồi thêm tiếp khoảng 1 gam đồng (II) oxit để phủ kín hỗn hợp. Nhồi một nhúm bông có rắc bột CuSO4 khan vào phần trên của ống số 1 rồi nút bằng nút cao su có ống dẫn khí.
Bước 2: Lắp ống số 1 lên giá thí nghiệm rồi nhúng ống dẫn khí vào dung dịch Ca(OH)2 đựng trong ống nghiệm (ống số 2).
Bước 3: Dùng đèn cồn đun nóng ống số 1 (lúc đầu đun nhẹ, sau đó đun tập trung vào phần có hỗn hợp phản ứng).
Cho các phát biểu sau:
(a) Sau bước 3, màu trắng của CuSO4 khan chuyển thành màu xanh của CuSO4.5H2O.
(b) Thí nghiệm trên, trong ống số 2 có xuất hiện kết tủa vàng.
(c) Ở bước 2, lắp ống số 1 sao cho miệng ống hướng xuống dưới.
(d) Thí nghiệm trên còn được dùng để xác định định tính nguyên tố oxi trong phân tử glucozơ.
(e) Kết thúc thí nghiệm: tắt đèn cồn, để ống số 1 nguội hẳn rồi mới đưa ống dẫn khí ra khỏi dung dịch trong ống số 2.
Số phát biểu sai là
 Xem đáp án
Xem đáp án
(a) Đúng
(b) Sai, kết tủa trắng (CaCO3)
(c) Đúng, ống hướng xuống để tránh hơi nước nưng tụ tại miệng ống chảy ngược xuống đáy ống có thể gây vỡ ống.
(d) Sai, chỉ định tính được C, H.
(e) Sai, đưa ống khí ra khỏi bình ngay khi ống 1 còn nóng để tránh nước bị hút vào ống 1 do áp suất giảm.
Đáp án B.