Dãy gồm các chất đều tác dụng với (xúc tác Ni, ) và với Na là:
A. , , .
B. , , .
C. , , .
D. , , .
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án C
A và B loại vì không phản ứng với Na
D loại vì không phản ứng với
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Axit X no, có 2 nguyên tử H trong phân tử. Số công thức cấu tạo của X
Dãy sắp xếp theo tính axit giảm dần trong các axit sau đây: , HCOOH, , là
Cho sơ đồ chuyển hóa sau: Tinh bột → X → Y → axit axetic. X và Y lần lượt là
Trong các chất: ancol propylic, anđehit fomic, axit butiric và etilen glycol, chất có nhiệt độ sôi nhỏ nhất là
Dung dịch axit axetic phản ứng được với tất cả các chất trong dãy nào sau đây?
Để trung hòa 6,72 gam một axit cacboxylic Y (no, đơn chức), cần dùng 200 gam dung dịch NaOH 2,24%. Công thức của Y là
I. Định nghĩa, phân loại, danh pháp
1. Định nghĩa
- Axit cacboxylic là những hợp chất hữu cơ mà phân tử có nhóm cacboxyl (-COOH) liên kết trực tiếp với nguyên tử cacbon hoặc nguyên tử hiđro.
- Ví dụ: H-COOH, COOH, HOOC-COOH
- Nhóm cacboxyl (-COOH) là nhóm chức của axit cacboxylic.
2. Phân loại
Dựa theo đặc điểm cấu tạo của gốc hiđrocacbon và số nhóm cacboxyl trong phân tử, các axit được chia thành:
- Axit no, đơn chức mạch hở, tổng quát (thường gặp):
CnH2n+1COOH (n ≥ 0) hay CmH2mO2 (m ≥ 1)
Ví dụ: H-COOH, COOH...
- Axit không no, đơn chức, mạch hở:
Ví dụ: C=CH-COOH,....
- Axit thơm, đơn chức:
Ví dụ: -COOH, C--COOH,...
- Axit đa chức:
Ví dụ: HOOC-COOH, HOOC-C-COOH...
3. Danh pháp
a) Tên thường
Một số axit có tên thông thường liên quan đến nguồn gốc tìm ra chúng. Ví dụ:

b) Tên thay thế
Tên thay thế của các axit no, đơn chức, mạch hở được xác định như sau:
+ Mạch chính của phân tử axit là mạch dài nhất, bắt đầu từ nhóm – COOH.
+ Mạch cacbon được đánh số bắt đầu từ nguyên tử cacbon của nhóm – COOH.
+ Tên thay thế =Axit + tên hiđrocacbon no tương ứng với mạch chính + oic.
Ví dụ: 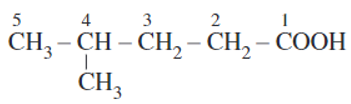
axit 4 – metylpentanoic
II. Đặc điểm cấu tạo
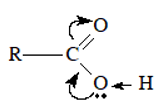
- Nhóm -COOH coi như được kết hợp bởi nhóm C = O và nhóm – OH.
- Liên kết O -H trong phân tử axit phân cực hơn liên kết O–H trong phân tử ancol, do đó nguyên tử H của nhóm COOH linh động hơn nguyên tử H của nhóm – OH ancol.
- Liên kết C- OH của nhóm cacboxyl phân cực mạnh hơn liên kết C – OH của ancol, phenol nên nhóm – OH của axit cacboxylic cũng dễ bị thay thế.
III. Tính chất vật lý
-Ở điều kiện thường các axit cacboxylic đều là những chất lỏng hoặc rắn.
- Nhiệt độ sôi tăng theo chiều tăng M và cao hơn các ancol có cùng M: nguyên nhân là do giữa các phân tử axit cacboxylic có liên kết hiđro bền hơn liên kết hidro giữa các phân tử ancol.
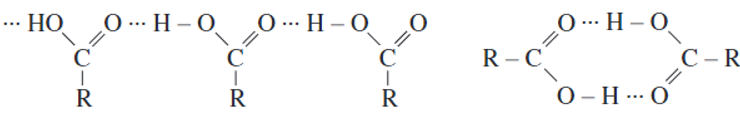
- Mỗi axit có vị riêng: axit axetic có vị giấm ăn, axit oxalic có vị chua của me …
IV. Tính chất hóa học
1.Tính axit
- Trong dung dịch, axit cacboxylic phân li thuận nghịch:
CCOOH ⇄ H+ + CCOO-
Dung dịch axit cacboxylic làm quỳ tím chuyển sang màu đỏ
- Tác dụng với bazơ, oxit bazơ tạo thành muối và nước. Ví dụ:
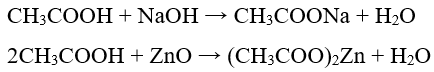
- Tác dụng với muối:
![]()
- Tác dụng với kim loại trước hiđro:
![]()
2. Phản ứng thế nhóm –OH
- Phản ứng giữa axit và ancol tạo thành este và nước được gọi là phản ứng este hóa.
- Tổng quát:
![]()
- Đặc điểm: phản ứng thuận nghịch, xúc tác S đặc.
- Ví dụ:
![]()
V. Điều chế
1. Phương pháp lên men giấm (phương pháp cổ truyền sản xuất axit axetic)
![]()
2. Oxi hóa anđehit axetic:
![]()
3.Oxi hóa ankan:
![]()
4.Từ metanol:
![]()
Đây là phương pháp hiện đại để sản xuất axit axetic.
VI. Ứng dụng
Các axit hữu cơ có ứng dụng trong nhiều lĩnh vực: làm nguyên liệu cho công nghiệp mĩ phẩm, công nghiệp dệt, công nghiệp hóa học …