Dãy các chất nào sau đây là muối axit
A.
B.
C.
D.
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án B
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Dãy gồm các chất đều phản ứng với dung dịch HCl ở điều kiện thường là
Nung hoàn toàn hỗn hợp 2 muối thu được 76 gam hai oxit và 33,6 lít (đktc). Khối lượng hỗn hợp muối ban đầu là
Cho 4 gam tác dụng với một lượng vừa đủ dung dịch HCl 2M. Thể tích dung dịch HCl đã dùng là
Khối lượng kết tủa tạo ra, khi cho 10,6 gam tác dụng vừa đủ với dung dịch là
Có 2 dung dịch thuốc thử nào sau đây có thể nhận biết 2 dung dịch trên
I. Axit cacbonic (Công thức hóa học C)
1. Trạng thái tự nhiên và tính chất vật lí
- Trong nước tự nhiên và nước mưa có hòa tan khí cacbonic: 1000 m3 nước hòa tan được 90 m3 khí C.
- Một phần khí C tác dụng với nước tạo thành dung dịch axit cacbonic, phần lớn vẫn tồn tại ở dạng phân tử C
2. Tính chất hóa học
- C là một axit yếu: dung dịch C chỉ làm quỳ tím chuyển thành màu đỏ nhạt, bị axit mạnh đẩy ra khỏi muối.
- C là một axit không bền: C tạo thành trong các phản ứng hóa học bị phân hủy ngay thành C và O.
II. Muối cacbonat
1. Phân loại:
Có hai loại muối cacbonat:
- Muối cacbonat trung hòa (hay muối cacbonat), không còn nguyên tố H trong thành phần gốc axit.
Ví dụ: NC, CaC,..
- Muối cacbonat axit (hay muối hiđrocacbonat), có nguyên tố H trong thành phần gốc axit.
Ví dụ: NaHC, Ca(HC)2...
2. Tính chất
a) Tính tan:
- Đa số muối cacbonat không tan trong nước, trừ một số muối cacbonat của kim loại kiềm như NCO3, C...
- Hầu hết các muối hiđrocacbonat tan trong nước như Ca(HC)2; Mg(HC)2 …
b) Tính chất hóa học
- Tác dụng với axit:
+ Muối cacbonat tác dụng với dung dịch axit mạnh hơn axit cacbonic (như HCl, HN, H,S,...) tạo thành muối mới và giải phóng C.
+ Ví dụ:

Hình 1: NaHC tác dụng với HCl
- Tác dụng với dung dịch bazơ
+ Một số dung dịch muối cacbonat tác dụng với dung dịch bazơ tạo thành muối cacbonat không tan và bazơ mới.
+ Ví dụ:

Hình 2: C tác dụng với Ba(OH)2
+ Muối hiđrocacbonat tác dụng với dung dịch kiềm tạo thành muối trung hòa và nước
Ví dụ:
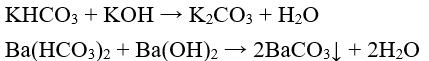
-Tác dụng với dung dịch muối
- Dung dịch muối cacbonat tác dụng với một số dung dịch muối tạo thành 2 muối mới
Ví dụ:
NC + CaC → 2NaCl + CaC↓
- Muối cacbonat bị nhiệt phân hủy
Nhiều muối cacbonat (trừ muối cacbonat trung hòa của kim loại kiềm) dễ bị nhiệt phân hủy giải phóng khí C
Ví dụ:
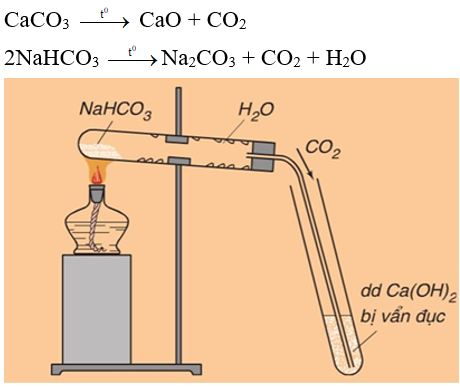
Hình 3: Nhiệt phân muối NaHC
3. Ứng dụng:
- CaC là thành phần chính của đá vôi, được dùng để sản xuất vôi, xi măng…
- NC được dùng để nấu xà phòng, sản xuất thủy tinh,..
- NaHC được dùng làm dược phẩm, hóa chất trong bình cứu hỏa,...
III. Chu trình cacbon trong tự nhiên
Trong tự nhiên luôn có sự chuyển hóa cacbon tự dạng này sang dạng khác. Sự chuyển hóa này diễn ra thường xuyên, liên tục và tạo thành chu trình khép kín.
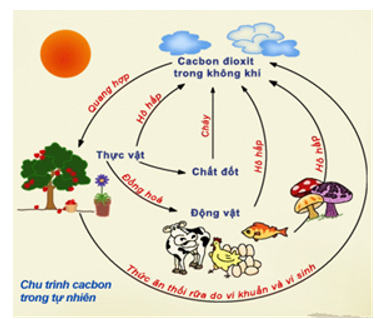
Hình 4: Chu trình cacbon trong tự nhiên