Giải Hoá học 10 Chân trời sáng tạo Bài 11: Liên kết hydrogen và tương tác van der Waals
Hamchoi.vn trân trọng giới thiệu: lời giải bài tập Hoá học lớp 10 Bài 11: Liên kết hydrogen và tương tác van der Waals sách Chân trời sáng tạo hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hoá học 10 Bài 11. Mời các bạn đón xem:
Giải bài tập Hóa lớp 10 Bài 11: Liên kết hydrogen và tương tác van der Waals
Video giải Hóa lớp 10 Bài 11: Liên kết hydrogen và tương tác van der Waals
Mở đầu trang 67 Hóa học 10: Các nhà hóa học đã nghiên cứu và kết luận rằng nếu không có liên kết hydrogen thì nước sẽ sôi ở -80oC. Như vậy, trong điều kiện thường, nước sẽ tồn tại ở thể khí (hơi nước). Khi đó, trên Trái Đất sẽ chẳng có các đại dương, sông, hồ,… và cũng không bao giờ có mưa. Mọi sự sống sẽ không tồn tại. Trái Đất sẽ là một hành tinh chết nếu không có sự hiện của liên kết hydrogen.
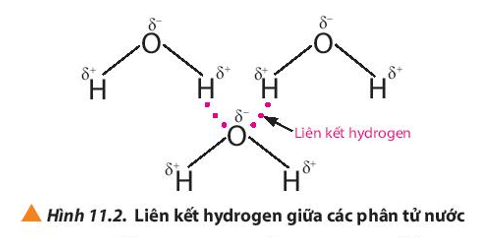
Liên kết hydrogen giữa các phân tử nước được tạo thành như thế nào? Ảnh hưởng của liên kết hydrogen với tính chất vật lí của nước ra sao?

Lời giải:
Lực hút tĩnh điện giữa nguyên tử H mang một phần điện tích dương (linh động) của phân tử H2O này với nguyên tử O mang một phần điện tích âm của phân tử nước khác, tạo thành liên kết giữa các phân tử nước, gọi là liên kết hydrogen, thường được biểu diễn bằng dấu ba chấm (…).
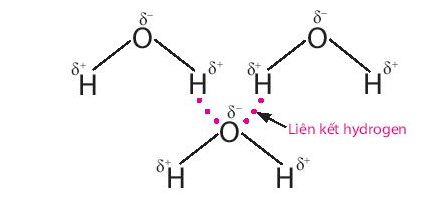
Nhờ có liên kết hydrogen mà ở điều kiện thường nước ở thể lỏng, có nhiệt độ sôi cao (100oC).
1. Liên kết hydrogen
Câu hỏi 1 trang 67 Hóa học 10: Giữa liên kết S-H và liên kết O-H, liên kết nào phân cực mạnh hơn? Vì sao?
Lời giải:
- Xét liên kết O – H:
∆χ = 3,44 – 2,2 = 1,24 ⇒ Liên kết O-H là liên kết cộng hóa trị phân cực.
- Xét liên kết S – H:
∆χ = 2,58 – 2,2 = 0,38 ⇒ Liên kết S-H là liên kết cộng hóa trị không phân cực.
Vậy liên kết O-H phân cực mạnh hơn.
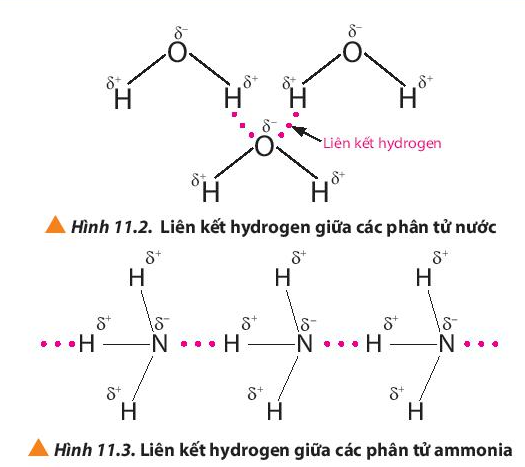
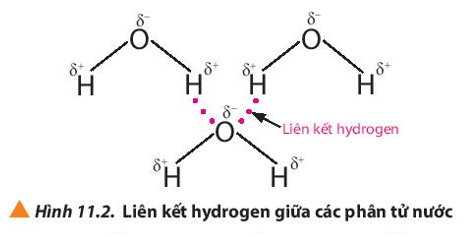
Câu hỏi 2 trang 68 Hóa học 10: Quan sát các Hình 11.2 và 11.3, em hiểu thế nào là liên kết hydrogen giữa các phân tử?
Lời giải:
Liên kết hydrogen là một loại liên kết yếu, được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết.
Liên kết hydrogen thường được biểu diễn bằng dấu ba chấm (…)
Câu hỏi 3 trang 68 Hóa học 10: So sánh độ bền của liên kết hydrogen với liên kết cộng hóa trị và liên kết ion.
Lời giải:
Thứ tự tăng dần độ bền liên kết: Liên kết hydrogen < liên kết cộng hóa trị < liên kết ion.
Luyện tập trang 68 Hóa học 10: Điều gì đã khiến H2O có nhiệt độ sôi cao hơn H2S? Giải thích.
Lời giải:
H2O có liên kết hydrogen liên phân tử còn H2S không có liên kết này nên H2O có nhiệt độ sôi cao hơn H2S.
Câu hỏi 4 trang 68 Hóa học 10: So sánh nhiệt độ sôi và khả năng hòa tan trong nước giữa NH3 và CH4. Giải thích.
Lời giải:
- NH3 có nhiệt độ sôi cao hơn CH4 do các phân tử NH3 có thể tạo liên kết hydrogen với nhau (còn CH4 thì không):
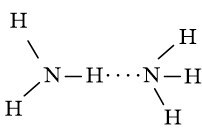
- NH3 tan trong nước nhiều hơn CH4 do phân tử NH3 có thể tạo liên kết hydrogen với nước còn CH4 thì không.
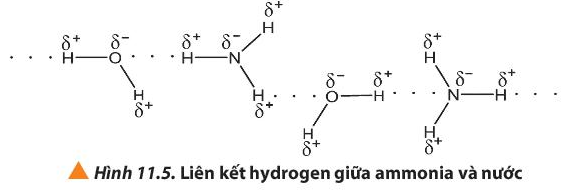
Câu hỏi 5 trang 69 Hóa học 10: Giải thích vì sao một phân tử nước có thể tạo được liên kết hydrogen tối đa với bốn phân tử nước khác
Lời giải:
![]()
Nguyên tử O có 2 cặp electron chưa liên kết nên có thể tạo 2 liên kết hydrogen với 2 nguyên tử H của các phân tử nước khác; 2 nguyên tử H của phân tử nước đủ điều kiện tạo liên kết hydrogen với 2 nguyên tử O của các phân tử nước khác.
Như vậy, một phân tử nước có thể tạo 4 liên kết hydrogen với các phân tử nước khác xung quanh.
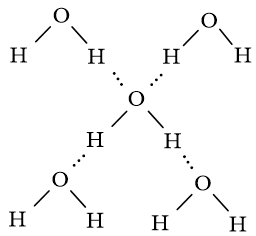
Vận dụng trang 69 Hóa học 10: Vì sao nên tránh ướp lạnh các lon bia, nước giải khát,… trong ngăn đá của tủ lạnh?
Lời giải:
Khi cho nước vào ngăn đá tủ lạnh, nước chuyển từ trạng thái lỏng thành trạng thái rắn. Ở trạng thái rắn nước có cấu trúc tinh thể phân tử với bốn phân tử H2O phân bố ở bốn đỉnh của một tứ diện đều, bên trong là cấu trúc rỗng.
Ướp lạnh các lon bia, nước giải khát,… trong ngăn đá của tủ lạnh thể tích dung dịch trong chai giãn nở làm lon bị biến dạng và có thể phát nổ.

2. Tương tác Van Der Waals
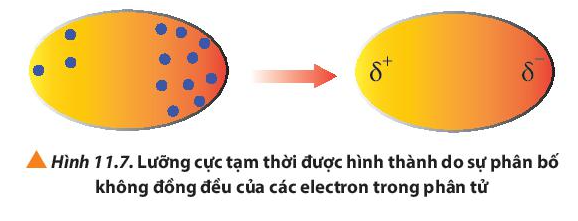
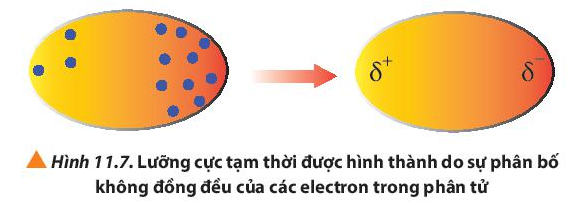
Câu hỏi 6 trang 69 Hóa học 10: Quan sát Hình 11.7, cho biết thế nào là một lưỡng cực tạm thời?
Lời giải:
Trong các phân tử, các electron không ngừng chuyển động. Khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các lưỡng cực tạm thời.
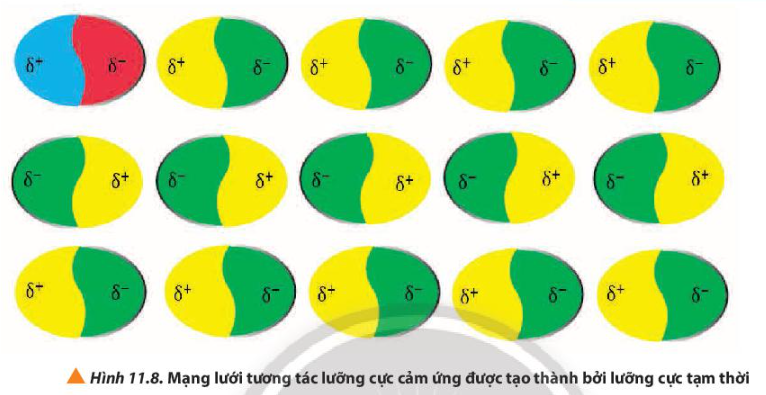
Câu hỏi 7 trang 70 Hóa học 10: Các lưỡng cực tạm thời và lưỡng cực cảm ứng hút nhau bằng lực hút nào?
Lời giải:
Các lưỡng cực tạm thời và lưỡng cực cảm ứng hút nhau bằng lực hút trái dấu.
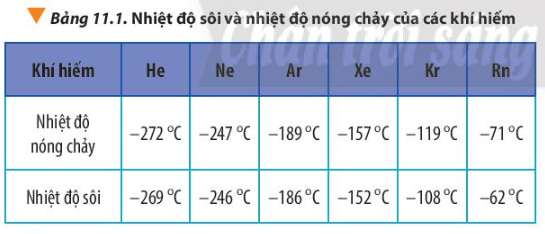
Câu hỏi 8 trang 70 Hóa học 10: Giải thích xu hướng biến đổi bán kính nguyên tử, nhiệt độ nóng chảy và nhiệt độ sôi của các nguyên tố khí hiếm trong Bảng 11.1
Lời giải:
Theo chiều tăng dần của điện tích hạt nhân nguyên tử trong nhóm VIIIA, bán kính nguyên tử tăng đồng thời khối lượng nguyên tử tăng ⇒ Tương tác van der Waals tăng ⇒ Nhiệt độ nóng chảy và nhiệt độ sôi tăng.
Vận dụng trang 70 Hóa học 10: Tại sao nhện nước có thể di chuyển trên mặt nước?

Lời giải:
Liên kết hydrogen giữa các phân tử nước trên bề mặt nước và giữa các phân tử nước trên bề mặt với lớp nước bên dưới tạo ra sức căng bề mặt cho nước. Con nhện nước có khối lượng nhỏ, chân của con nhện nước gồm các chất kị nước, phân tử các chất này đẩy nước khiến cho chân của nhện nước không bị nước bao bọc và tụt xuống dưới nước. Vì vậy chúng có thể di chuyển trên bề mặt nước mà không làm vỡ bề mặt nước.
Bài tập (trang 71)
Bài 1 trang 71 Hóa học 10: Hợp chất nào dưới đây tạo được liên kết hydrogen liên phân tử
A. CH4
B. H2O
C. PH3
D. H2S
Lời giải:
Đáp án đúng là: B
H2O tạo được liên kết hydrogen liên phân tử:
Bài 2 trang 71 Hóa học 10: Sự phân bố electron không đồng đều trong một nguyên tử hay một phân tử hình thành nên
A. một ion dương
B. một ion âm
C. một lưỡng cực vĩnh viễn
D. một lưỡng cực tạm thời
Lời giải:
Đáp án đúng là: D
Sự phân bố electron không đồng đều trong một nguyên tử hay một phân tử hình thành nên một lưỡng cực tạm thời.
Bài 3 trang 71 Hóa học 10: Khí hiếm nào dưới đây có nhiệt độ sôi thấp nhất?
A. Ne
B. Xe
C. Ar
D. Kr
Lời giải:
Đáp án đúng là: A
Ne có nhiệt độ sôi thấp nhất do trong nhóm VIIIA, từ Ne đến Rn bán kính nguyên tử tăng đồng thời khối lượng nguyên tử tăng ⇒ Tương tác van der Waals tăng ⇒ Nhiệt độ nóng chảy và nhiệt độ sôi tăng.
Bài 4 trang 71 Hóa học 10: Biểu diễn liên kết hydrogen giữa các phân tử:
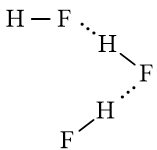
a) Hydrogen fluoride
b) Ethanol (C2H5OH) và nước
Lời giải:
b) Liên kết hydrogen được hình thành giữa các phân tử HF:
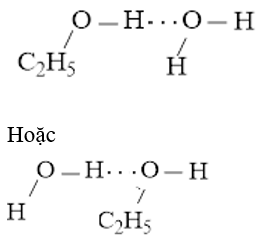
b) Liên kết hydrogen được hình thành giữa H2O và C2H5OH
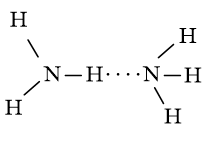
Bài 5 trang 71 Hóa học 10: Trong hai chất ammonia (NH3) và phosphine (PH3), theo em chất nào có nhiệt độ sôi và độ tan trong nước lớn hơn? Giải thích
Lời giải:
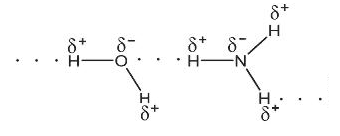
NH3 có nhiệt độ sôi và độ tan trong nước lớn hơn PH3 do NH3 có thể tạo liên kết hydrogen với nhau và với nước.
Bài viết liên quan
- Giải Hoá học 10 Chân trời sáng tạo Bài 9: Liên kết ion
- Giải Hoá học 10 Chân trời sáng tạo Bài 10: Liên kết cộng hóa trị
- Giải Hoá học 10 Chân trời sáng tạo Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống
- Giải Hoá học 10 Chân trời sáng tạo Bài 13 Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
- Giải Hoá học 10 Chân trời sáng tạo Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
