Cho một lượng sắt vào 100 ml dung dịch HCl. Phản ứng xong, thu được 3,36 lít khí (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính khối lượng Fe đã tham gia phản ứng.
c) Tính nồng độ mol của dung dịch HCl đã dùng.
d) Tính khối lượng muối sắt tạo thành.
(Cho: H = 1; Fe = 56; O = 16; Cl = 35,5)
 Giải bởi Vietjack
Giải bởi Vietjack
a) Phương trình hóa học:
Fe + 2HCl → FeCl2+ H2↑
b) Số mol H2là: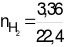 = 0,15 mol
= 0,15 mol
Phương trình phản ứng:

Số mol Fe là: nFe= 0,15 mol
Vậy khối lượng Fe đã tham gia phản ứng là:
mFe= 0,15.56 = 8,4 gam.
c) Phương trình phản ứng:
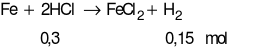
Số mol HCl là: nHCl= 0,3 mol
Vậy nồng độ mol của dung dịch HCl đã dùng là:
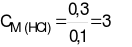 M
M
d) Phương trình phản ứng:
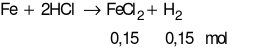
Theo phương trình phản ứng: = 0,15 mol
= 0,15 mol
Vậy khối lượng FeCl2là: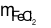 = 0,15.127 = 19,05 gam.
= 0,15.127 = 19,05 gam.
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Cho các oxit sau: Al2O3, MgO, CO, CO2, Fe2O3, NO. Hãy cho biết trong các oxit trên, oxit nào là oxit bazơ, oxit axit, oxit lưỡng tính, oxit trung tính.
Cho các chất sau: BaO, SO3, Fe3O4. Viết phương trình với:
a) Chất nào tác dụng được với dung dịch HCl?
b) Chất nào tác dụng được với dung dịch Ca(OH)2?
Có những chất: Ba, BaO, BaCO3, Ba(HCO3)2, Ba(OH)2, BaCl2. Dựa vào mối quan hệ giữa các chất, hãy sắp xếp thành một dãy chuyển đổi hóa học. Viết các PTHH.