Tính chất hóa học nào không phải của axit?
A. Tác dụng với kim loại
B. Tác dụng với muối
C. Tác dụng với oxit axit
D. Tác dụng với oxit bazơ
 Giải bởi Vietjack
Giải bởi Vietjack
Chọn C
Axit thường không phản ứng với oxit axit
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Chất tác dụng với dung dịch HCl tạo thành chất khí nhẹ hơn không khí là:
Cho 11,2 lít vào 500 ml dung dịch NaOH 25% (D = 1,3 g/ml). Nồng độ mol/lit của dung dịch muối tạo thành là
Cho 2,24 lít C (đktc) tác dụng với dung dịch Ba( dư. Khối lượng chất kết tủa thu được là :
Phải đốt bao nhiêu gam cacbon để khi cho khí tạo ra trong phản ứng trên tác dụng với 3,4 lít dung dịch NaOH 0,5M ta được 2 muối với muối hiđrocacbonat có nồng độ mol bằng 1,4 lần nồng độ mol của muối trung hoà.
Dẫn 448 ml (đktc) sục vào bình chứa 100 ml dung dịch KOH 0,25M. Khối lượng hai muối tạo thành là
Dùng 400ml dung dịch Ba 0,1M hấp thụ hoàn toàn V lít khí S (đktc). Sau phản ứng thu được muối BaS không tan. Giá trị bằng số của V là:
Dung dịch A tác dụng với CuO tạo ra dung dịch có màu xanh lam. A là
Dãy gồm các oxit tác dụng được với nước tạo thành dung dịch axit là:
Dẫn 22,4 lít khí ( đktc) vào 200g dung dịch NaOH 20%. Sau phản ứng tạo ra sản phẩm nào trong số các sản phẩm sau:
Khử 16 gam bằng CO dư , sản phẩm khí thu được cho đi vào dung dịch dư thu được a gam kết tủa. Giá trị của a là
Dẫn 3,36 lít khí (đktc) vào 40g dung dịch NaOH 20%. Sản phẩm thu được sau khi cô cạn dung dịch và khối lượng tương ứng là:
Chất nào sau đây tác dụng với Fe ở nhiệt độ thường tạo ra khí hiđro là
Hiện tượng quan sát được khi cho mẩu magie vào ống nghiệm chứa axit HCl dư là:
I. Tính chất hóa học của axit
1. Axit làm đổi màu chất chỉ thị màu
- Dung dịch axit làm đổi màu quỳ tím thành đỏ.
- Trong hóa học, quỳ tím là chất chỉ thị màu để nhận biết dung dịch axit.
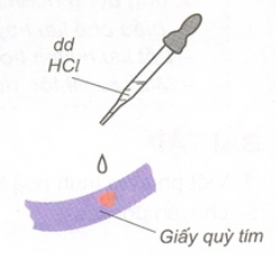
Hình 1: Dung dịch axit HCl làm quỳ tím đổi màu
2. Axit tác dụng với kim loại
- Dung dịch axit tác dụng được với nhiều kim loại tạo thành muối và giải phóng khí hiđro.
Ví dụ:
3S (dd loãng) + 2Al → (SO4)3 + 3 (↑)
Mg + 2HCl → Mg + (↑)

Hình 2: Nhôm tác dụng với S loãng
Chú ý:
- Các kim loại Hg, Cu, Ag, Au, Pt …không tác dụng với HCl, S loãng.
- Các kim loại có nhiều hóa trị như Fe, Cr … phản ứng với HCl, S loãng thu được muối, trong đó kim loại ở mức hóa trị thấp. Ví dụ:
2HCl + Fe → Fe + (↑)
- Axit HN và S đặc tác dụng được với nhiều kim loại nhưng không giải phóng khí hiđro. Ví dụ:
Cu + 2S đặc CuS + S↑ + 2O
3Cu + 8HN loãng → 3Cu(N)2 + 2NO ↑ + 4O
3. Axit tác dụng với bazơ
Tổng quát: Axit + bazơ → muối + O
Ví dụ:
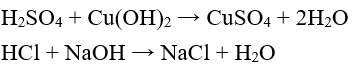
Phản ứng của axit với bazơ được gọi là phản ứng trung hòa.
4. Axit tác dụng với oxit bazơ
Tổng quát: Axit + oxit bazơ → muối + O
Ví dụ:
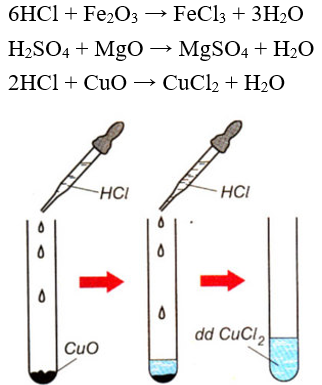
Hình 3: CuO tác dụng với HCl
5. Axit tác dụng với muối
Tổng quát: Axit + muối → axit mới + muối mới
Ví dụ:
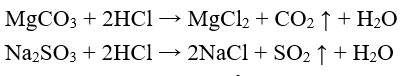
II. Axit mạnh và axit yếu
Dựa vào tính chất hóa học, axit được phân làm 2 loại:
+ Axit mạnh như HCl, S, HN,…
+ Axit yếu như S, C,…