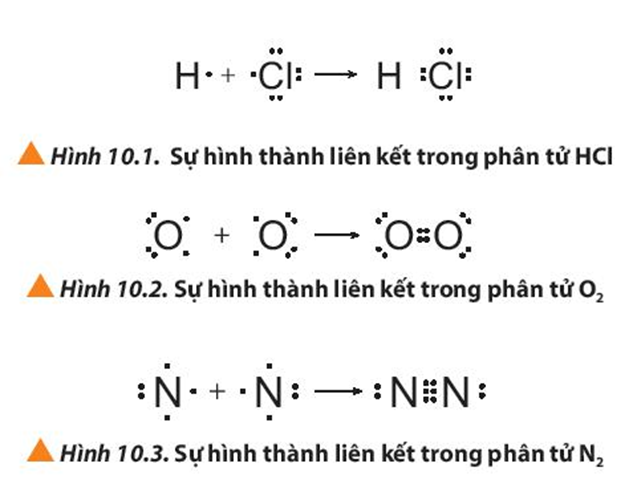
Quan sát các Hình 10.1 đến 10.3, cho biết quy tắc octet đã được áp dụng ra sao khi các nguyên tử tham gia hình thành liên kết.
 Giải bởi Vietjack
Giải bởi Vietjack
Các nguyên tử đã góp chung electron khi tham gia hình thành liên kết để mỗi nguyên tử đều đạt được cấu hình electron bền vững giống khí hiếm với 8 electron lớp ngoài cùng.
- Để tạo thành liên kết trong phân tử HCl: Nguyên tử H và Cl, mỗi nguyên tử góp chung 1 electron tạo thành 1 cặp electron dùng chung. Khi đó H đạt được cấu hình electron của khí hiếm He với 2 electron lớp ngoài cùng. Cl đạt được cấu hình electron của khí hiếm Ar với 8 electron lớp ngoài cùng.
- Để tạo thành liên kết trong phân tử O2: Mỗi nguyên tử O góp chung 2 electron tạo thành 2 cặp electron dùng chung. Khi đó mỗi nguyên tử O đều đạt được cấu hình electron của khí hiếm Ne với 8 electron lớp ngoài cùng.
- Để tạo thành liên kết trong phân tử N2: Mỗi nguyên tử N góp chung 3 electron tạo thành 3 cặp electron dùng chung. Khi đó mỗi nguyên tử N đều đạt được cấu hình electron của khí hiếm Ne với 8 electron lớp ngoài cùng.
Gói VIP thi online tại VietJack (chỉ 400k/1 năm học), luyện tập gần 1 triệu câu hỏi có đáp án chi tiết
Sự xen phủ giữa hai orbital p trong trường hợp nào sẽ tạo thành liên kết σ? Trong trường hợp nào sẽ tạo thành liên kết π? Cho ví dụ.
Trình bày sự hình thành liên kết cho – nhận trong phân tử sulfur dioxide (SO2).
Hydrogen sulfide (H2S) và phosphine (PH3) đều là những chất có mùi khó ngửi và rất độc. Trình bày sự tạo thành liên kết cộng hóa trị trong phân tử các chất trên.
Năng lượng liên kết của các hydrogen halide được liệt kê trong bảng sau:
|
Hydrogen halide |
Năng lượng liên kết (kJ/mol) |
|
HF |
565 |
|
HCl |
427 |
|
HBr |
363 |
|
HI |
295 |
Sắp xếp theo chiều tăng dần độ bền liên kết trong các phân tử HF, HCl, HBr và HI
Cho biết số liên kết σ và liên kết п trong phân tử acetylene (C2H2).
Mô tả sự tạo thành liên kết trong phân tử chlorine bằng sự xen phủ của các AO.
Trình bày sự hình thành liên kết cộng hóa trị trong phân tử NH3.
Trong một số trường hợp đặc biệt, khí nitrogen được sử dụng để bơm lốp (vỏ) xe thay cho không khí là do khí oxygen có trong không khí có thể oxi hóa cao su theo thời gian. Khí nitrogen vì sao khắc phục được nhược điểm này?
Viết công thức electron, công thức Lewis và công thức cấu tạo của Cl2, H2O, CH4.
Giải thích sự hình thành liên kết trong các phân tử HCl, O2 và N2.