Vận dụng quy tắc octet để giải thích sự hình thành liên kết trong các phân tử
Giải Hóa 10 Bài 10 - Kết nối tri thức: Quy tắc octet
Câu hỏi 3 trang 50 Hóa học 10: Vận dụng quy tắc octet để giải thích sự hình thành liên kết trong các phân tử F2, CCl4 và NF3.
Lời giải:
- Sự hình thành liên kết trong phân tử F2
Khi hình thành liên kết hóa học trong phân tử F2, nguyên tử fluorine có 7 electron hóa trị, mỗi nguyên tử fluorine cần thêm 1 electron để đạt cấu hình electron bão hòa theo quy tắc octet nên mỗi nguyên tử fluorine góp chung 1 electron.
Phân tử Fe được biểu diễn 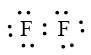
Xung quanh mỗi nguyên tử fluorine đều có 8 electron.
- Sự hình thành liên kết hóa học trong phân tử CCl4
Nguyên tử C có 4 electron hóa trị, nguyên tử Cl có 7 electron hóa trị. Mỗi nguyên tử Cl cần thêm 1 electron và nguyên tử C cần thêm 4 electron để đạt cấu hình electron bão hòa theo quy tắc octet.
Phân tử CCl4 được biểu diễn 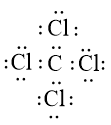
Xung quanh mỗi nguyên tử C và Cl đều có 8 electron.
- Sự hình thành liên kết hóa học trong phân tử NF3
Nguyên tử N có 5 electron hóa trị, nguyên tử F có 7 electron hóa trị. Mỗi nguyên tử F cần thêm 1 electron và nguyên tử N cần thêm 3 electron để đạt cấu hình electron bão hòa theo quy tắc octet.
Phân tử NF3 được biểu diễn 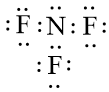
Xung quanh mỗi nguyên tử N và F đều có 8 electron.
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức với cuộc sống hay, chi tiết khác:
Câu hỏi 4 trang 50 Hóa học 10: Phosphine là hợp chất hoá học giữa phosphorus với hydrogen...
Bài viết liên quan
- Khi nguyên tử fluorine nhận thêm 1 electron thì ion tạo thành có cấu hình electron
- Để giảm năng lượng, các nguyên tử kết hợp lại thành phân tử theo xu hướng nào
- Phosphine là hợp chất hoá học giữa phosphorus với hydrogen
- Vận dụng quy tắc octet để giải thích sự hình thành liên kết hóa học
- Hợp chất NaCl nóng chảy ở nhiệt độ cao và có khả năng dẫn điện khi nóng chảy hoặc khi hòa tan trong dung dịch
