Giải Hóa 10 Kết nối tri thức Bài 3: Cấu trúc lớp vỏ electron nguyên tử
Hamchoi.vn trân trọng giới thiệu: lời giải bài tập Hóa lớp 10 Bài 3: Cấu trúc lớp vỏ electron nguyên tử sách Kết nối tri thức hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa 10 Bài 3. Mời các bạn đón xem:
Giải bài tập Hóa lớp 10 Bài 3: Cấu trúc lớp vỏ electron nguyên tử
Video giải bài tập Hóa lớp 10 Bài 3: Cấu trúc lớp vỏ electron nguyên tử
Lời giải:
- Theo mô hình hành tinh nguyên tử: Các electron chuyển động xung quanh hạt nhân nguyên tử theo những quỹ đạo tròn hay bầu dục, giống như quỹ đạo của các hành tinh quay xung quanh Mặt Trời.
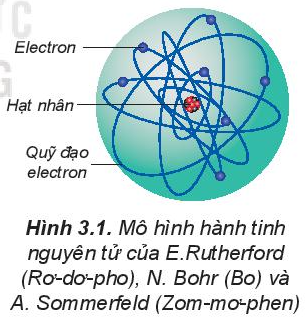
- Theo mô hình hiện đại: Trong nguyên tử, electron chuyển động rất nhanh, không theo quỹ đạo xác định. Tuy nhiên, người ta có thể xác định được vùng không gian xung quanh hạt nhân mà ở đó xác suất có mặt (xác suất tìm thấy) electron là lớn nhất (khoảng 90%). Vùng không gian xung quanh hạt nhân tìm thấy electron có thể hình dung như một đám mây electron, được gọi là orbital nguyên tử (kí hiệu là AO).

- Cấu hình electron của nguyên tử và cách viết cấu hình electron của 20 nguyên tố đầu tiên trong bảng tuần hoàn tuần theo: nguyên tí vững bền, nguyên lí Pauli và quy tắc Hund.
+ Nguyên lí vững bền: Các electron trong nguyên tử ở trạng thái cơ bản lần lượt chiếm các orbital có mức năng lượng từ thấp đến cao: 1s 2s 2p 3s 3p 4s ...
+ Nguyên lí Pauli: Các phân lớp 1s, 2s, 2p, 3s đều chứa tối đa các electron nên trong mỗi AO có 2 electron (kí hiệu ↑, ↓) có chiều quay ngược nhau được viết là ↑↓.
+ Quy tắc Hund: Phân lớp 3p chỉ có 2 electron nên các electron phải phân bố sao cho số electron độc thân là tối đa và các electron này có chiều tự quay giống nhau (↑).
I. Chuyển động của electron trong nguyên tử
Lời giải:
Theo mô hình hiện đại: Trong nguyên tử, electron chuyển động rất nhanh, không theo quỹ đạo xác định. Tuy nhiên, người ta có thể xác định được vùng không gian xung quanh hạt nhân mà ở đó xác suất có mặt (xác suất tìm thấy) electron là lớn nhất (khoảng 90%). Vùng không gian xung quanh hạt nhân tìm thấy electron có thể hình dung như một đám mây electron, được gọi là orbital nguyên tử (kí hiệu là AO).

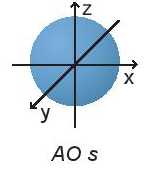
Câu hỏi 2 trang 22 Hóa học 10: Orbital s có dạng
Lời giải:
Đáp án đúng là: C
Orbital s có dạng hình cầu.
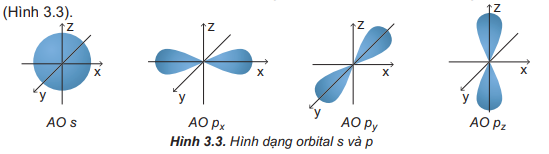
Câu hỏi 3 trang 22 Hóa học 10: Quan sát Hình 3.3 và nêu sự định hướng của các AO p trong không gian.
Lời giải:
Orbital p có dạng hình số 8 nổi và có 3 sự định hướng:
+ Orbital px định hướng theo trục x.
+ Orbital py định hướng theo trục y.
+ Orbital pz định hướng theo trục z.
II. Lớp và phân lớp electron
Câu hỏi 4 trang 23 Hóa học 10: Hãy cho biết tổng số electron tối đa chứa trong:
Lời giải:
a) Phân lớp p có 3 AO px, py, pz 
Mỗi AO chứa tối đa 2 electron
⇒ Tổng số electron tối đa chứa trong phân lớp p là 2.3 = 6 electron
b) Phân lớp d có 5 AO 
Mỗi AO chứa tối đa 2 electron
⇒ Tổng số electron tối đa chứa trong phân lớp d là 2.5 = 10 electron
Lời giải:
Đáp án đúng là: C
Em cần nhớ:
- Trong lớp electron thứ n có n2 AO (n ≤ 4)
- Mỗi AO chứa tối đa 2 electron
Lớp L (n = 2) có 22 = 4 AO ⇒ Tổng số electron tối đa bằng 4.2 = 8 electron
Lớp M (n = 3) có 32 = 9 AO ⇒ Tổng số electron tối đa bằng 9.2 = 18 electron.
III. Cấu hình electron của nguyên tử
Câu hỏi 6 trang 24 Hóa học 10: Cấu hình electron của nguyên tử có Z = 16 là
Lời giải:
Đáp án đúng là: C
Nguyên tử có Z = 16 nên nguyên tử có 16 electron.
⇒ Cấu hình electron là 1s22s22p63s23p4.
Lời giải:
- Cấu hình electron của nguyên tử có Z = 8 là 1s22s22p4, được biểu diễn theo ô orbital là:
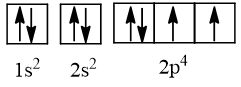
- Cấu hình electron của nguyên tử có Z = 11 là 1s22s22p63s1, được biểu diễn theo ô orbital là:
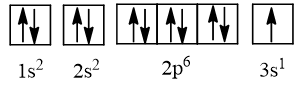
Lời giải:
Ta có: Z = 14 ⇒ Nguyên tử silicon có 14 electron.
- Viết thứ tự các lớp và phân lớp electron theo chiều tăng của năng lượng:
1s 2s 2p 3s 3p 4s …
- Điền các electron vào các phân lớp electron theo nguyên lí vững bền cho đến electron cuối cùng
1s22s22p63s23p2.
⇒ Cấu hình electron của nguyên tử silicon có Z = 14: 1s22s22p63s23p2, được biểu diễn theo ô orbital là:
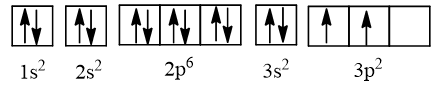
Lưu ý:
- Nguyên lí vững bền: Các electron trong nguyên tử ở trạng thái cơ bản lần lượt chiếm các orbital có mức năng lượng từ thấp đến cao: 1s 2s 2p 3s 3p 4s ...
- Nguyên lí Pauli: Các phân lớp 1s, 2s, 2p, 3s đều chứa tối đa các electron nên trong mỗi AO có 2 electron (kí hiệu ↑, ↓) có chiều quay ngược nhau được viết là ↑↓.
- Quy tắc Hund: Phân lớp 3p chỉ có 2 electron nên các electron phải phân bố sao cho số electron độc thân là tối đa và các electron này có chiều tự quay giống nhau (↑).
Lời giải:
Chlorine có Z = 17 nên nguyên tử chlorine có 17 electron.
- Viết thứ tự các lớp và phân lớp electron theo chiều tăng của năng lượng:
1s 2s 2p 3s 3p 4s …
- Điền các electron vào các phân lớp electron theo nguyên lí vững bền:
1s22s22p63s23p5.
⇒ Cấu hình electron của nguyên tử chlorine là: 1s22s22p63s23p5.
⇒ Lớp ngoài cùng có 7 electron.
⇒ Chlorine là phi kim.
Lời giải:
- Cấu hình electron nguyên tử của nitrogen (Z = 7) là 1s22s22p3.
⇒ Lớp ngoài cùng có 5 electron.
⇒ Nitrogen là phi kim.
- Cấu hình electron nguyên tử của oxygen (Z = 8) là 1s22s22p4.
⇒ Lớp ngoài cùng có 6 electron.
⇒ Oxygen là phi kim.
- Cấu hình electron nguyên tử của aluminium (Z = 13) là 1s22s22p63s23p1.
⇒ Lớp ngoài cùng có 3 electron.
⇒ Aluminium là kim loại.
Bài viết liên quan
- Giải Hóa 10 Kết nối tri thức Bài 1: Thành phần của nguyên tử
- Giải Hóa 10 Kết nối tri thức Bài 2: Nguyên tố hóa học
- Giải Hóa 10 Kết nối tri thức Bài 4: Ôn tập chương 1
- Giải Hóa 10 Kết nối tri thức Bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
- Giải Hóa 10 Kết nối tri thức Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một chu kì và trong một nhóm