Xét phản ứng: H2 + Cl2 → 2HCl
Giải Hóa 10 Bài 19 - Kết nối tri thức: Tốc độ phản ứng
Câu hỏi 1 trang 93 Hóa học 10: Xét phản ứng: H2 + Cl2 → 2HCl.
Nghiên cứu sự thay đổi nồng độ một chất trong phản ứng theo thời gian, thu được đồ thị sau:
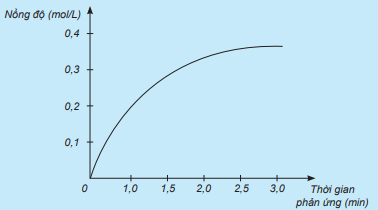
a) Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất nào?
b) Nêu đơn vị của tốc độ phản ứng trong trường hợp này.
Lời giải:
a) Dựa vào đồ thị ta thấy: Nồng độ ban đầu của chất là 0 mol/L. Thời gian của phản ứng tăng, nồng độ dung dịch chất tăng.
⇒ Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất sản phẩm HCl.
b) Đơn vị của tốc độ phản ứng trong trường hợp này là mol/(L.min).
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức với cuộc sống hay, chi tiết khác:
Câu hỏi 1 trang 93 Hóa học 10: Xét phản ứng: H2 + Cl2 → 2HCl...
Hoạt động trang 93 Hóa học 10: Phản ứng phân hủy H2O2: H2O2 ⟶ H2O + O2...
Câu hỏi 2 trang 94 Hóa học 10: Cho phản ứng của các chất ở thể khí: 2NO + 2H2 → N2 + 2H2O...
Câu hỏi 3 trang 96 Hóa học 10: Cho phản ứng: X + Y → XY...
Câu hỏi 4 trang 97 Hóa học 10: Nêu mối liên hệ giữa nồng độ và áp suất của khí trong hỗn hợp....
Câu hỏi 5 trang 97 Hóa học 10: Áp suất ảnh hưởng đến tốc độ phản ứng nào sau đây...
Câu hỏi 6 trang 98 Hóa học 10: Hãy giải thích tại sao khi nhiệt độ tăng thì tốc độ phản ứng tăng...
Câu hỏi 7 trang 98 Hóa học 10: Nêu ý nghĩa của hệ số nhiệt độ Van't Hoff....
Câu hỏi 8 trang 98 Hóa học 10: Ở 20 °C, tốc độ một phản ứng là 0,05 mol/(L.min)...
Hoạt động trang 98 Hóa học 10: Nghiên cứu ảnh hưởng của diện tích bề mặt đến tốc độ phản ứng...
Hoạt động trang 99 Hóa học 10: Nghiên cứu ảnh hưởng của chất xúc tác đến tốc độ phản ứng...
Câu hỏi 9 trang 99 Hóa học 10: Thực hiện hai phản ứng phân huỷ H2O2 một phản ứng có xúc tác MnO2...
Bài viết liên quan
- Một bình gas (khí hoá lỏng) chứa hỗn hợp propane và butane với tỉ lệ số mol 1:2
- Làm thế nào có thể so sánh sự nhanh, chậm của các phản ứng hoá học để thúc đẩy
- Phản ứng phân hủy H2O2: H2O2 ⟶ H2O + 1/2 O2
- Cho phản ứng của các chất ở thể khí: 2NO + 2H2 → N2 + 2H2O
- Nghiên cứu ảnh hưởng của nồng độ đến tốc độ phản ứng
