Chủ đề 7: Bài toán Etilen, Axetilen cộng H2, Br2 có đáp án
-
537 lượt thi
-
11 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Chọn đáp án A
X phản ứng với Br2 theo tỉ lệ 1:1 nên CTTQ của X là CnH2n
CnH2n + Br2 → CnH2nBr2
→ Chất hữu cơ Y là CnH2nBr2
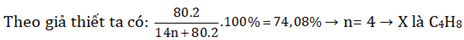
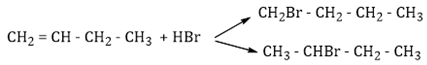
Khi X phản ứng với HBr cho 2 sản phẩm hữu cơ khác nhau → X là but-1-en
Câu 2:
 Xem đáp án
Xem đáp án
Chọn đáp án C
Trong cùng 1 điều kiện thì tỉ lệ thể tích cũng chính là tỉ lệ về số mol
Theo giả thiết ta chọn: nH2 = nCnH2n = 1 mol
CnH2n + H2 → CnH2n+2
Theo phương trình , số mol khí giảm chính là số mol của H2
H% = 75% → nH2(pư) = 0,75 mol
→ Số mol khí sau phản ứng là: n khí sau pư = nH2(sau pư) + nCnH2n(sau pư) + nCnH2n+2 = 1 + 1 - 0,75 = 1,25 mol
Áp dụng định luật bảo toàn khối lượng ta có: mA = mH2 + mCnH2n = 2+14n
→ MA = mA/nA → 23.2,2 = mA/1,25 → mA = 58 → 2 + 14n = 58 → n = 4 → anken là C4H8
Câu 3:
 Xem đáp án
Xem đáp án
Chọn đáp án C
nX = 1,68/22,4 = 0,075 mol; nBr2 = 0,025 mol
n Khí còn lại = 1,12/22,4 = 0,05 mol → nkhí pư với Br2 = nX - n khí còn lại = 0,075 - 0,05 = 0,025 mol
→ nkhí pư với Br2 = nBr2 = 0,025 mol
→ Khí phản ứng với Br2 là anken → nanken = 0,025 mol
Khí còn lại là ankan, nankan = 0,05 mol
nCO2 = 2,8/22,4 = 0,125 mol
→ Đốt cháy hoàn toàn 0,075mol X thì sinh ra 0,125 mol khí CO2
→ Số C trung bình của X là: 0,125/0,075 = 1,67
→ Trong X phải chứa CH4 → nCH4 = 0,05 mol
Bảo toàn nguyên tố C: 0,05.1 + 0,025.n = 0,125 (n là số nguyên tử C trong anken)
→ n = 3 → anken đó là C3H6
Câu 4:
 Xem đáp án
Xem đáp án
Ta thấy thể tích hidrocacbon sau khi tham gia phản ứng cộng H2 không thay đổi, chỉ có thể tích giảm đi là H2 vào Hidrocacbon.
Suy ra: VX = 6,72 lit
Câu 5:
 Xem đáp án
Xem đáp án
Hỗn hợp Y không làm mất màu nước Brom, suy ra Hidrocacbon không no phản ứng hết thành hidrocacbon no, H2 còn dư.
Theo định luật bảo toàn khối lượng ta có:
mX = mY
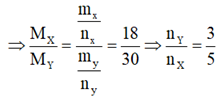
CnH2n + H2 → CnH2n+2
Giả sử số mol Y là 3 mol, số mol của X là 5 mol.
Khi đó số mol X giảm sau phản ứng chính là số mol H2 phản ứng và cũng là số mol của Hidrocacbon.
⇒ nX giảm = 5-3 = 2 mol
⇒ nH2 (bđ) = 5-2 = 3 mol
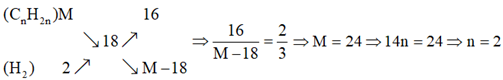
Vậy CTPT của anken là C2H4.
Câu 6:
 Xem đáp án
Xem đáp án
Giả sử hidrocacbon là anken, suy ra sản phẩm là CnH2nBr2.
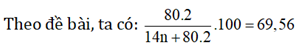
⇒ n = 5 → C5H10
Câu 7:
 Xem đáp án
Xem đáp án
Chọn đáp án B
Tương tự câu 5
Câu 8:
 Xem đáp án
Xem đáp án
Chọn đáp án A
Tương tự câu 5
Câu 9:
 Xem đáp án
Xem đáp án
Chọn đáp án A
Tương tự câu 5
