Đề thi Hóa 9 giữa kì 1 có đáp án (Đề 1)
-
3355 lượt thi
-
9 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Dung dịch H2SO4tác dụng được với chất nào sau đây
 Xem đáp án
Xem đáp án
Đáp án C
Phương trình phản ứng:
H2SO4+ 2NaOH → Na2SO4+ 2H2O
Câu 2:
Trong các oxit sau, oxit không tan trong nước là
 Xem đáp án
Xem đáp án
Đáp án A
MgO không tan trong nước.
P2O5, Na2O tan tốt trong nước còn CO2tan ít trong nước.
Phương trình phản ứng:
P2O5+ 3H2O → 2H3PO4
Na2O + H2O → 2NaOH
CO2+ H2O H2CO3
H2CO3
Câu 3:
Oxit tác dụng được với dung dịch H2SO4là
 Xem đáp án
Xem đáp án
Đáp án C
Phương trình phản ứng:
CuO + H2SO4→ CuSO4+ H2O
Câu 4:
Dãy chất nào sau đây khi nhiệt phân hoàn toàn, sản phẩm thu được chỉ toàn là oxit
 Xem đáp án
Xem đáp án
Đáp án C
Phương trình phản ứng:
+) 4Fe(OH)2+ O2+ 2H2O → 4Fe(OH)3
2Fe(OH)3 Fe2O3+ 3H2O
Fe2O3+ 3H2O
+) 2Al(OH)3 Al2O3+ 3H2O
Al2O3+ 3H2O
Câu 5:
Chất nào sau đây tác dụng với dung dịch Ba(OH)2?
 Xem đáp án
Xem đáp án
Đáp án A
Phương trình phản ứng:
Ba(OH)2 + CO2→ BaCO3↓ + H2O
Câu 6:
Axit sunfuric loãng tác dụng được với dãy chất nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án D
Phương trình phản ứng:
Zn + H2SO4→ ZnSO4+ H2
2NaOH + H2SO4→ Na2SO4+ 2H2O
Na2O + H2SO4→ Na2SO4+ H2O
Câu 7:
Hoàn thành chuỗi biến hóa sau:
CuO CuCl2
CuCl2
 Cu(OH)2
Cu(OH)2 CuSO4
CuSO4 CuCl2
CuCl2
 Xem đáp án
Xem đáp án
Phương trình hóa học:
(1) CuO + 2HCl → CuCl2+ H2O
(2) CuCl2+ 2NaOH → Cu(OH)2↓+ 2NaCl
(3) Cu(OH)2+ H2SO4→ CuSO4+ 2H2O
(4) CuSO4+ BaCl2→ CuCl2+ BaSO4↓
Câu 8:
Bằng phương pháp hóa học hãy nhận biết các dung dịch sau: NaCl, HCl, K2SO4.
 Xem đáp án
Xem đáp án
- Đánh số thứ tự và trích mẫu thử
- Cho quỳ tím vào 3 mẫu thử:
+ Mẫu làm quỳ tím hóa đỏ là HCl
+ Mẫu không làm đổi màu quì tím là NaCl, K2SO4(nhóm I).
- Cho BaCl2vào hai mẫu ở nhóm I:
+ Mẫu tạo kết tủa trắng là K2SO4:
BaCl2+ K2SO4→ BaSO4(↓ trắng)+ 2KCl
+ Mẫu không có hiện tượng gì xuất hiện là NaCl.
Câu 9:
Cho một hỗn hợp 2 muối khan MgCl2 và CaCO3 phản ứng vừa đủ với 400 ml dung dịch HCl. Sau phản ứng thu được 6,72 lít khí CO2(đktc).
a. Viết PTHH xảy ra.
b. Tính nồng độ mol của dung dịch axit đã dùng.
c. Nếu dùng 80 ml dung dịch axit HCl nên trung hòa với 80 ml NaOH 2M thì dung dịch sau phản ứng làm quỳ tím chuyển sang màu gì?
 Xem đáp án
Xem đáp án
a. Phương trình hóa học:
MgCl2+ HCl → Phản ứng không xảy ra
CaCO3+ 2HCl → CaCl2+ CO2+ H2O
b. Ta có: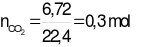
Phương trình phản ứng:

Theo phương trình phản ứng ta có: nHCl= 0,6 mol
Mà VHCl= 400 ml = 0,4 lít
Vậy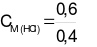 = 1,5 M
= 1,5 M
c. Có VHCl= 80 ml = 0,08 lít
Suy ra nHCl= 0,08.1,5 = 0,12 mol
VNaOH= 80 ml = 0,08 lít
Suy ra nNaOH= 0,08.2 = 0,16 mol
Phương trình hóa học:
HCl + NaOH → NaCl + H2O
Xét tỉ lệ: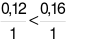
Suy ra NaOH dư, dung dịch sau phản ứng có tính bazơ.
Vậy dung dịch sau phản ứng làm quỳ tím chuyển sang màu xanh.
