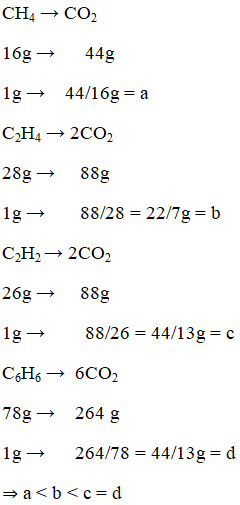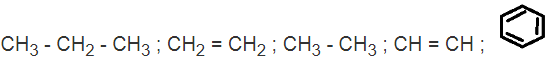Giải SBT Hóa học 9 Bài 39: Benzen
-
1441 lượt thi
-
7 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 2:
Cho benzen vào ống nghiệm đựng dung dịch brom, lắc đều sau đó để yên thấy chất lỏng trong ống nghiệm
 Xem đáp án
Xem đáp án
Đáp án B
Câu 3:
Đốt cháy cùng 1 gam các chất CH4, C2H4, C2H2, C6H6 thu được khí CO2 với khối lượng tương ứng là a, b, c, d gam. Trật tự của a, b, c, d là
 Xem đáp án
Xem đáp án
Đáp án C.
Câu 4:
Đốt cháy hiđrocacbon A, người ta thu được CO2 và H2O theo tỉ lệ mCO2 : mH2O = 44 : 9. Biết A không làm mất màu dung dịch brom.
Hỏi A là hiđrocacbon nào trong số các hiđrocacbon sau ?
CH ≡CH ; CH3 - CH3 ; CH2 = CH - C = CH ; CH2 = CH2 ;
 Xem đáp án
Xem đáp án
Gọi công thức phân tử của A là: CxHy
CxHy → xCO2 + y/2 H2O
Theo đề bài ta có: 44x : 9y = 44 : 9
⇒ x : y = 1 : 1 ⇒ C6H6
Câu 5:
a) Để đốt cháy 0,1 mol benzen cần dùng bao nhiêu lít oxi ở đktc ? Bao nhiêu lít không khí ở đktc ?
b) Từ kết quả trên hãy giải thích tại sao khi benzen cháy trong không khí lại sinh ra nhiều muội than.
 Xem đáp án
Xem đáp án
a) Phản ứng cháy của benzen:
2C6H6 + 15O2 → 12CO2 + 6H2O
nO2 = .nC6H6 = 0,75 mol
VO2 = 0,75 x 22,4 = 16,8l
Nếu dùng không khí thì Vkk = 16,8/20 x 100 = 84l
b) Vậy để đốt cháy 0,1 mol benzen cần một lượng không khí khá lớn nên khi benzen cháy trong không khí thường sinh ra muội than vì thiếu oxi.
Câu 6:
Trong những hiđrocacbon sau, những chất nào có phản ứng thế với brom ? Có phản ứng cộng với brom ? Viết phương trình hoá học minh hoạ và ghi rõ điều kiện phản ứng :
 Xem đáp án
Xem đáp án
Chất có phản ứng thế với brom khi chiếu sáng . CH3-CH2-CH3 ; CH3-CH3.
- Phản ứng thế với brom khi có mặt bột sắt và đun nóng : C6H6 (benzen).
- Chất có phản ứng cộng với brom (trong dung dịch): CH2 = CH2 ; CH ≡CH.
Các chất tham gia phản ứng thế brom:
CH3 – CH2 – CH3 + Br2 as→ CH3-CHCl – CH3 (spc)+CH3 – CH2 – CH2Cl(spp) + HCl
CH3 – CH3 + Br2 as→ CH3 – CH2Br + HBr
C6H6 + Br2 Bột Fe, t°→ C6H5Br + HBr
Phản ứng cộng:
C2H2 + 2Br2 → C2H2Br4
Câu 7:
Khi có mặt bột sắt, benzen phản ứng với clo tương tự như phản ứng với brom. Hãy tính lượng clobenzen thu được khi cho 15,6 gam benzen tác dụng với clo dư khi có mặt bột Fe và đun nóng. Biết hiệu suất phản ứng đạt 80%.
 Xem đáp án
Xem đáp án
Phương trình hoá học của phản ứng giữa benzen và clo
C6H6 + Cl2 to→ C6H5Cl + HCl
Theo phương trình hoá học : số mol C6H6 = số mol C6H5Cl.
Vì hiệu suất 80% và clo dư nên số mol clobenzen thu được là :
nC6H5Cl = 15,6/78 x 80/100 = 0,16mol
=> mC6H5Cl = 0,16 x 112,5 = 18g