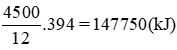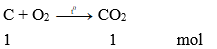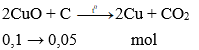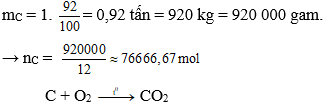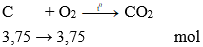Giải SGK Hóa học 9 Chương 3: Phi kim. Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Bài 27: Cacbon
-
5040 lượt thi
-
15 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Dạng thù hình của nguyên tố là gì? Cho hai ví dụ.
 Xem đáp án
Xem đáp án
– Dạng thù hình của nguyên tố là những đơn chất khác nhau do cùng một nguyên tố hóa học tạo nên.
– Một nguyên tố hóa học có thể tạo ra hai hay nhiều đơn chất. Ví dụ:
Cacbon có ba dạng thù hình: kim cương, than chì, cacbon vô định hình.
Photpho có ba dạng thù hình: photpho trắng, photpho đỏ và photpho đen.
Câu 2:
Viết phương trình hóa học của cacbon với các oxit sau:
a) CuO.
b) PbO.
c) CO2.
d) FeO.
Hãy cho biết loại phản ứng: vai trò của C trong các phản ứng, ứng dụng của các phản ứng đó trong sản xuất.
 Xem đáp án
Xem đáp án
Phương trình hóa học của phản ứng:
a) 2CuO + C 
b) 2PbO + C 
c) CO2 + C 
d) 2FeO + C 
Trong các phản ứng trên cacbon là chất khử.
– Ứng dụng của cacbon:
Tùy thuộc vào tính chất mỗi dạng thù hình, người ta sử dụng cacbon trong đời sống, sản xuất, kĩ thuật.
– Ví dụ: Than chì được dùng làm điện cực, chất bôi trơn, ruột bút chì. Kim cương dùng làm đồ trang sức, mũi khoan, sao cắt hình.
Than đá, than gỗ được dùng làm nhiên liệu trong công nghiệp, chất khử để điều chế một số kim loại kém hoạt động.
Câu 3:
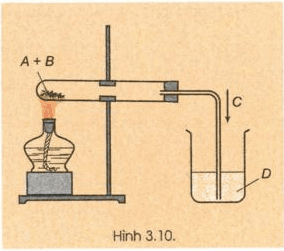
Hãy xác định công thức hóa học thích hợp của A, B, C, D trong thí nghiệm ở hình vẽ bên.
Nêu hiện tượng thí nghiệm và viết phương trình hóa học.
 Xem đáp án
Xem đáp án
Công thức hóa học thích hợp của các chất:
A: CuO;
B: C (cacbon);
C: CO2;
D: dung dịch Ca(OH)2.
Khí CO2 sinh ra làm vẩn đục nước vôi trong và tạo kết tủa CaCO3.
Phương trình hóa học của các phản ứng:
2CuO + C 
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O.
Câu 4:
Tại sao sử dụng than để đun nấu, nung gạch ngói, nung vôi gây ô nhiễm môi trường. Hãy nêu biện pháp chống ô nhiễm môi trường và giải thích.
 Xem đáp án
Xem đáp án
Khi đốt cháy than làm cho lượng oxi giảm đồng thời sản phẩm sinh ra là khí CO2, CO, SO2 gây độc cho con người, gây mưa axit, hiệu ứng nhà kính, nên có ảnh hưởng rất lớn đến sức khỏe con người. Do đó, nên xây lò ỏ những khu xa dân cư, thoáng mát, đồng thời tăng cường trồng cây xanh để giúp hấp thụ khí CO2 và giải phóng khí oxi.
Câu 5:
Trong công nghiệp, người ta sử dụng cacbon để làm nhiên liệu. Tính nhiệt lượng tỏa ra khi đốt cháy 5kg than đá chứa chứa 90% cacbon, biết rằng 1 mol cacbon cháy thì tỏa ra 394kJ.
 Xem đáp án
Xem đáp án
Khối lượng cacbon: 5 x 90% = 4,5 (kg)
1 mol C (12g) khi đốt cháy tỏa ra 394 (kJ)
Vậy 4,5kg = 4500g C khi đốt cháy tỏa ra x (kJ).
Nhiệt lượng tỏa ra khi đốt cháy 5kg là:
Câu 10:
Dãy oxit phản ứng với cacbon ở nhiệt độ cao tạo thành đơn chất kim loại là
 Xem đáp án
Xem đáp án
Đáp án: B
C khử được oxit của các kim loại đứng sau Al trong dãy hoạt động hóa học thành kim loại.
Câu 11:
Để có thể nhận biết 3 lọ mất nhãn, mỗi lọ đựng một chất rắn màu đen là: bột than, bột đồng (II) oxit và bột mangan đioxit, ta dùng
 Xem đáp án
Xem đáp án
Đáp án: A
Sử dụng dung dịch HCl đặc, nóng.
+ Chất rắn tan dần, có khí màu vàng lục, mùi xốc thoát ra → mangan đioxit (MnO2)
+ Chất rắn tan dần, sau phản ứng thu được dung dịch màu xanh → đồng (II) oxit (CuO)
CuO + 2HCl → CuCl2 (xanh) + H2O
+ hông có hiện tượng gì xuất hiện → cacbon.
Câu 12:
Đốt cháy hoàn toàn 12 gam C thì thể tích tối đa của khí CO2 thu được ở đktc là
 Xem đáp án
Xem đáp án
Đáp án: D
Số mol cacbon: nC = 12 : 12 = 1 mol
→ Thể tích CO2: V = 1.22,4 = 22,4 lít.
Câu 13:
Khối lượng C cần dùng để khử hoàn toàn 8 gam CuO thành kim loại là
 Xem đáp án
Xem đáp án
Đáp án: D
Số mol CuO: nCuO = 8 : 80 = 0,1 mol
→ mC pư = 0,05.12 = 0,6 gam.
Câu 14:
Thể tích cacbon đioxit (đktc) thu được khi đốt cháy hoàn toàn 1 tấn than chứa 8% tạp chất là
 Xem đáp án
Xem đáp án
Đáp án: A
%C có trong than là 100% - 8% = 92%
Khối lượng C có trong 1 tấn than là:
→ VCO2 = nCO2.22,4 = nC.22,4
= 76 666,67.22,4 = 1717333,408 lít ≈ 1717,33 m3.
Câu 15:
Đốt cháy hoàn toàn 45g cacbon cần dùng V lít không khí (đktc). Biết Vkk = 5VO2 và sản phẩm tạo thành chỉ có cacbonđioxit.
 Xem đáp án
Xem đáp án
Đáp án: C
Số mol cacbon: nC = 45 : 12 = 3,75 mol
Thể tích khí O2 cần dùng: VO2 = 3,75.22,4 = 84 lít
→ Thể tích không khí cần dùng: Vkk = 5.84 = 420 lít.