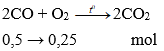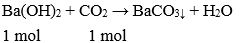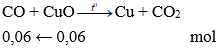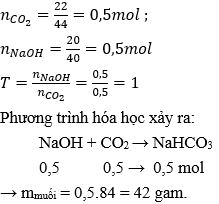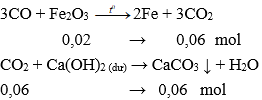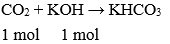Giải SGK Hóa học 9 Chương 3: Phi kim. Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Bài 28: Các oxit của cacbon
-
5038 lượt thi
-
15 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Hãy viết phương trình hóa học của CO với: a) Khí O2; b) CuO.
Cho biết: loại phản ứng, điều kiện phản ứng, vai trò của CO và ứng dụng của mỗi phản ứng đó.
 Xem đáp án
Xem đáp án
a) 2CO + O2 
b) CO + CuO 
- Điều kiện phản ứng: nhiệt độ cao.
- Vai trò của CO: là chất khử.
- Ứng dụng: phản ứng (1) CO cháy và tỏa nhiều nhiệt dùng trong các lò luyện gang, thép.
Phản ứng (2) ở điều kiện nhiệt độ cao khử oxit CuO tạo kim loại Cu (điều chế Cu)
Câu 2:
Hãy viết phương trình hóa học của CO2 với dung dịch NaOH, dung dịch Ca(OH)2 trong trường hợp:
a) Tỉ lệ số mol n : n = 1 : 1
b) Tỉ lệ số mol n : n = 2 : 1
 Xem đáp án
Xem đáp án
Phương trình hóa học của CO2 với:
a) Dung dịch NaOH theo tỉ lệ nCO2 : nNaOH = 1 : 1
CO2 + NaOH → NaHCO3
b) Dung dịch Ca(OH)2 theo tỉ lệ nCO2 : nCa(OH)2 = 2 : 1.
2CO2 + Ca(OH)2 → Ca(HCO3)2↓.
Câu 3:
Có hỗn hợp hai khí CO và CO2. Nêu phương pháp hóâ học để chứng minh sự có mặt của hai khí đó. Viết các phương trình hóa học.
 Xem đáp án
Xem đáp án
– Cho hỗn hợp khí lội qua bình chứa dung dịch nước vôi trong, nếu nước vôi trong vẩn đục, chứng tỏ trong hỗn hợp khí có khí CO2.
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
- Khí đi ra khỏi bình nước vôi trong được dẫn qua ống thủy tinh đựng CuO nung nóng, nếu thấy có kim loại màu đỏ sinh ra và khí sinh ra khỏi ống thủy tinh làm vẩn đục nước vôi trong thì chứng tỏ trong hỗn hợp đó có khí CO.
CO + CuO → Cu + CO2.
Câu 4:
Trên bề mặt hồ nước tôi vôi lâu ngày thường có lớp màng chất rắn. Hãy giải thích hiện tượng này và viết phương trình hóa học.
 Xem đáp án
Xem đáp án
Do Ca(OH)2 tác dụng với khí CO2 trong không khí tạo nên lớp CaCO3 rất mỏng trên bề mặt nước vôi.
Ca(OH)2 + CO2 → CaCO3 ↓ + H2O.
Câu 5:
Hãy xác định thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp CO và CO2, biết các số liệu thực nghiệm sau:
– Dẫn 16 lít hỗn hợp CO và CO2 qua nước vôi trong dư thu được khí A.
– Để đốt cháy A cần 2 lít khí oxi. Các thể tích khí đo được ở cùng điều kiện nhiệt độ và áp suất.
 Xem đáp án
Xem đáp án
Dẫn hỗn hợp khí CO và CO2 qua nước vôi trong dư thu được khí A là khí CO, trong cùng điều kiện về nhiệt độ, áp suất thì tỉ lệ thể tích cũng bằng tỉ lệ về số mol.
Phương trình phản ứng đốt cháy khí A:
2CO + O2 → 2CO2.
Từ phương trình trên ta nhận thấy: nCO = 2.nO2
⇒ VCO = 2.VO2 = 2. 2 = 4 lít. (tỉ lệ mol cũng chính là tỉ lệ thể tích)
Từ phương trình trên ta nhận thấy: VCO = 4 lít.
Vậy VCO2 = 16 – 4 = 12 lít.
% VCO2 = 12 /16 x 100% = 75 %;
%VCO = 100% – 75% = 25%.
Câu 7:
Phản ứng nào sau đây là sai?
 Xem đáp án
Xem đáp án
Đáp án: D
CO chỉ khử được oxit của những kim loại đứng sau nhôm trong dãy hoạt động hóa học.
Câu 8:
Đốt cháy 11,2 lít CO (đktc). Thể tích không khí cần cho phản ứng trên là
 Xem đáp án
Xem đáp án
Đáp án: D
Số mol CO: nCO = 11,2 : 22,4 = 0,5 mol
Thể tích oxi cần dùng: Voxi = 0,25.22,5 = 5,6 lít
→ Thể tích không khí cần dùng: Vkk = 5,6.5 = 28 lít.
Câu 11:
Khử hoàn toàn 4,8 gam đồng (II) oxit bằng khí CO. Thể tích khí CO cần dùng (đktc) là
 Xem đáp án
Xem đáp án
Đáp án: A
Số mol CuO là: nCuO = 4,8 : 80 = 0,06 mol
→ VCO pư = 0,06.22,4 = 1,344 lí
Câu 12:
Người ta dùng 22 gam CO2 hấp thụ 20 gam NaOH. Khối lượng muối tạo thành là
 Xem đáp án
Xem đáp án
Đáp án: D
Ta có:
Câu 13:
Khử hoàn toàn 3,2 gam Fe2O3 bằng khí CO dư. Sản phẩm khí thu được cho vào bình đựng nước vôi trong dư được a gam kết tủa màu trắng. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án: B
Số mol Fe2O3 là 3,2 : 160 = 0,02 mol
Phương trình hóa học:
Vậy a = 0,06.100 = 6 gam.
Câu 14:
Khí CO dùng làm chất đốt trong công nghiệp có lẫn tạp chất là CO2 và SO2. Có thể làm sạch CO bằng
 Xem đáp án
Xem đáp án
Đáp án: D
Cho hỗn hợp khí qua lượng dư nước vôi trong; CO2 và SO2 phản ứng với nước vôi trong bị giữ lại; CO không phản ứng thoát ra khỏi dung dịch thu được CO tinh khiết.
CO2 + Ca(OH)2 (dư) → CaCO3 ↓ + H2O
SO2 + Ca(OH)2 (dư) → CaSO3 ↓ + H2O