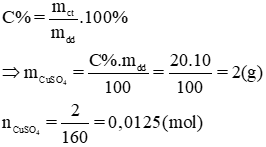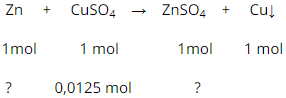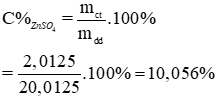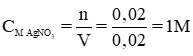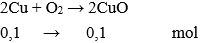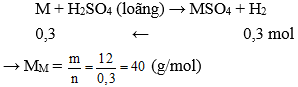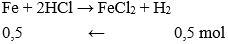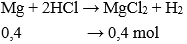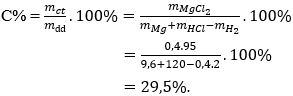Bài 16: Tính chất hóa học của kim loại
-
4968 lượt thi
-
17 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Kim loại có những tính chất hóa học nào? Lấy ví dụ và viết các phương trình hóa học minh họa với kim loại magie.
 Xem đáp án
Xem đáp án
Kim loại có những tính chất hóa học chung:
1. Phản ứng của kim loại với phi kim:
2Mg + O2 → 2MgO
Mg + Cl2 → MgCl2
2. Phản ứng của kim loại với dung dịch axit:
Mg + 2HCl → MgCl2 + H2 ↑
Mg + H2SO4loãng → MgSO4 + H2 ↑
3. Phản ứng của kim loại với dung dịch muối:
Mg + CuSO4 → MgSO4 + Cu.
Câu 2:
Hãy hoàn thành các phương trình hóa học sau đây:
a) ... + HCl -⇒ MgCl2 + H2
b) ... + AgNO3 ⇒ Cu(NO3)2 + Ag
c) ... + ... ⇒ ZnO
d) ... + Cl2 ⇒ HgCl2
e) ... + S ⇒ K2S.
 Xem đáp án
Xem đáp án
Phương trình hóa học:
a) Mg + 2HCl → MgCl2 + H2 ↑
b) Cu + 2AgNO3 → Cu(NO3)2 + 2Ag ↓
c) 2Zn + O2 → 2ZnO
d) Hg + Cl2 → HgCl2
e) 2K + S → K2S.
Câu 3:
Viết các phương trình hóa học xảy ra giữa các cặp chất sau đây:
a) Kẽm + axit sunfuric loãng.
b) Kẽm + dung dịch bạc nitrat.
c) Natri + lưu huỳnh.
d) Canxi + clo.
 Xem đáp án
Xem đáp án
Các phương trình phản ứng hóa học:
a) Zn + H2SO4loãng → ZnSO4 + H2 ↑
b) Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
c) 2Na + S → Na2S
d) Ca + Cl2 → CaCl2.
Câu 4:
Dựa vào tính chất hóa học của kim loại, hãy viết các phương trình hóa học biểu diễn các chuyển hóa sau đây:
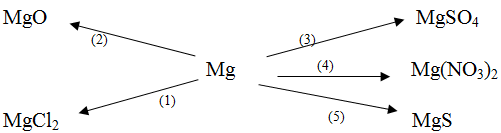
 Xem đáp án
Xem đáp án
(1) Mg + Cl2 → MgCl2
(2) 2Mg + O2 → 2MgO
(3) Mg + H2SO4loãng → MgSO4 + H2 ↑
(4) Mg + 2AgNO3 → Mg(NO3)2 + 2Ag ↓
(5) Mg + S → MgS
Câu 5:
Dự đoán hiện tượng và viết phương trình hóa học xảy ra, khi:
a) Đốt dây sắt trong khí clo.
b) Cho một đinh sắt vào trong ống nghiệm đựng dung dịch CuCl2.
c) Cho một viên kẽm vào dung dịch CuSO4.
 Xem đáp án
Xem đáp án
a) Khối màu nâu tạo thành:
2Fe + 3Cl2 → 2FeCl3
b) Dung dịch CuCl2 nhạt màu xanh, kim loại màu đỏ bám vào đinh sắt.
Fe + CuCl2 → FeCl2 + Cu ↓
c) Zn tan dần, dung dịch CuSO4 nhạt màu xanh, kim loại màu đỏ bám vào viên kẽm.
Zn + CuSO4 → ZnSO4 + Cu ↓
Câu 6:
Ngâm một lá kẽm trong 20g dung dịch muối đồng sunfat 10% cho đến khi phản ứng kết thúc. Tính khối lượng kẽm đã phản ứng với dung dịch trên và nồng độ phần trăm của dung dịch sau phản ứng.
 Xem đáp án
Xem đáp án
Theo pt: nZn = nCuSO4 = 0,0125 mol → mZn = 0,0125. 65 = 0,8125 (g)
nZnSO4 = 0,0125 mol → mZnSO4 = 0,0125. 161 = 2,0125 (g)
Theo pt nCu = nCuSO4 = 0,0125 mol ⇒ mCu= 64. 0,0125 = 0,8g
mdd sau phản ứng = mZn + mCuSO4 - mCu = 0,8125 + 20 – 0,8 = 20,0125g
Câu 7:
Ngâm một lá đồng trong 20 ml dung dịch bạc nitrat cho tới khi đồng không thể tan thêm được nữa. Lấy lá đồng ra, rửa nhẹ, làm khô và cân thì thấy khối lượng lá đồng tăng thêm 1,52 g. Hãy xác định nổng độ mol của dung dịch bạc nitrat đã dùng (giả thiết toàn bộ lượng bạc giải phóng bám hết vào lá đồng).
 Xem đáp án
Xem đáp án
PTHH: Cu + 2AgNO3 → Cu(NO3)2 + 2Ag ↓
Gọi x là số mol Cu phản ứng
Theo phương trình ta có: nAg sinh ra = 2nCu pư = 2x mol
Khối lượng lá đồng tăng thêm 1,52g ⇒ mAg sinh ra – mCu pư = 1,52
⇒ 108. 2x – 64x = 1,52 ⇒ x = 0,01 (mol)
Theo pt nAgNO3 = 2.nCu = 2. 0,01 = 0,02 mol
Nồng độ dung dịch AgNO3:
Câu 8:
Đơn chất tác dụng với dung dịch H2SO4 loãng giải phóng khí hiđro là:
 Xem đáp án
Xem đáp án
Đáp án: C
Zn + H2SO4 (loãng) → ZnSO4 + H2
Câu 9:
Dung dịch FeCl2 có lẫn tạp chất là CuCl2 có thể dùng kim loại nào sau đây để làm sạch dung dịch FeCl2 trên:
 Xem đáp án
Xem đáp án
Đáp án: B
Sử dụng một lượng dư kim loại Fe
Fe + CuCl2 → FeCl2 + Cu↓
Lọc bỏ kết tủa thu được dung dịch FeCl2 tinh khiết.
Câu 11:
Các kim loại tác dụng được với nước ở nhiệt độ thường tạo thành dung dịch kiềm và giải phóng khí hidro:
 Xem đáp án
Xem đáp án
Đáp án: A
Câu 12:
Lấy một ít bột Fe cho vào dung dịch HCl vừa đủ rồi nhỏ từ từ dung dịch NaOH đến dư vào dung dịch. Hiện tượng xảy ra là:
 Xem đáp án
Xem đáp án
Đáp án: C
Fe + 2HCl → FeCl2 + H2↑
FeCl2 + 2NaOH → Fe(OH)2 (↓ trắng xanh) + 2NaCl
4Fe(OH)2 (↓) + O2 + 2H2O → 4Fe(OH)3 (↓ nâu đỏ)
Câu 14:
Nung 6,4g Cu ngoài không khí thu được 6,4g CuO. Hiệu suất phản ứng là:
 Xem đáp án
Xem đáp án
Đáp án: B
nCu = 6,4 : 64 = 0,1 mol
Khối lượng CuO theo lý thuyết tạo thành là : mCuO = 0,1.80 = 8 gam.
Hiệu suất phản ứng (tính theo CuO) là:
Câu 15:
Hoà tan hết 12g một kim loại ( hoá trị II) bằng dung dịch H2SO4 loãng thu được 6,72 lít khí H2 (đktc). Kim loại này là:
 Xem đáp án
Xem đáp án
Đáp án: C
Gọi kim loại là M, tính được nkhí = 6,72 : 22,4 = 0,3 mol
Vậy kim loại cần tìm là Ca.
Câu 16:
Cho vào dung dịch HCl một cây đinh sắt , sau một thời gian thu được 11,2 lít khí hiđro (đktc). Khối lượng sắt đã phản ứng là:
 Xem đáp án
Xem đáp án
Đáp án: A
nkhí = 11,2 : 22,4 = 0,5 mol
→ mFe = 0,5.56 = 28 gam.
Câu 17:
Cho 9,6 gam kim loại Magie vào 120 gam dung dịch HCl (vừa đủ). Nồng độ phần trăm của dung dịch sau phản ứng là:
 Xem đáp án
Xem đáp án
Đáp án: B
nMg = 9,6 : 24 = 0,4 mol
Dung dịch sau phản ứng chứa MgCl2: 0,4 mol