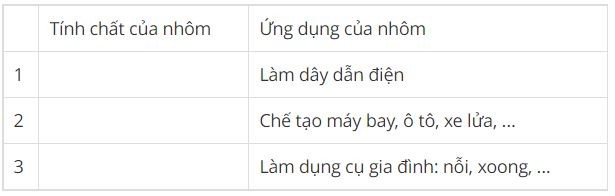
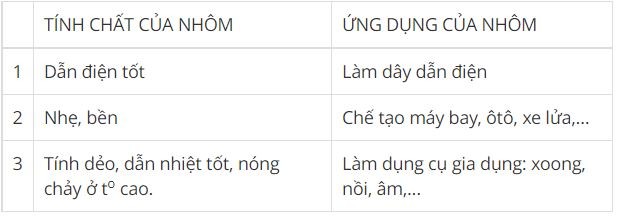
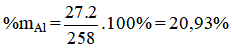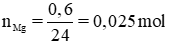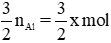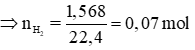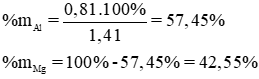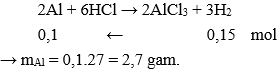Bài 18: Nhôm
-
4973 lượt thi
-
16 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 2:
Thả một mảnh nhôm vào các ống nghiệm chứa các dung dịch sau:
a) MgSO4.
b) CuCl2.
c) AgNO3.
d) HCl.
Cho biết hiện tượng xảy ra? Giải thích và viết phương trình hóa học.
 Xem đáp án
Xem đáp án
a) Không có phản ứng, vì hoạt động hóa học của Mg > Al.
b) Al tan dần, màu xanh lam của dung dịch nhạt dần, có chất rắn màu đỏ bám vào bề mặt nhôm.
2Al + 3CuCl2 → 2AlCl3 + 3Cu ↓
c) Al tan dần, có chất rắn màu xám bám ngoài Al.
Al + 3AgNO3 → Al(NO3)3 + 3Ag ↓
d) Có khí hiđro bay lên:
2Al + 6HCl → 2AlCl3 + 3H2 ↑ .
Câu 3:
Có nên dùng xô, chậu, nồi nhôm để đựng vôi, nước vôi tôi hoặc vữa xây dựng không? Giải thích.
 Xem đáp án
Xem đáp án
Nếu dùng xô, chậu, nồi nhôm để đựng vôi, nước vôi hoặc vữa thì
Các dụng cụ này sẽ bị chóng hư vì trong vôi, nước vôi hoặc vữa đều có chứa Ca(OH)2 là một chất kiềm nên tác dụng được với Al2O3 (vỏ bọc ngoài các đồ dùng bằng nhôm), sau đó đến Al bị ăn mòn.
Phương trình phản ứng:
Al2O3 + Ca(OH)2 → Ca(AlO2)2 + H2O
2Al + Ca(OH)2 + 2H2O → Ca(AlO2)2 + 3H2 ↑ .
Câu 4:
Có dung dịch muối AlCl3 lẫn tạp chất là CuCl2. Có thể dùng chất nào sau đây để làm sạch muối nhôm? Giải thích sự lựa chọn.
a) AgNO3.
b) HCl.
c) Mg.
d) Al.
e) Zn.
 Xem đáp án
Xem đáp án
d) Dùng Al để làm sạch muối nhôm vì:
2Al + 3CuCl2 → 2AlCl3 + 3Cu ↓
Câu 5:
Thành phần chính của đất sét là Al2O3.2SiO2.2H2O. Hãy tính thành phần phần trăm theo khối lượng của Al có trogn hợp chất trên.
 Xem đáp án
Xem đáp án
M Al2O3. 2SiO2. 2H2O = 27.2 + 16.3 + 2.(28 + 16.2) + 2.(2 + 16) = 258 (g)
Câu 6:
Để xác định phần trăm khối lượng của hỗn hợp A gồm nhôm và magie, người ta thực hiện hai thí nghiệm sau:
– Thí nghiệm 1: Cho m gam hỗn hợp A tác dụng với dung dịch H2SO4 loãng dư, thu được 1568ml khí ở điều kiện tiêu chuẩn.
– Thí nghiệm 2: Cho m gam hỗn hợp A tác dụng với dung dịch NaOH dư thì sau phản ứng thấy còn lại 0,6g chất rắn.
Tính phần trăm khối lượng của mỗi chất trong hỗn hợp A.
 Xem đáp án
Xem đáp án
Ở thí nghiệm 2: Al tác dụng hết với NaOH, còn Mg không phản ứng nên khối lượng chất rắn còn lại là Mg, mMg = 0,6g.
Gọi nAl = x
Phương trình phản ứng:
2Al + 3H2SO4 → Al2(SO4)3 + 3H2 ↑ ( 1)
Mg + H2SO4 → MgSO4 + H2 ↑ (2)
Theo pt (2) nH2 (2) = nMg = 0,025 mol
Theo pt (1) nH2 (1) =
⇒ Tổng số mol H2 là 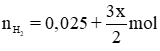
Theo đề bài ta có: VH2 = 1568ml = 1,568 l
Từ (∗) và (∗∗) ⇒ 0,025 + 3x/2 = 0,07
Giải ra ta có : x = 0,03 mol ⇒ mAl = 0,03 x 27 = 0,81g
mhỗn hợp A = 0,81 + 0,6 = 1,41 g
Câu 8:
Người ta có thể dát mỏng được nhôm thành thìa, xoong, chậu, giấy gói bánh kẹo là do nhôm có tính:
 Xem đáp án
Xem đáp án
Đáp án: A
Câu 11:
Thả một mảnh nhôm vào ống nghiệm chứa dung dịch CuSO4. Xảy ra hiện tượng:
 Xem đáp án
Xem đáp án
Đáp án: C
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
→ Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
Câu 14:
Cặp chất nào dưới đây có phản ứng?
 Xem đáp án
Xem đáp án
Đáp án: C
2Al + 6HCl → 2AlCl3 + 3H2
A và B sai vì Nhôm không tác dụng với H2SO4 đặc nguội và HNO3 đặc, nguội,
D sai vì Fe đứng sau Al trong dãy hoạt động hóa học của kim loại.
Câu 15:
Cho 10,8 g một kim loại M (hóa trị III) phản ứng với khí clo tạo thành 53,4g muối. Kim loại M là:
 Xem đáp án
Xem đáp án
Đáp án: C
2M + 3Cl2 → 2MCl3
Câu 16:
Cho lá nhôm vào dung dịch axit HCl có dư thu được 3,36 lít khí hiđro (ở đktc). Khối lượng nhôm đã phản ứng là :
 Xem đáp án
Xem đáp án
Đáp án: B.
Ta có: nkhí = 3,36 : 22,4 = 0,15 mol