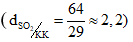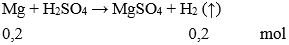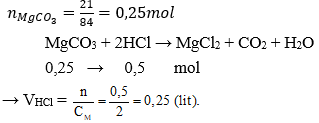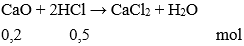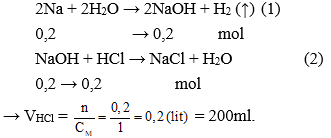Bài 3 : Tính chất hóa học của axit
-
5717 lượt thi
-
14 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Từ Mg, MgO, Mg(OH)2 và dung dịch axit sunfuric loãng, hãy viết các phương trình phản ứng hóa học điều chế magie sunfat.
 Xem đáp án
Xem đáp án
Phương trình hóa học:
Mg + H2SO4(loãng) → MgSO4 + H2
MgO + H2SO4 → MgSO4 + H2O
Mg(OH)2 + H2SO4 → MgSO4 + 2H2O
Câu 2:
Có những chất sau: CuO, Mg, Al2O3, Fe(OH)3, Fe2O3. Hãy chọn một trong những chất đã cho tác dụng với dung dịch HCl sinh ra:
a) Khí nhẹ hơn không khí và cháy được trong không khí.
b) Dung dịch có màu xanh lam.
c) Dung dịch có màu vàng nâu.
d) Dung dịch không có màu.
Viết các phương trình phản ứng.
 Xem đáp án
Xem đáp án
a) Khí nhẹ hơn không khí và cháy được trong không khí là khí H2.
Mg + 2HCl → MgCl2 + H2 ↑
b) Dung dịch có màu xanh lam là dung dịch CuCl2.
CuO + 2HCl → CuCl2 + H2O
c) Dung dịch có màu vàng nâu là dung dịch FeCl3.
Fe(OH)3 + 3HCl → FeCl3 + 3H2O
Hoặc Fe2O3 + 6HCl → 2FeCl3 + 3H2O
d) Dung dịch không màu là các dung dịch MgCl2, AlCl3.
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mg + 2HCl → MgCl2 + H2 ↑
Câu 3:
Hãy viết các phương trình phản ứng trong mỗi trường hợp sau:
a) Magie oxit và axit nitric.
b) Đồng (II) oxit và axit clohiđric.
c) Nhôm oxit và axit sunfuric.
d) Sắt và axit clohiđric.
e) Kẽm và axit sunfuric loãng.
 Xem đáp án
Xem đáp án
Phương trình hóa học của các phản ứng:
a) MgO + 2HNO3 → Mg(NO3)2 + H2O
b) CuO + 2HCl → CuCl2 + H2O
c) Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
d) Fe + 2HCl → FeCl2 + H2 ↑
e) Zn + H2SO4(loãng) → ZnSO4 + H2 ↑.
Câu 4:
Có 10g hỗn hợp bột các kim loại đồng và sắt. Hãy giới thiệu phương pháp xác định thành phần phần trăm (theo khối lượng) của mỗi kim loại trong hỗn hợp theo:
a) Phương pháp hóa học. Viết phương trình hóa học.
b) Phương pháp vật lí.
(Biết rằng đồng không tác dụng với axit HCl và axit H2SO4 loãng).
 Xem đáp án
Xem đáp án
a) Phương pháp hóa học:
- Ngâm hỗn hợp Cu và Fe trong dung dịch HCl dư.
- Phản ứng xong, lọc lấy chất rắn, rửa nhiều lần trên giấy lọc.
- Làm khô chất rắn, thu được bột Cu.
- Cân, giả sử ta cân được 7,2g. Từ đó suy ra trong hỗn hợp có 7,2g Cu và
10-7,2= 2,8g Fe
⇒ % Cu = (7,2/10).100% = 72% và % Fe = 100% - 72% = 28%
PTHH: Fe + 2HCl → FeCl2 + H2↑
Cu + HCl → không phản ứng.
b) Phương pháp vật lí:
Dùng thanh nam châm, sau khi đã bọc đầu nam châm bằng mảnh nilon mỏng và nhỏ. Chà nhiều lần trên hỗn hợp bột ta cũng thu được 2,8g bột Fe.
Câu 5:
Chất tác dụng với dung dịch HCl tạo thành chất khí nhẹ hơn không khí là
 Xem đáp án
Xem đáp án
Đáp án: A
Mg + 2HCl → MgCl2 + H2 ↑
Khí H2 nhẹ hơn không khí.
Câu 6:
Dãy gồm các kim loại tác dụng được với dung dịch H2SO4 loãng là:
 Xem đáp án
Xem đáp án
Đáp án: C
Cu, Ag không phản ứng với H2SO4 loãng → đáp án C thỏa mãn.
Câu 7:
Dãy oxit tác dụng với dung dịch HCl tạo thành muối và nước là
 Xem đáp án
Xem đáp án
Đáp án: C
Oxit bazơ + axit → muối + nước
CuO, Na2O, CaO là oxit bazơ (thỏa mãn).
Câu 8:
Chất phản ứng được với dung dịch HCl tạo ra một chất khí có mùi hắc, nặng hơn không khí và làm đục nước vôi trong:
 Xem đáp án
Xem đáp án
Đáp án: B
Na2SO3 + 2HCl → 2NaCl + SO2 ↑ + H2O
SO2 là khí có mùi hắc, nặng hơn không khí
SO2 làm đục nước vôi trong theo phản ứng:
SO2 + Ca(OH)2 → CaSO3↓ + H2O
Câu 9:
MgCO3 tác dụng với dung dịch HCl sinh ra:
 Xem đáp án
Xem đáp án
Đáp án: B
MgCO3 + 2HCl → MgCl2 + CO2 ↑ + H2O
CO2 là khí không cháy, không duy trì sự cháy, sư sống.
Khí CO2 tan ít trong nước và làm đục nước vôi trong theo phản ứng:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Câu 10:
Cho phản ứng: BaCO3 + 2X → H2O + Y + CO2
X và Y lần lượt là:
 Xem đáp án
Xem đáp án
Đáp án: B
BaCO3 + 2HCl → BaCl2 + CO2 + H2O
Câu 11:
Cho 4,8 gam kim loại magie tác dụng vừa đủ với dung dịch axit sunfuric loãng. Thể tích khí Hiđro thu được ở đktc là:
 Xem đáp án
Xem đáp án
Đáp án: B
nMg = 4,8 : 24 = 0,2 mol
→ Vkhí = 0,2.22,4 = 4,48 lít.
Câu 12:
Cho 21 gam MgCO3 tác dụng với một lượng vừa đủ dung dịch HCl 2M.
Thể tích dung dịch HCl đã dùng là:
 Xem đáp án
Xem đáp án
Đáp án: B
Câu 13:
Cho 0,2 mol Canxi oxit tác dụng với 500ml dung dịch HCl 1M. Khối lượng muối thu được là:
 Xem đáp án
Xem đáp án
Đáp án: B
nHCl = 0,5.1 = 0,5 mol
Có 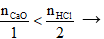
Theo PTHH có số mol muối = số mol CaO = 0,2 mol
→ mmuối = 0,2. (40 + 71) = 22,2 gam.
Câu 14:
Hòa tan hết 4,6 gam Na vào H2O được dung dịch X. Thể tích dung dịch HCl 1M cần để phản ứng hết với dung dịch X là:
 Xem đáp án
Xem đáp án
Đáp án: B
nNa = 4,6 : 23 = 0,2 mol
Các PTHH xảy ra: