Đề kiểm tra giữa học kì 2 môn Hoá 9 có đáp án (Mới nhất) (Đề 14)
-
5431 lượt thi
-
19 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Muối trung hòa là muối mà trong gốc axit không có nguyên tử H có thể thay thế bằng nguyên tử kim loại.
Các muối trung hòa là: BaCO3, Na2CO3, CaCO3, MgCO3, K2CO3.
Câu 2:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
Câu 3:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
%C (CH4) = .100 = 75%
%C (C4H8) = .100 = 85,71%
%C (C2H2) = .100 = 92, 31%
%C (C5H10) == 85,71%
Vậy C2H2 có hàm lượng cacbon cao nhất.
Câu 4:
Bạn Minh cầm bảng hệ thống tuần hoàn các nguyên tố hóa học đến thắc mắc với Mai. Không biết cấu tạo bảng tuần hoàn gồm bao nhiêu chu kì, bao nhiêu nhóm?
Là Mai, Em hãy nói cho bạn Minh biết cấu tạo bảng tuần hoàn các nguyên tố hóa học gồm:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Cấu tạo bảng tuần hoàn các nguyên tố hóa học gồm: 7 chu kì và 8 nhóm.
Câu 5:
Đốt cháy hoàn toàn 4,48 lít khí etilen sinh ra CO2 và H2O. Tính thể tích khí oxi cần dùng? Biết các thể tích khí đo ở điều kiện tiêu chuẩn.
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
netilen = = 0,2 (mol)
C2H4 + 3O2 2CO2 + 2H2O
Theo phương trình phản ứng:= 3netilen = 3.0,2 = 0,6 (mol)
= 0,6.22,4 = 13,44 (l)
Câu 6:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Nhiên liệu là những chất cháy được và tỏa nhiều nhiệt.
Câu 7:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Hiđrocacbon là những hợp chất hữu cơ mà phân tử chỉ có hai nguyên tố cacbon và hiđro.
Vậy các hiđrocacbon là: C6H6, C5H12, C4H8, C2H6, C2H2; C5H10; CH4, C3H4.
Câu 8:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Nguyên tố A có số hiệu nguyên tử là 15, chu kì 3, nhóm V trong bảng hệ thống tuần hoàn.
Nguyên tố A nằm ở ô số 15, chu kì 3, nhóm V trong bảng hệ thống tuần hoàn.
Vậy A là photpho (P)
Câu 9:
Cho sơ đồ phản ứng sau: CH4 + Cl2 A + HCl
Công thức phân tử của A là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Metan phản ứng với khí clo khi được chiếu sáng theo phương trình hóa học sau:
CH4 + Cl2 CH3Cl + HCl
Câu 10:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Etilen đã phản ứng với brom trong dung dịch tạo ra sản phẩm không màu.
CH2 = CH2 + Br2Br – CH2 – CH2 – Br
Vậy hiện tượng quan sát được là dung dịch brom bị mất màu.
Câu 11:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Để sử dụng nhiên liệu có hiệu quả cần phải cung cấp đủ không khí hoặc oxi vừa đủ cho quá trình cháy để đảm bảo an toàn và tiết kiệm.
Câu 12:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Trạng thái khí là trạng thái dễ cháy nhất của chất.
Câu 13:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Khi than cháy tạo ra rất nhiều khí CO, CO2. Nếu đun bếp than trong phòng kín nồng độ khí CO sinh ra quá mức cho phép. Khí CO kết hợp với hemoglobin trong máu ngăn không cho máu nhận oxi và cung cấp oxi cho các tế bào và do đó gây tử vong cho con người.
Câu 14:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
... + CH2 = CH2 + CH2 = CH2 + ... ... – CH2 – CH2 – CH2 – CH2 - ...
Sản phẩm trùng hợp etilen là polietilen (viết tắt là PE).
Câu 15:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Những nguyên tử cacbon trong phân tử hợp chất hữu cơ có thể liên kết trực tiếp với nhau tạo thành mạch vòng, mạch thẳng, mạch nhánh.
Câu 16:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
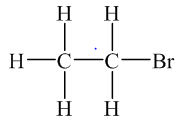
Dựa vào công thức cấu tạo ta thấy hợp chất này có 2 nguyên tử C, 5 nguyên tử H và 1 nguyên tử Br.
Vậy công thức cấu tạo trên là của hợp chất: C2H5Br.
Câu 17:
 Xem đáp án
Xem đáp án
Để nhận biết bốn chất khí C2H4, CH4, Cl2, CO2 ta có thể tiến hành các thí nghiệm sau:
Dẫn các khí trên qua dung dịch brom, khí nào làm mất màu dung dịch brom là C2H4
CH2 = CH2 + Br2Br – CH2 – CH2 – Br
Ba khí còn lại không làm mất màu dung dịch brom là CH4, Cl2, CO2
Dẫn ba khí còn lại vào cốc đựng nước rồi nhúng mẩu giấy quỳ tím vào dung dịch thu được.
Trường hợp nào giấy quỳ tím chuyển sang màu đỏ, sau đó mất màu ngay là khí Cl2.
Cl2 + H2OHCl + HClO
Trường hợp nào giấy quỳ tím chuyển sang màu đỏ nhạt là khí CO2.
CO2 + H2OH2CO3
Trường hợp còn lại không làm đổi màu quỳ tím là CH4
Câu 18:
Hoàn thành các phương trình hóa học sau, ghi rõ điều kiện phản ứng (nếu có).
1, CH4 + ?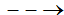 HCl + ?
HCl + ?
2, Zn + HCl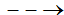 ? + ?
? + ?
3, CH2 = CH2 + Br2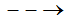 ?
?
4, CaCO3 + ? CaCl2 + ? + H2O
CaCl2 + ? + H2O
 Xem đáp án
Xem đáp án
1, CH4 + Cl2 HCl + CH3Cl
2, Zn + 2HClZnCl2 + H2
3, CH2 = CH2 + Br2Br – CH2 – CH2 – Br
4, CaCO3 + 2HClCaCl2 + CO2 + H2O
Câu 19:
Cho 2,8 lít hỗn hợp metan và etilen (đktc) lội qua dung dịch brom (dư), người ta thu được 4,7 gam đibrometan.
a) Viết phương trình phản ứng xảy ra.
b) Tính thành phần phần trăm của hỗn hợp theo thể tích.
 Xem đáp án
Xem đáp án
a) CH2 = CH2 + Br2Br – CH2 – CH2 – Br (1)
b) nKhí == 0,125 (mol)
= = 0,025 (mol)
Theo phương trình phản ứng (1): = = 0,025 (mol)
= nKhí - = 0,125 – 0,025 = 0,1 (mol)
= 0,1.22,4 = 2,24 (l)
= 0,025.22,4 = 0,56 (l)
% = .100 = 80%
% = 100% - % = 100% - 80% = 20%
