Bộ 30 đề thi vào 10 Chuyên Hóa năm 2022-2023 có lời giải chi tiết ( Đề 25)
-
9455 lượt thi
-
13 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Tổng số hạt (proton, electron và notron) trong nguyên tử nguyên tố M là 80. Trong đó, số hạt không mang điện gấp 1,2 lần số hạt mang điện âm. Xác định số hiệu nguyên tử của nguyên tố M.
Câu 2:
Viết các phương trình hóa học xảy ra và nêu hiện tượng khi:
a) Trộn dung dịch NaHCO3 với dung dịch hỗn hợp KOH và Ba(NO3)2
 Xem đáp án
Xem đáp án
a)
Phương trình hóa học:
Hiện tượng: Xuất hiện kết tủa trắng, lượng kết tủa tăng dần đến cực đại.
Câu 3:
b) Sục khí SO2 dư vào dung dịch brom, thu được dung dịch X. Sau đó thêm tiếp vào X một lượng dư dung dịch BaCl2
 Xem đáp án
Xem đáp án
b) Phương trình hóa học
Hiện tượng: Sục dư SO2 vào dung dịch Br2 thì dung dịch Br2 nhạt màu dần rồi mất màu. Thêm vào X một lượng dư dung dịch BaCl2 thì dung dịch xuất hiện kết tủa trắng, lượng kết tủa tăng dần đến cực đại.
Câu 4:
c) Cho mẩu Na vào dung dịch FeCl3
 Xem đáp án
Xem đáp án
c) Phương trình hóa học
Hiện tượng: Mẩu Na tan dần, có khí không màu, không mùi thoát ra. Đồng thời tạo kết tủa màu nâu đỏ.
Câu 5:
Chỉ dùng 1 thuốc thử hãy phân biệt 4 dung dịch sau đây bằng phương pháp hóa học: KCl, NH4NO3, Ca(H2PO4)2, (NH4)2SO4
 Xem đáp án
Xem đáp án
- Lấy mẫu thử, đánh dấu tương ứng.
- Trộn lần lượt từng mẫu thử với dung dịch Ba(OH)2 dư:
+ Có khí mùi khai thoát ra: NH4NO3
+ Có kết tủa xuất hiện trắng: Ca(H2PO4)2
+ Vừa xuất hiện kết tủa trắng, vừa có khí mùi khai thoát ra: (NH4)2SO4
+ Không xuất hiện kết tủa hay khí: KCl
Câu 6:
Cho sơ đồ biến hóa sau:
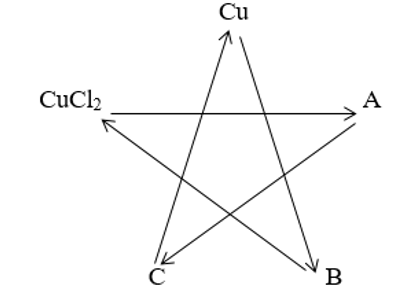
Hãy xác định các chất A, B, C rồi hoàn thành các phản ứng.
 Xem đáp án
Xem đáp án
A: FeCl2
B: CuO
C: Fe
Phương trình hóa học:
Câu 7:
 Xem đáp án
Xem đáp án
Theo định luật bảo toàn khối lượng:
Ta có phương trình hóa học:
Câu 8:
Cho 24,48 gam hỗn hợp X gồm (Fe, Zn, Al) tác dụng với dung dịch HCl dư thu được 0,54 mol khí H2. Mặt khác, 0,24 mol X tác dụng vừa đủ với 0,33 mol khí clo (nung nóng). Xác định khối lượng mỗi kim loại trong 24,48 gam X.
 Xem đáp án
Xem đáp án
Đặt số mol của Fe, Zn, Al trong 24,48 gam hỗn hợp X lần lượt là a, b, c
Ta có phương trình hóa học
Có 0,24 mol X tác dụng vừa đủ với 0,33 mol khí Cl2 nung nóng
⇒ số mol Cl2 cần để phản ứng hết với hỗn hợp X gấp 1,375 lần số mol hỗn hợp X
Ta có:
Từ (1), (2), (3)
a = 0,24 ⇒ mFe = 13,44 g
b = 0,12 ⇒ mZn = 7,8 g
c = 0,12 ⇒ mAl = 3,24 g
Câu 9:
Hòa tan 14,2 gam hỗn hợp A gồm MgCO3 và muối cacbonat của kim loại R bằng lượng vừa đủ dung dịch HCl 7,3% thu được dung dịch D và 3,36 lít khí CO2(ở đktc). Thêm 32,4 gam nước vào dung dịch D được dung dịch E. Nồng độ của MgCl2 trong dung dịch E là 5%.
Xác định kim loại R và tính thành phần % theo khối lượng của mỗi chất trong hỗn hợp A.
 Xem đáp án
Xem đáp án
Đặt công thức tổng quát của muối cacbonat kim loại là: R2(CO3)n n ![]() {1;2;3}
{1;2;3}
Đặt số mol của MgCO3 và R2(CO3)n lần lượt là: a, b (mol) với a, b > 0
Hòa tan hỗn hợp A vào dung dịch HCl, ta có phương trình hóa học:
Suy ra:
bn = 0.05
MR = 28n
Xét bảng
|
n |
1 |
2 |
3 |
|
MR |
28 |
56 |
84 |
|
|
Loại |
Chọn |
Loại |
Suy ra R là Fe
Câu 10:
Dung dịch X chứa 0,1 mol NaHCO3 và 0,2 mol Na2CO3. Thêm dung dịch chứa 0,32 mol Ca(OH)2 vào X. Viết các phương trình phản ứng xảy ra và tính khối lượng kết tủa tạo thành.
 Xem đáp án
Xem đáp án
Phương trình hóa học
Nếu muối trong dung dịch X còn dư thì :
Bảo toàn nguyên tố Cacbon ta có:
Mà
Suy ra Ca(OH)2 dư
Vậy khối lượng kết tủa tạo thành là 0,3.100 = 100 gam.
Câu 11:
Hợp chất hữu cơ X chứa các nguyên tố C,H,O. Đốt cháy hoàn toàn 9,25 gam X, sau đó dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch nước vôi trong dư thu được 37,5 gam kết tủa và khối lượng dung dịch giảm 14,25 gam so với khối lượng dung dịch nước vôi trong ban đầu. Biết tỉ khối hơi của X so với khí oxi bằng 2,3125. Xác định công thức phân tử của chất X.
 Xem đáp án
Xem đáp án
Bảo toàn nguyên tố H:
g/mol
Gọi công thức phân tử của A là
Ta có: x : y : z = 0,375 : 0,75 : 0,25 = 3 : 6 : 2
⇒ Công thức đơn giản của A: (C3H6O2)n
Ta có: 74.n = 74 ⇒ n = 1Vậy CTPT của A: C3H6O2
Câu 12:
Trộn a gam rượu với b gam axit được hỗn hợp X. Chia X làm 2 phần bằng nhau:
- Phần 1: Tác dụng với Na dư, sau khi phản ứng kết thúc thu được 0,07 mol H2.
- Phần 2: Đốt cháy hoàn toàn bởi oxi vừa đủ thu được 0,22 mol CO2 và 0,28 mol H2O.
a) Xác định công thức cấu tạo của hai chất trong hỗn hợp X.
 Xem đáp án
Xem đáp án
Phần 1:
Theo phương trình có
Phần 2:
Theo phương trình:
Vì m nguyên, m
Xét bảng:
|
m |
0 |
1 |
|
n |
2,33 |
1 |
|
|
Loại |
Chọn |
Vậy rượu là CH3OH
axit là CH3COOH
