Bộ 30 đề thi vào 10 Chuyên Hóa năm 2022-2023 có lời giải chi tiết ( Đề 12)
-
9446 lượt thi
-
28 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Hoà tan hỗn hợp A gồm các chất: Na2O, NaHCO3, NH4Cl, BaCl2 có số mol mỗi chất bằng nhau vào nước dư. Sau phản ứng, đun nóng để khí bay ra hết thu được khí X, dung dịch Y và kết tủa M. Xác định các chất tan trong Y và viết các phương trình phản ứng xảy ra.
 Xem đáp án
Xem đáp án
Các phương trình hóa học minh họa:
Na2O + H2O → 2NaOH
NaOH + NaHCO3 → Na2CO3 + H2O
NaOH + NH4Cl → NaCl + NH3↑ + H2O
Na2CO3 + BaCl2 2NaCl + BaCO3↓.
Chất tan Y là NaCl
Câu 2:
Nguyên tử của nguyên tố R có tổng số hạt proton, nơtron và electron là 18, trong đó số hạt mang điện gấp đôi số hạt không mang điện.
a. Xác định tên gọi của R.
 Xem đáp án
Xem đáp án
a.
Gọi số proton trong R là Z → số electron trong R là Z.
Gọi số nơtron trong R là N.
Ta có hệ phương trình:
Vậy R là carbon.
Câu 3:
b. Nung nóng đỏ R rồi dẫn hơi nước đi qua thì thu được hỗn hợp gồm khí Z và khí T (trong đó Z là khí độc). Ở nhiệt độ cao, Z và T đều khử được oxit sắt từ thành kim loại. Xác định công thức của Z, T và viết phương trình phản ứng xảy ra.
 Xem đáp án
Xem đáp án
b.
Z là CO, T là H2. Các phương trình hóa học minh họa :
C + H2O CO + H2
4CO + Fe3O4 3Fe + 4CO2
4H2 + Fe3O4 3Fe + 4H2O
Câu 4:
Nêu hiện tượng và viết phương trình phản ứng xảy ra trong các quá trình sau:
a. Nhỏ từ từ đến dư dung dịch H2SO4 vào dung dịch Ba(OH)2 có nhỏ sẵn vài giọt phenolphtalein.
 Xem đáp án
Xem đáp án
a.
Hiện tượng: Xuất hiện kết tủa trắng, màu đỏ của dung dịch nhạt dần rồi mất màu
Phương trình hóa học:
H2SO4 + Ba(OH)2 → BaSO4↓ + H2O
Câu 5:
b. Cho dung dịch KOH vào dung dịch FeSO4 rồi để ống nghiệm ngoài không khí.
 Xem đáp án
Xem đáp án
b.
Hiện tượng: Xuất hiện kết tủa màu trắng xanh, sau một thời gian kết tủa chuyển dần sang màu nâu đỏ.
Phương trình hóa học:
2KOH + FeSO4 → K2SO4 + Fe(OH)2↓
4Fe(OH)2↓ + O2 + 2H2O → 4Fe(OH)3↓
Câu 6:
 Xem đáp án
Xem đáp án
CuO + H2SO4 → CuSO4 + H2O
0,2 → 0,2 → 0,2 mol
Giả sử có x mol CuSO4.5H2O tách ra:
Vậy m = 30,75 gam
Câu 7:
Cho các chất rắn sau: BaSO4, CH3COONa, Ba(HSO3)2, NaHCO3.
a. Chất nào không thể điều chế bằng cách cho kiềm tác dụng với oxit axit?
 Xem đáp án
Xem đáp án
a. CH3COONa không được điều chế bằng cách cho kiềm tác dụng với oxit axit.
Câu 8:
b. Chất nào tác dụng với dung dịch axit HCl tạo khí gây hiệu ứng nhà kính? Viết phương trình phản ứng.
 Xem đáp án
Xem đáp án
b. NaHCO3 tác dụng với HCl tạo khí gây hiệu ứng nhà kính (CO2).
Phương trình hóa học:
HCl + NaHCO3 → NaCl + CO2 + H2O.
Câu 9:
c. Chỉ dùng một thuốc thử, hãy phân biệt bốn chất trên bằng các phản ứng hóa học.
 Xem đáp án
Xem đáp án
c. Phân biệt: BaSO4, CH3COONa, Ba(HSO3)2, NaHCO3 bằng thuốc thử H2SO4.
Hiện tượng:
+ BaSO4 không tan, không hiện tượng.
+ CH3COONa tan.
H2SO4 + 2CH3COONa → 2CH3COOH + Na2SO4
+ NaHCO3 tan, có khí thoát ra.
H2SO4 + 2NaHCO3 → Na2SO4 + 2CO2 + 2H2O
+ Ba(HSO3)2 sau phản ứng có khí thoát ra, có kết tủa tạo thành.
H2SO4 + Ba(HSO3)2 → BaSO4↓ + 2SO2↑ + 2H2O
Câu 10:
Một học sinh làm thí nghiệm với ba chiếc đinh sắt có kích thước như nhau, chiếc thứ nhất để ngoài không khí, chiếc thứ 2 ngâm trong dầu hỏa (thành phần chính là các hiđrocacbon), chiếc thứ 3 ngâm trong dung dịch muối ăn.
Em hãy dự đoán thứ tự về tốc độ ăn mòn của ba chiếc đinh sắt và đề xuất biện pháp bảo vệ vật làm bằng sắt, thép đối với sự ăn mòn.
 Xem đáp án
Xem đáp án
Thứ tự tốc độ ăn mòn tăng dần: chiếc đinh 2 < chiếc đinh 1 < chiếc đinh 3
Một số biện pháp chống ăn mòn các đồ dụng vật dụng bằng thép:
- Sơn, mạ lên bề mặt kim loại.
- Bôi dầu mỡ lên bề mặt kim loại.
- Chế tạo hợp kim ít ăn mòn.
Câu 11:
Cho m gam hỗn hợp các muối MgSO4, CuSO4 và BaSO4 trong đó lưu huỳnh chiếm 19,07% về khối lượng vào nước được dung dịch A và một phần không tan có khối lượng 9,32 gam. Nhúng thanh nhôm (dư) vào dung dịch A. Sau phản ứng khối lượng thanh kim loại tăng 4,14 gam. Tính m.
 Xem đáp án
Xem đáp án
Phần không tan là BaSO4 → = 0,04 mol
Gọi số mol CuSO4 và MgSO4 lần lượt là x và y (mol)
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
Câu 12:
Đốt một lượng sắt trong oxi sau một thời gian thu được m gam chất rắn X gồm Fe, FeO, Fe2O3, Fe3O4. Hòa tan X vào 200 ml dung dịch H2SO4 1M đến phản ứng hoàn toàn thì thu được 1,12 lít khí H2, còn lại 2,8 gam kim loại chưa tan. Tính m.
 Xem đáp án
Xem đáp án
Vì sau phản ứng Fe cón dư nên sản phẩn chỉ có FeSO4, H2 và H2O
- Bảo toàn nguyên tố S:
- Bảo toàn nguyên tố H:
- Bảo toàn nguyên tố O:
Vậy m = mFe + mO = 0,2.56 + 0,15.16 + 2,8 = 16,4 gam
Câu 13:
Công thức đơn giản nhất của một chất hữu cơ cho biết tỷ lệ nguyên, tối giản số nguyên tử của các nguyên tố trong hợp chất. Ví dụ: Buten có công thức phân tử là C4H8 thì công thức đơn giản nhất là CH2. Hiđrocacbon A mạch hở, có công thức phân tử trùng với công thức đơn giản nhất, tỉ lệ khối lượng giữa hiđro và cacbon trong A là 1 : 5.
a. Xác định công thức phân tử của A.
 Xem đáp án
Xem đáp án
a.
Gọi công thức A là CxHy, ta có:
Vậy A là C5H12
Câu 14:
b. Bậc của mỗi nguyên tử cacbon trong phân tử hợp chất hữu cơ là số nguyên tử cacbon liên kết trực tiếp với nguyên tử cacbon đó. Biết trong mỗi phân tử A có một nguyên tử cacbon bậc IV, viết công thức cấu tạo của A.
 Xem đáp án
Xem đáp án
b. Công thức cấu tạo của A:
Câu 15:
c. A có tính chất hóa học tương tự metan. Viết phương trình phản ứng của A với Cl2 theo tỉ lệ mol 1:1.
 Xem đáp án
Xem đáp án
c. Phương trình hóa học:
C(CH3)4 + Cl2 (CH3)3C-CH2Cl + HCl
Câu 16:
Sơ đồ dưới đây mô tả thí nghiệm điều chế khí X từ đất đèn:
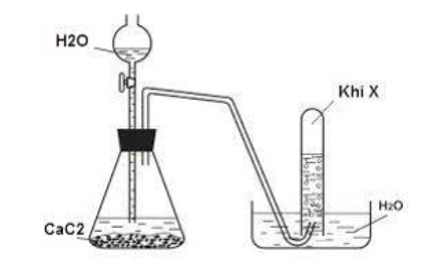
a. Xác định công thức cấu tạo, tên gọi của X, viết phương trình phản ứng điều chế trong thí nghiệm.
 Xem đáp án
Xem đáp án
a.
Công thức cấu tạo của X: CH ≡ CH (tên gọi: axetilen).
Phương trình điều chế axetilen (C2H2 trong phòng thí nghiệm):
CaC2 + 2H2O → Ca(OH)2 + C2H2↑
Câu 17:
b. Khí X có khả năng làm mất màu nước brom. Khi cháy trong oxi tỏa nhiều nhiệt nên được dùng để hàn, cắt kim loại. Viết phương trình phản ứng của X với dung dịch brom dư và phản ứng đốt cháy X.
 Xem đáp án
Xem đáp án
b. Phản ứng của axetilen với Br2:
CH ≡ CH + 2Br2 → CHBr2 – CHBr2
Phản ứng đốt cháy C2H2:
2C2H2 + 5O2 4CO2 + 2H2O
Câu 18:
c. Đất đèn ngoài thành phần chính là CaC2 còn có thêm tạp chất, khi thực hiện phản ứng trên thường sinh ra H2S là khí rất độc, có mùi khó chịu. Em hãy nêu giải pháp loại bỏ H2S trước khi thu khí X.
 Xem đáp án
Xem đáp án
c. Để loại bỏ H2S, người ta dẫn hỗn hợp khí qua bình đựng lượng dư dung dịch kiềm.
H2S + Ca(OH)2 dư → CaS + 2H2O
Câu 19:
d. Trong điều kiện thích hợp, X cũng có phản ứng cộng hiđro và một số chất khác. Thực hiện phản ứng cộng hỗn hợp gồm 0,15 mol X và 0,3 mol H2 trong bình kín có xúc tác thích hợp thì thu được hỗn hợp Y gồm hiđro, chất X, một hiđrocacbon chứa liên kết đôi trong phân tử và một hiđrocacbon chỉ chứa liên kết đơn có tính chất tương tự metan. Tỉ khối của Y so với H2 là 5,625. Dẫn Y qua dung dịch brom dư thì có m gam brom phản ứng. Tính m.
 Xem đáp án
Xem đáp án
d.
CH ≡ CH + H2 CH2 = CH2
CH ≡ CH + 2H2 CH3 – CH3
Hỗn hợp Y gồm: H2, CH ≡ CH , CH2 = CH2, CH3 – CH3.
Các phản ứng khi Y tác dụng với dung dịch brom:
CH ≡ CH + 2Br2 → CHBr2 – CHBr2
CH2 = CH2 + Br2 → CH2Br – CH2Br
Gọi số mol C2H2; C2H4 và C2H6 trong Y lần lượt là x, y và z (mol)
Bảo toàn khối lượng có:
0,15.26 + 0,3.2 = nY.11,25 suy ra nY = 0,4 mol
Lại có:
= 0,15 – y – z
⇒ 2x + y = 0,25 = nbrom
Vậy khối lượng brom là 40 gam.
Câu 20:
Glucozơ là một cacbohiđrat quan trọng, có nhiều ứng dụng như làm thuốc tăng lực cho người già, trẻ em, người ốm, là nguyên liệu phản ứng tráng gương, sản xuất rượu etylic…
a. Tính % khối lượng của nguyên tố oxi trong glucozơ.
 Xem đáp án
Xem đáp án
a)
Câu 21:
b. Viết các phương trình phản ứng theo sơ đồ chuyển hóa sau:
glucozơ → rượu etylic → axit axetic → etyl axetat
 Xem đáp án
Xem đáp án
b. Các phương trình hóa học xảy ra theo sơ đồ chuyển hóa:
C6H12O6 2C2H5OH + 2CO2
C2H5OH + O2 CH3COOH + H2O
CH3COOH + C2H5OH CH3COOC2H5 + H2O
Câu 22:
c. Thực hiện lên men glucozơ với hiệu suất quá trình đạt 75%. Tính thể tích rượu etylic (lit) thu được từ 90kg glucozơ. Biết khối lượng riêng của rượu etylic nguyên chất là 0,8 g/ml.
 Xem đáp án
Xem đáp án
c.
C6H12O6 2C2H5OH + 2CO2
- m glucozơ phản ứng =
-
Câu 23:
Các axit cacboxilic no đơn chức, mạch hở là các chất có chứa nhóm COOH trong phân tử và có tính chất hóa học tương tự nhau (axit axetic là một trong các chất này). Hỗn hợp A gồm hai axit cacboxilic no đơn chức mạch hở X, Y có công thức lần lượt là CnH2nO2 và CmH2mO2 (n + 2 = m). Cho a gam hỗn hợp A tác dụng với lượng dư dung dịch NaHCO3 thì thu được 6,72 lít khí CO2. Đốt cháy hoàn toàn a gam A rồi dẫn toàn bộ sản phẩm cháy chỉ gồm CO2 và hơi nước qua bình 1 đựng P2O5 khan, dư, sau đó qua bình 2 đựng 400 gam dung dịch NaOH x%. Sau khi phản ứng xảy ra hoàn toàn thấy khối lượng bình 1 tăng 14,4 gam, bình 2 được dung dịch B có chứa 88,8 gam chất tan và không thấy có khí thoát ra (giả thiết lượng khí chưa phản ứng không hòa tan trong dung dịch).
a. Xác định công thức phân tử, tính phần trăm khối lượng mỗi axit trong A.
 Xem đáp án
Xem đáp án
a.
Cho hỗn hợp axit phản ứng với NaHCO3:
RCOOH + NaHCO3 → RCOONa + CO2↑ + H2O
Theo PTHH có nA = nkhí = 0,3 mol
Đốt cháy hỗn hợp axit:
2CnH2nO2 + (3n - 2) O2 → 2nCO2 + 2nH2O
⇒ 0,3.n = 0,8
Trường hợp 1: Hai axit là HCOOH (a mol) và C2H5COOH (b mol)
Vậy %mHCOOH = 11,06%;
Trường hợp 2: Hai axit là CH3COOH (x mol) và C3H7COOH (y mol)
Ta có hệ phương trình:
Vậy
Câu 24:
b. Tính x.
 Xem đáp án
Xem đáp án
b.
Có
Giả sử 0,8 mol CO2 khi tác dụng với NaOH tạo hết muối Na2CO3 thì khối lượng muối thu được tối đa là 84,8 gam. Nếu tạo hết muối NaHCO3 thì khối lượng muối thu được tối đa là 67,2 gam.
Nếu có tạo thành NaHCO3 thì khối lượng muối < 84,8 gam
Vì khối lượng chất tan trong dung dịch là 88,8 > 84,8 nên dung dịch có Na2CO3 và NaOH dư. Phương trình hóa học:
CO2 + 2NaOH Na2CO3 + H2O
Từ PTHH có:
mNaOH dư = 88,8 – 0,8.106 = 4 gam.
→ nNaOH dư = 0,1 mol; vậy nNaOH ban đầu = 1,7 mol
Câu 25:
Biến thiên entanpi chuẩn của một phản ứng hóa học, kí hiệu là ∆rHo298, chính là nhiệt tỏa ra hay thu vào kèm theo phản ứng đó ở điều kiện chuẩn. Nếu giá trị ∆rHo298 < 0 thì phản ứng tỏa nhiệt, nếu giá trị ∆rHo298 > 0 thì phản ứng thu nhiệt. Khi các chất trong phản ứng đều là chất khí, có thể tính ∆rHo298 bằng cách lấy tổng năng lượng liên kết (Eb) của các chất phản ứng trừ đi tổng năng lượng liên kết (Eb) của các chất sản phẩm. Cho giá trị trung bình của một số năng lượng liên kết ở điều kiện chuẩn:
|
Liên kết |
C-H |
C-C |
C=C |
C≡C |
|
Eb (kJ/mol) |
418 |
346 |
612 |
837 |
a. Tính giá trị ∆rHo298 cho phản ứng CH3-CH2-CH3 (k) → CH4 (k) + CH2=CH2 (k) và nhận định phản ứng tỏa nhiệt hay thu nhiệt? Biết các chất phản ứng và các sản phẩm đều ở thể khí.
 Xem đáp án
Xem đáp án
a. Ta có:
∆rHo298 = 8.418 + 2.346 – 8.418 – 612 = 80 kJ > 0
Vậy phản ứng thu nhiệt
Câu 26:
b. Một loại gas (khí hóa lỏng) chứa hỗn hợp propan (C3H8) và butan (C4H10) với tỉ lệ mol 1 : 2.
Cho biết giá trị ∆rHo298 (lượng chất tham gia phản ứng tính theo mol) của các phản ứng:
|
C3H8 (k) + O2 (k) → 3CO2 (k) + 4H2O (l) C4H10 (k) + O2 (k) → 4CO2 (k) + 5H2O (l) |
∆rHo298 = -2220 kJ ∆rHo298 = -2874 kJ |
Xác định lượng nhiệt tỏa ra khi đốt cháy hoàn toàn 12 kg khí gas trên ở điều kiện chuẩn.
Trung bình mỗi ngày, một hộ gia đình cần đốt gas để cung cấp 10.000 kJ nhiệt (hiệu suất hấp thụ nhiệt là 80%). Sau bao nhiêu ngày hộ gia đình trên sẽ sử dụng hết bình gas 12 kg?
 Xem đáp án
Xem đáp án
b.
-Tính được: = 75 mol, = 150 mol
-Lượng nhiệt: 75.(-2220) + 150.(-2874) = 597600 kJ
-Thời gian sử dụng là: = 47,8 ngày.
Câu 27:
c. Từ ý nghĩa của hiệu ứng nhiệt của phản ứng, em hãy lí giải ngắn gọn tại sao người ta khuyến cáo không nên bón phân đạm cho lúa vào buổi sáng sớm hay những ngày quá rét?
 Xem đáp án
Xem đáp án
c.
Vì quá trình hòa tan của phân đạm thu nhiệt làm nhiệt độ giảm, vào buổi sớm hay quá rét làm nhiệt độ giảm sâu gây hại cho lúa.
Câu 28:
Độ tan của một chất trong nước là số gam chất đó hòa tan trong 100 gam nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định. Thông thường, độ tan của chất rắn tăng còn độ tan của chất khí giảm khi nhiệt độ tăng. Đồ thị dưới đây thể hiện sự thay đổi độ tan của một số chất tan theo nhiệt độ (ký hiệu các chất là X1, X2, X3, X4):
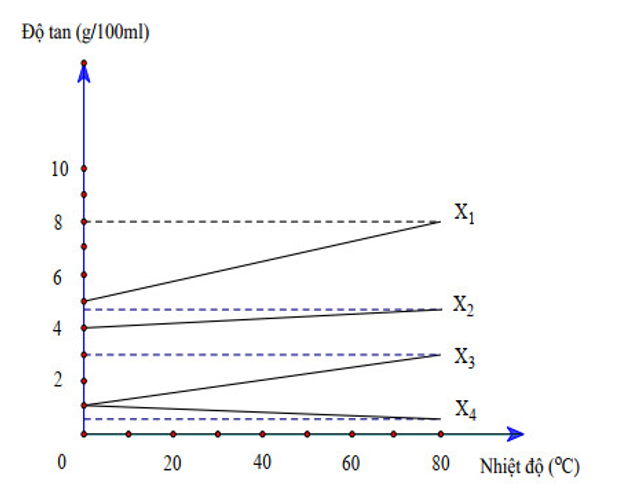
Các dung dịch X1, X2, X3, X4 đang đạt trạng thái bão hòa ở 80oC, nếu hạ nhiệt độ xuống 0oC thì phần trăm khối lượng chất tách ra khỏi dung dịch so với khối lượng chất tan ban đầu của chất nào là lớn nhất ? Giải thích.
 Xem đáp án
Xem đáp án
Từ đồ thị ta có thể ước lượng được phần trăm chất tách ra của các chất:
X4 không tách ra
Nên X3 là chất có tỷ lệ tách ra cao nhất
