Trắc nghiệm Bài 17. Biến thiên enthapy trong các phản ứng hóa học có đáp án
Trắc nghiệm Bài 17. Biến thiên enthapy trong các phản ứng hóa học có đáp án
-
703 lượt thi
-
15 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Phản ứng tỏa nhiệt là gì?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
Câu 2:
Phản ứng thu nhiệt là gì?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt.
Câu 3:
Phản ứng nào sau đây là phản ứng thu nhiệt?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Các phản ứng: tôi vôi, đốt than củi, đốt nhiên liệu đều giải phóng năng lượng dưới dạng nhiệt ra môi trường ⇒ Là phản ứng tỏa nhiệt.
Phản ứng phân hủy đá vôi cần cung cấp nhiệt để phản ứng xảy ra, ngừng cung cấp nhiệt phản ứng sẽ dừng lại ⇒ Là phản ứng thu nhiệt.
Câu 4:
Nhiệt lượng tỏa ra hay thu vào của một phản ứng ở một điều kiện xác định được gọi là gì?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Biến thiên enthalpy của phản ứng là nhiệt lượng tỏa ra hay thu vào của một phản ứng ở một điều kiện xác định.
Câu 5:
Điều kiện chuẩn của biến thiên enthalpy là?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Biến thiên enthapy chuẩn là nhiệt tỏa ra hai thu vào của phản ứng được xác định ở điều kiện chuẩn: áp suất 1 bar (đối với chất khí), nồng độ 1 mol/L (đối với chất tan trong dung dịch) và nhiệt độ là 25oC (298K).
Câu 6:
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Giá trị tuyệt đối của biến thiên enthalpy càng lớn thì nhiệt lượng tỏa ra hay thu vào của phản ứng càng nhiều.
Câu 7:
Kí hiệu của nhiệt tạo thành chuẩn là?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Nhiệt tạo thành ⧍fH của một chất là biến thiên enthalpy của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền vững nhất, ở một điều kiện xác định.
Nhiệt tạo thành chuẩn ( ) là nhiệt tạo thành ở điều kiện chuẩn.
Câu 8:
Đơn vị của nhiệt tạo thành chuẩn là?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Đơn vị của nhiệt tạo thành chuẩn là kJ/mol.
Câu 9:
Phát biểu nào sau đây là sai?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Nhiệt tạo thành chuẩn của các đơn chất ở dạng bền vững nhất bằng không.
Câu 10:
Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết khi các chất ở trạng thái nào?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết khi các chất đều ở thể khí.
Câu 12:
Xác định biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn:
biết nhiệt tạo thành của CH4(g) là -74,9 kJ/mol, của CO2(g) là - 393,5 kJ/mol, của H2O(l) là -285,8 kJ/mol.
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Tổng nhiệt tạo thành các chất đầu là:
Tổng nhiệt tạo thành các chất sản phẩm là:
Biến thiên enthalpy của phản ứng là:
.
Câu 13:
Tính biến thiên enthalpy chuẩn của phản ứng:
Biết Eb (H-H) = 436 kJ/mol, Eb (C-H) = 418 kJ/mol, Eb (C-C) = 346 kJ/mol, Eb (C=C) = 612 kJ/mol.
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
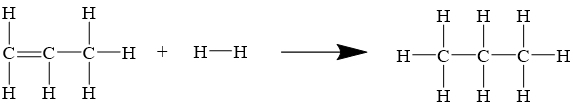
Câu 14:
Công thức nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Biểu thức tính biến thiên enthalpy ở điều kiện chuẩn theo nhiệt tạo thành là:
Câu 15:
Công thức tính biến thiên enthalpy của phản ứng theo năng lượng liên kết đúng là?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Biểu thức tính biến thiên enthalpy ở điều kiện chuẩn theo năng lượng liên kết (các chất đều ở thể khí) là: .
