Trắc nghiệm Hóa học 10 Bài 5. Cấu tạo bảng tuần hoàn các nguyên tố hóa học có đáp án
Trắc nghiệm Hóa học 10 Bài 5. Cấu tạo bảng tuần hoàn các nguyên tố hóa học có đáp án
-
562 lượt thi
-
15 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Năm 1869, nhà hóa học đã công bố bảng tuần hoàn các nguyên tố hóa học là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Năm 1869, nhà hóa học đã công bố bảng tuần hoàn các nguyên tố hóa học là Mendeleev.
Câu 2:
Theo bảng tuần hoàn của Mendeleev, các nguyên tố được sắp xếp theo thứ tự tăng dần
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Theo bảng tuần hoàn của Mendeleev, các nguyên tố được sắp xếp theo thứ tự tăng dần khối lượng nguyên tử.
Câu 3:
Bảng tuần hoàn các nguyên tố hóa học hiện đại ngày nay được xây dựng dựa trên cơ sở mối liên hệ giữa
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Bảng tuần hoàn các nguyên tố hóa học hiện đại ngày nay được xây dựng dựa trên cơ sở mối liên hệ giữa số hiệu nguyên tử và tính chất của các nguyên tố, các nguyên tố được sắp xếp theo thứ tự tăng dần của số hiệu nguyên tử.
Câu 4:
Số thứ tự của một ô nguyên tố bằng
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Số thứ tự của một ô nguyên tố bằng số hiệu nguyên tử của nguyên tố hóa học trong ô đó.
Câu 5:
Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một hàng, gọi là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một hàng, gọi là chu kì.
Câu 6:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Bảng tuần hoàn gồm có 7 chu kì:
3 chu kì nhỏ là các chu kì 1; 2 và 3.
4 chu kì lớn là các chu kì 4; 5; 6 và 7.
Câu 7:
Nguyên tố có số hiệu nguyên tử là 19 thuộc chu kì nào trong bảng tuần hoàn?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Nguyên tố có số hiệu nguyên tử là 19 ⇒ Cấu hình electron: 1s22s22p63s23p64s1
⇒ Có 4 lớp electron.
Mà số thứ tự chu kì = số lớp electron
Do đó, thứ tự chu kì = số lớp electron = 4
Vậy nguyên tố có số hiệu nguyên tử là 19 thuộc chu kì 4 trong bảng tuần hoàn.
Câu 8:
Các electron có khả năng tham gia hình thành liên kết hóa học là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Các electron có khả năng tham gia hình thành liên kết hóa học là electron hóa trị.
Chúng thường nằm ở lớp ngoài cùng hoặc cả phân lớp sát lớp ngoài cùng nếu phân lớp đó chưa bão hòa.
Câu 9:
Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn là:
- Các nguyên tố được xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử
- Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp cùng một chu kì
- Các nguyên tố mà nguyên tử có cấu hình electron tương tự nhau được xếp cùng một nhóm.
Câu 10:
Nguyên tố aluminium (Al) có số hiệu nguyên tử là 13. Al thuộc khối nguyên tố
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Cấu hình electron nguyên tử của Al là: 1s22s22p63s23p1⇒ cấu hình electron lớp ngoài cùng là 3s23p1.
Nên Al thuộc khối nguyên tố p.
Câu 11:
Nguyên tố Y (Z = 17). Trong bảng tuần hoàn, Y thuộc nhóm
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Nguyên tố Y (Z = 17) ⇒ Cấu hình electron: 1s22s22p63s23p5
⇒ cấu hình electron lớp ngoài cùng là 3s23p5.
Nên Y thuộc khối nguyên tố p ⇒ Y thuộc nhóm A.
Số thứ tự nhóm A = số electron lớp ngoài cùng = 2 + 5 = 7
Vậy Y thuộc nhóm VIIA.
Câu 12:
Nguyên tố Y ở chu kì 3 nhóm IVA. Cấu hình electron nguyên tử của Y là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Nguyên tố Y ở chu kì 3 ⇒ Y có 3 lớp electron
Nhóm IVA nên cấu hình electron lớp ngoài cùng có dạng 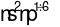 và có 4 electron lớp ngoài cùng ⇒ cấu hình electron lớp ngoài cùng có dạng ns2np2
và có 4 electron lớp ngoài cùng ⇒ cấu hình electron lớp ngoài cùng có dạng ns2np2
Cấu hình electron nguyên tử của Y là: 1s22s22p63s23p2
Câu 13:
Cho nguyên tố X có số hiệu nguyên tử là 23. Vị trí của X trong bảng tuần hoàn là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
ZX= 23 ⇒ Cấu hình electron nguyên tử của X: 1s22s22p63s23p63d34s2
ZX= 23 ⇒ X ở ô số 23
X có 4 lớp electron ⇒ X ở chu kì 4
Phân lớp 3d có mức năng lượng cao nhất ⇒ X là nguyên tố d ⇒ X thuộc nhóm B
Số thứ tự nhóm B = số electron hóa trị
= số electron lớp ngoài cùng + số electron ở phân lớp sát lớp ngoài cùng chưa bão hòa
= 2 + 3 = 5
Vậy X ở ô số 23, chu kì 4, nhóm VB.
Câu 14:
Argon (Ar) có số hiệu nguyên tử là 18. Ar là nguyên tố
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Argon (Ar) có số hiệu nguyên tử là 18 ⇒ Cấu hình electron nguyên tử của Ar: 1s22s22p63s23p6
⇒ có 8 electron lớp ngoài cùng ⇒ Ar là nguyên tố khí hiếm.
Câu 15:
Cấu hình electron của nguyên tố khí hiếm thuộc chu kì 2 là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Nguyên tố thuộc chu kì 2 ⇒ có 2 lớp electron.
Nguyên tố kí hiếm từ chu kì 2 trở đi có 8 electron lớp ngoài cùng.
⇒Cấu hình electron lớp ngoài cùng là: 2s22p6
⇒ Cấu hình electron: 1s22s22p6.
